1 . 下列有关铁及其化合物的说法错误的是
| A.将饱和氯化铁溶液滴入沸水中继续煮沸,可得到红褐色分散系 |
B. 既有氧化性又能被某些氧化剂氧化 既有氧化性又能被某些氧化剂氧化 |
| C.铁是地壳中含量最多的金属元素 |
| D.若人体摄取的铁量不足,则易导致缺铁性贫血 |
您最近一年使用:0次
2021-12-29更新
|
51次组卷
|
3卷引用:吉林油田高级中学2021-2022学年高一上学期期中考试化学试题
名校
解题方法
2 . 下列有关胶体的说法错误 的是
| A.将饱和FeCl3溶液逐滴加入沸水中可制得Fe(OH)3胶体 |
| B.胶体与其它分散系的本质区别是分散质粒子直径大小不同 |
| C.向Fe(OH)3胶体中加入K2SO4溶液,有沉淀析出 |
| D.在通电的情况下,Fe(OH)3胶粒向与直流电源正极相连的一极移动 |
您最近一年使用:0次
名校
解题方法
3 . 下列实验过程可以达到实验目的的是
| 编号 | 实验目的 | 实验过程 |
| A | 检验FeCl2溶液中的Fe2+ | 取少量样品溶液于试管,加入少量酸性KMnO4溶液 |
| B | 制备Fe(OH)3胶体 | 将NaOH浓溶液滴加到饱和FeCl3溶液中 |
| C | 制取干燥纯净的氢气 | 向稀盐酸中加入锌粒,将生成的气体依次通过浓硫酸、NaOH溶液,然后收集 |
| D | 探究维生素C的还原性 | 向盛有2mL氯化铁溶液的试管中滴加浓的维生素C溶液,观察颜色变化 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2021-11-17更新
|
459次组卷
|
2卷引用:吉林省长春外国语学校2021-2022学年高一上学期第二次月考化学试题
名校
解题方法
4 . 下列有关说法错误的是
| A.清晨在树林中有可能观察到丁达尔效应 |
| B.一般情况下溶液中的溶质不会自动与溶剂分离 |
| C.分散质粒子直径在1×10-7~1×10-5cm的分散系叫做胶体 |
| D.饱和氯化铁溶液加热煮沸可制得Fe(OH)3胶体 |
您最近一年使用:0次
2021-11-11更新
|
92次组卷
|
2卷引用:吉林省长春市第二实验中学2021-2022学年高一上学期期中考试化学试题
名校
5 . 下列实验不能达到实验目的的是
| A.证明氯化钠是电解质 | B.证明酸性高锰酸钾有氧化性 | C.从食盐水中获取氯化钠 | D.制备氢氧化铁胶体 |
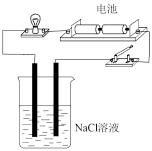 | 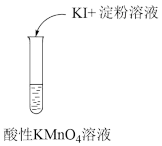 | 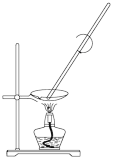 | 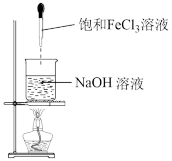 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2021-11-07更新
|
290次组卷
|
2卷引用:吉林省长春市东北师范大学附属中学2022-2023学年高一上学期阶段考试化学试题
名校
解题方法
6 . 现有如下物质:①液态HCl②NaHCO3固体③FeCl3溶液④CO2⑤BaSO4固体⑥Ba(OH)2固体⑦熔融KCl⑧Cu⑨酒精溶液。回答下列问题:
(1)以上物质能导电的是___________ (填序号);
(2)所给物质中的两种物质在水溶液中发生反应,离子方程式为:H++OH-=H2O,该反应的化学方程式为___________ ;
(3)⑤在水中的电离方程式为:___________ ;
(4)胃液中含有盐酸,胃酸过多的人可服用适量的②治疗胃酸过多,写出反应的离子方程式:___________ ;
(5)向⑥的溶液中通入少量④,写出反应的离子方程式___________ ;
(6)将③的饱和溶液分别滴入下述液体中,能形成胶体的是___________;
(1)以上物质能导电的是
(2)所给物质中的两种物质在水溶液中发生反应,离子方程式为:H++OH-=H2O,该反应的化学方程式为
(3)⑤在水中的电离方程式为:
(4)胃液中含有盐酸,胃酸过多的人可服用适量的②治疗胃酸过多,写出反应的离子方程式:
(5)向⑥的溶液中通入少量④,写出反应的离子方程式
(6)将③的饱和溶液分别滴入下述液体中,能形成胶体的是___________;
| A.冷水 | B.沸水 | C.NaOH溶液 | D.氨水 |
您最近一年使用:0次
名校
7 . 水解原理在生产和生活中都具有重要的用途。下列应用与盐类的水解无关的是
| A.TiCl4溶于大量水加热制备TiO2 |
| B.热的纯碱溶液用于清洗油污 |
| C.次氯酸钠常用作消毒剂 |
| D.FeCl3饱和溶液滴入沸水中制Fe(OH)3胶体 |
您最近一年使用:0次
2021-11-04更新
|
254次组卷
|
4卷引用:吉林省白城市第一中学2021-2022学年高二上学期期中考试化学试题
8 . 含铁元素的物质有很多,在生产、生活中应用广泛。
(1)取少量某油漆的原料Fe2O3(红棕色粉末),加入适量浓盐酸,反应后得到棕黄色溶液,取少量棕黄色溶液置于试管中再滴入NaOH溶液,可观察到有沉淀生成,生成沉淀的离子方程式为_______ ,
(2)另在小烧杯中加入20mL蒸馏水,加热至沸腾后,向沸水中滴入2mL上述棕黄色溶液,继续加热至液体呈红褐色,此时体系无浑浊,停止加热,生成红褐色物质的离子方程式:___________ 。
(3)若需分离提纯该物质,可使用如下装置:
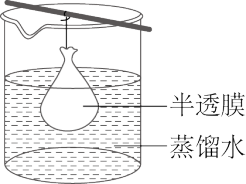
半透膜袋内外物质最本质的区别是___________ 。
A.分散质粒子直径大小 B.丁达尔效应 C.是否能透过半透膜
(1)取少量某油漆的原料Fe2O3(红棕色粉末),加入适量浓盐酸,反应后得到棕黄色溶液,取少量棕黄色溶液置于试管中再滴入NaOH溶液,可观察到有沉淀生成,生成沉淀的离子方程式为
(2)另在小烧杯中加入20mL蒸馏水,加热至沸腾后,向沸水中滴入2mL上述棕黄色溶液,继续加热至液体呈红褐色,此时体系无浑浊,停止加热,生成红褐色物质的离子方程式:
(3)若需分离提纯该物质,可使用如下装置:

半透膜袋内外物质最本质的区别是
A.分散质粒子直径大小 B.丁达尔效应 C.是否能透过半透膜
您最近一年使用:0次
9 . 请按题目要求完成相应问题:
(1)碳酸钙与稀盐酸反应的离子方程式___ 。
(2)Fe(OH)3胶体制备的离子方程式___ 。
(3)向NaHSO4溶液中逐滴加入Ba(OH)2溶液至中性,请写出发生反应的离子方程式___ 。在以上中性溶液中,继续滴加Ba(OH)2溶液,发生反应的离子方程式___ 。
(1)碳酸钙与稀盐酸反应的离子方程式
(2)Fe(OH)3胶体制备的离子方程式
(3)向NaHSO4溶液中逐滴加入Ba(OH)2溶液至中性,请写出发生反应的离子方程式
您最近一年使用:0次
名校
解题方法
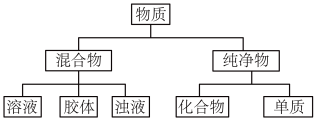
10 . 物质可根据其组成和性质进行分类:___ 。
(2)人体胃液中含有胃酸(0.2%~0.4%的盐酸),起杀菌、帮助消化等作用,但胃酸的量不能过多或过少,它必须控制在一定范围内。当胃酸过多时就会出现“吐酸水”“烧心”“胃部隐隐作痛”等症状。目前市场上的抗酸药主要有:①吸收性抗酸药,如NaHCO3等;②非吸收性抗酸药,如CaCO3、MgO等。
①将上述所举抗酸药填入表对应类别,属于盐的有___ ,属于氧化物的有___ 。
②写出CaCO3与胃酸反应的化学方程式:___ 。
(3)写出制备氢氧化铁胶体的化学方程式:___ ,胶体和溶液的本质区别是___ 。
(2)人体胃液中含有胃酸(0.2%~0.4%的盐酸),起杀菌、帮助消化等作用,但胃酸的量不能过多或过少,它必须控制在一定范围内。当胃酸过多时就会出现“吐酸水”“烧心”“胃部隐隐作痛”等症状。目前市场上的抗酸药主要有:①吸收性抗酸药,如NaHCO3等;②非吸收性抗酸药,如CaCO3、MgO等。
①将上述所举抗酸药填入表对应类别,属于盐的有
②写出CaCO3与胃酸反应的化学方程式:
(3)写出制备氢氧化铁胶体的化学方程式:
您最近一年使用:0次
2021-10-19更新
|
146次组卷
|
2卷引用:吉林省长春市第二十九中学2021-2022学年高一上学期第一次月考化学试题



