名校
解题方法
1 . 用铁铝合金片制造的铁心,涡流损耗小,重量较轻,有良好的耐中子辐射性能。下列关于铁、铝两种元素的说法中错误的是
| A.Fe(OH)3和Al(OH)3都不溶于氨水 |
| B.常温下,浓硫酸可用铝制或者铁制容器贮存、运输 |
| C.控制发生条件,可将铁盐和铝盐转化为Fe(OH)3和Al(OH)3胶体 |
| D.两金属与稀硫酸反应,若消耗金属的物质的量相等,则产生气体的量一定相等 |
您最近一年使用:0次
解题方法
2 . 化学是以实验为主的自然科学,实验操作有严格的规范。下列实验操作的描述错误的是
| A.向沸水中滴加饱和FeCl3溶液,用玻璃棒不断搅拌并继续煮沸至溶液呈透明的红褐色即可制得氢氧化铁胶体 |
| B.配制一定体积某浓度的稀硫酸,将浓硫酸稀释后立即转移入容量瓶并定容,所配溶液浓度偏大 |
| C.容量瓶检漏方法:向容量瓶中加水,塞好瓶塞,将容量瓶倒转过来,若不漏水,将容量瓶正立后,将瓶塞旋转180°,再倒转,看是否漏水 |
| D.用质量分数为98%,密度为1.84g·mL-1浓硫酸,配240mL 2mol·L-1稀硫酸,需用量筒量取浓硫酸26.1mL |
您最近一年使用:0次
3 . 生活处处有化学,化学知识无处不在。用所学知识解释工业、生产、生活与科研中的相关现象。
(1)写出H2C2O4在溶液中发生第一步电离的方程式:_______ ,写出该步电离常数的表达式Ka1=_______ 。
(2)水的离子积表达式Kw=_______ 。常温下0.01 mol/L HCl 溶液的水电离出的 c(H +)=_______ pH=11的CH3 COONa 溶液中由水电离产生的 c(OH-)=_______ 。
(3)CH3COONa溶液呈碱性的原因_______ (用离子方程式)。
(4)将饱和FeCl3的水溶液加入沸水中可以制备胶体,原因是:_______ (用离子方程式表示)。如果加热制备所得胶体,观察到颜色变化为_______ 。
(5)学过的平衡常数有化学平衡常数(K)、电离平衡常数(Ka\Kb)、水的离子积常数(Kw)、盐的水解常数(Kh),后面还会学习沉淀溶解平衡,其常数叫溶度积Ksp。其实这些常数有很多相似之处。任写一点_______ 。(符合题意的答案,均可给分)
(6)如除去MgCl2溶液中Fe3+需要的除杂试剂是_______ 。
(7)泡沫灭火器中筒体内的硫酸铝酸性溶液与碳酸氢钠碱性溶液混合发生化学反应,将生成的泡沫压出喷嘴, 喷射出去进行灭火的。写出对应的离子方程式_______ 。
(1)写出H2C2O4在溶液中发生第一步电离的方程式:
(2)水的离子积表达式Kw=
(3)CH3COONa溶液呈碱性的原因
(4)将饱和FeCl3的水溶液加入沸水中可以制备胶体,原因是:
(5)学过的平衡常数有化学平衡常数(K)、电离平衡常数(Ka\Kb)、水的离子积常数(Kw)、盐的水解常数(Kh),后面还会学习沉淀溶解平衡,其常数叫溶度积Ksp。其实这些常数有很多相似之处。任写一点
(6)如除去MgCl2溶液中Fe3+需要的除杂试剂是
(7)泡沫灭火器中筒体内的硫酸铝酸性溶液与碳酸氢钠碱性溶液混合发生化学反应,将生成的泡沫压出喷嘴, 喷射出去进行灭火的。写出对应的离子方程式
您最近一年使用:0次
4 . Ⅰ.物质性质研究是化学研究的一项重要内容,按要求回答下列问题:
有下列物质:①熔融 ;②
;② 固体;③盐酸;④
固体;③盐酸;④ ;⑤
;⑤ 溶液;⑥
溶液;⑥ ;⑦蔗糖。请用序号填空:
;⑦蔗糖。请用序号填空:
(1)上述状态下的物质可导电的是______ (填序号,下同),属于非电解质的是______ ;
(2)②属于______ (填“酸”、“碱”或“盐”),请写出②在熔融状态下的电离方程式____________ 。
(3)写出①的溶液与③反应的离子方程式____________ 。
Ⅱ.按题目要求填空:
(4)将饱和 滴入沸水中,制备氢氧化铁胶体的化学方程式:
滴入沸水中,制备氢氧化铁胶体的化学方程式:____________ ;
(5)如何除去碳酸钠固体中的碳酸氢钠,相关化学方程式为____________ ;
(6)已知 属于二元酸,请写出
属于二元酸,请写出 与过量氢氧化钠溶液反应的化学方程式为
与过量氢氧化钠溶液反应的化学方程式为____________ 。
有下列物质:①熔融
 ;②
;② 固体;③盐酸;④
固体;③盐酸;④ ;⑤
;⑤ 溶液;⑥
溶液;⑥ ;⑦蔗糖。请用序号填空:
;⑦蔗糖。请用序号填空:(1)上述状态下的物质可导电的是
(2)②属于
(3)写出①的溶液与③反应的离子方程式
Ⅱ.按题目要求填空:
(4)将饱和
 滴入沸水中,制备氢氧化铁胶体的化学方程式:
滴入沸水中,制备氢氧化铁胶体的化学方程式:(5)如何除去碳酸钠固体中的碳酸氢钠,相关化学方程式为
(6)已知
 属于二元酸,请写出
属于二元酸,请写出 与过量氢氧化钠溶液反应的化学方程式为
与过量氢氧化钠溶液反应的化学方程式为
您最近一年使用:0次
解题方法
5 . 在化学活动周中,某校兴趣小组的同学在老师指导下探究铁元素相关物质的性质。回答下列问题:
(1)实验室现有一瓶 饱和溶液,甲同学向
饱和溶液,甲同学向 沸水中逐滴加入
沸水中逐滴加入 饱和溶液,煮沸至液体呈红褐色,停止加热,写出此过程中的离子方程式
饱和溶液,煮沸至液体呈红褐色,停止加热,写出此过程中的离子方程式_______ 。为了证明制得的红褐色液体属于胶体,可以使用的方法是_______ ;乙同学将少量钠单质投入氯化铁溶液中制得铁单质,请评价这一实验方案的可行性_______ (若可行,请写出发生反应的离子方程式,若不可行,请说明理由)。
(2)丙同学意图用干燥、纯净的一氧化碳还原氧化铁。实验装置如图,其中装置 是实验室用草酸
是实验室用草酸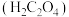 和浓硫酸加热制取一氧化碳的气体发生装置,反应的化学方程式是:
和浓硫酸加热制取一氧化碳的气体发生装置,反应的化学方程式是:
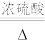
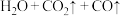 。
。
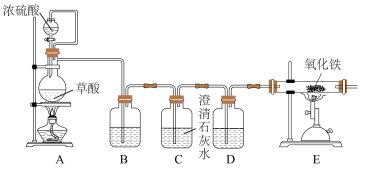
①装置B中盛放的药品为_______ ,装置D的作用为_______ 。
②在实验开始前,应先打开装置_______ (选填“A”或“E”)中的加热装置。写出装置 中发生反应的化学方程式并用双线桥法标出电子转移
中发生反应的化学方程式并用双线桥法标出电子转移_______ ,其中氧化产物与还原产物的质量比为_______ 。
③该装置的主要缺陷是_______ 。
(1)实验室现有一瓶
 饱和溶液,甲同学向
饱和溶液,甲同学向 沸水中逐滴加入
沸水中逐滴加入 饱和溶液,煮沸至液体呈红褐色,停止加热,写出此过程中的离子方程式
饱和溶液,煮沸至液体呈红褐色,停止加热,写出此过程中的离子方程式(2)丙同学意图用干燥、纯净的一氧化碳还原氧化铁。实验装置如图,其中装置
 是实验室用草酸
是实验室用草酸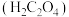 和浓硫酸加热制取一氧化碳的气体发生装置,反应的化学方程式是:
和浓硫酸加热制取一氧化碳的气体发生装置,反应的化学方程式是:
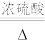
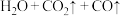 。
。
①装置B中盛放的药品为
②在实验开始前,应先打开装置
 中发生反应的化学方程式并用双线桥法标出电子转移
中发生反应的化学方程式并用双线桥法标出电子转移③该装置的主要缺陷是
您最近一年使用:0次
名校
解题方法
6 . “价-类”二维图是研究物质性质的常用工具,下图是铁元素的部分“价-类”二维图。回答下列问题:

(1) 是一种用途广泛的盐类物质。
是一种用途广泛的盐类物质。
①用煤埚钳夹住一束铁丝,灼烧后立即放入充满氯气的集气瓶中,观察到的现象是___________ ,发生反应的化学方程式为___________ 。
②实验室中制取 胶体的步骤依次为:a.用洁净的烧杯取少量蒸馏水;b.用酒精灯加热至沸腾;c.………;d.至液体呈透明的红褐色。其中步骤c是
胶体的步骤依次为:a.用洁净的烧杯取少量蒸馏水;b.用酒精灯加热至沸腾;c.………;d.至液体呈透明的红褐色。其中步骤c是___________ ,证明胶体制备成功的实验是___________ 。
(2)写出一个能生成 且属于氧化还原反应的化学方程式
且属于氧化还原反应的化学方程式___________ 。
(3)根据上述“价-类”二维图,判断 中Fe元素价态有
中Fe元素价态有___________ ,写出 与稀盐酸反应的离子方程式
与稀盐酸反应的离子方程式___________ 。

(1)
 是一种用途广泛的盐类物质。
是一种用途广泛的盐类物质。①用煤埚钳夹住一束铁丝,灼烧后立即放入充满氯气的集气瓶中,观察到的现象是
②实验室中制取
 胶体的步骤依次为:a.用洁净的烧杯取少量蒸馏水;b.用酒精灯加热至沸腾;c.………;d.至液体呈透明的红褐色。其中步骤c是
胶体的步骤依次为:a.用洁净的烧杯取少量蒸馏水;b.用酒精灯加热至沸腾;c.………;d.至液体呈透明的红褐色。其中步骤c是(2)写出一个能生成
 且属于氧化还原反应的化学方程式
且属于氧化还原反应的化学方程式(3)根据上述“价-类”二维图,判断
 中Fe元素价态有
中Fe元素价态有 与稀盐酸反应的离子方程式
与稀盐酸反应的离子方程式
您最近一年使用:0次
名校
7 . 现代化学在材料、资源、能源、环境、医药、信息技术等领域均有重大应用。
I.新疆也要建造磁悬浮列车了。在磁悬浮列车制造过程中将使用大量含钇(Y)元素的超导材料。钇(Y)元素在元素周期表中的信息如图所示:
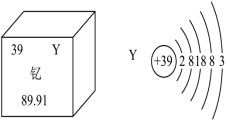
(1)钇原子核内有___________ 个质子,图中89.91表示的是___________ 。
(2)钇元素形成氧化物的化学式是___________ 。
II.电解质是维持人体生理活动的基础之一、请回答下列问题:
①CO2 ②Al ③乙醇 ④Fe(OH)3胶体 ⑤熔融BaSO4 ⑥KOH溶液 ⑦固态
(3)上述物质中属于电解质的是___________ 。(填序号)
(4)属于非电解质的是___________ 。(填序号)
(5)能导电的纯净物是___________ 。(填序号)
(6)写出⑦在水中的电离方程式___________ 。
(7)写出①和⑥的反应方程式___________ 。
(8)请写出实验室中制备Fe(OH)3胶体的化学反应方程式___________ 。
I.新疆也要建造磁悬浮列车了。在磁悬浮列车制造过程中将使用大量含钇(Y)元素的超导材料。钇(Y)元素在元素周期表中的信息如图所示:

(1)钇原子核内有
(2)钇元素形成氧化物的化学式是
II.电解质是维持人体生理活动的基础之一、请回答下列问题:
①CO2 ②Al ③乙醇 ④Fe(OH)3胶体 ⑤熔融BaSO4 ⑥KOH溶液 ⑦固态

(3)上述物质中属于电解质的是
(4)属于非电解质的是
(5)能导电的纯净物是
(6)写出⑦在水中的电离方程式
(7)写出①和⑥的反应方程式
(8)请写出实验室中制备Fe(OH)3胶体的化学反应方程式
您最近一年使用:0次
8 . 氢氧化铁胶体的制备步骤如下:
Ⅰ.用烧杯取少量蒸馏水,放在酒精灯上加热至沸腾;
Ⅱ.向烧杯中逐滴加入饱和FeCl3溶液;
Ⅲ.继续煮沸至液体呈透明的红褐色,即得Fe(OH)3胶体。
(1)确定制备的胶体是否成功,最简单的方法是___________ 。
(2)若向FeCl3溶液中逐滴滴加稀NaOH溶液,并控制溶液的酸碱性,也可制得Fe(OH)3胶体,若要提纯Fe(OH)3胶体可采取的方法是___________ 。
(3)Fe(OH)3胶体与Al(OH)3胶体相似,也具有净水作用,原因是___________ 。
(4)FeCl3与H2O制得胶体的胶团结构为{[Fe(OH)3]m·nFeO+·(n-x)Cl-}x+·xCl-,下列说法正确的是___。

(5)下列现象或新技术应用中,涉及胶体性质的有______。
①使用微波手术刀进行外科手术,可使开刀处的血液迅速凝固而减少出血
②肾功能衰竭等疾病引起的血液中毒,可利用血液透析进行治疗
③使用静电除尘器除去空气中的飘尘粒子
④豆浆中加入石膏后迅速凝固
Ⅰ.用烧杯取少量蒸馏水,放在酒精灯上加热至沸腾;
Ⅱ.向烧杯中逐滴加入饱和FeCl3溶液;
Ⅲ.继续煮沸至液体呈透明的红褐色,即得Fe(OH)3胶体。
(1)确定制备的胶体是否成功,最简单的方法是
(2)若向FeCl3溶液中逐滴滴加稀NaOH溶液,并控制溶液的酸碱性,也可制得Fe(OH)3胶体,若要提纯Fe(OH)3胶体可采取的方法是
(3)Fe(OH)3胶体与Al(OH)3胶体相似,也具有净水作用,原因是
(4)FeCl3与H2O制得胶体的胶团结构为{[Fe(OH)3]m·nFeO+·(n-x)Cl-}x+·xCl-,下列说法正确的是___。

| A.Fe(OH)3胶体带正电 |
| B.16.25g FeCl3生成的胶体粒子数为6.02×1022 |
| C.Fe(OH)3胶体粒子的直径可能是5×10-7m |
| D.在U形管中注入Fe(OH)3胶体,插入石墨电极通电,阴极周围颜色加深 |
(5)下列现象或新技术应用中,涉及胶体性质的有______。
①使用微波手术刀进行外科手术,可使开刀处的血液迅速凝固而减少出血
②肾功能衰竭等疾病引起的血液中毒,可利用血液透析进行治疗
③使用静电除尘器除去空气中的飘尘粒子
④豆浆中加入石膏后迅速凝固
| A.1项 | B.2项 | C.3项 | D.4项 |
您最近一年使用:0次
9 . 胶体和溶液、浊液都是我们生活中常见的分散系,具有特殊性质,生活中常利用其性质。
(1)新冠病毒可以通过气溶胶传播,气溶胶属于胶体的一种,下列叙述错误的是________。
实验室可制备 胶体供学生探究胶体的性质,具体操作方法为:沸腾的蒸馏水中逐滴加入饱和
胶体供学生探究胶体的性质,具体操作方法为:沸腾的蒸馏水中逐滴加入饱和 溶液,继续煮沸至烧杯内液体呈均匀红褐色后停止加热。
溶液,继续煮沸至烧杯内液体呈均匀红褐色后停止加热。
(2)以上反应的化学方程式为:___________ 。
(3)某同学在制备过程中未使用洁净的烧杯(残留少量 固体),加水煮沸并滴入饱和
固体),加水煮沸并滴入饱和 后,观察到产生红褐色沉淀,因为
后,观察到产生红褐色沉淀,因为___________ 。
在一篇关于“生活中的胶体”文章中,介绍了如何利用牛奶或淀粉等生活中常见物质制备胶体,如将少量淀粉分散在水中可得无色澄清透明的淀粉溶液。某同学对“淀粉溶液”这种说法产生了疑惑,为探究“淀粉溶液”到底是溶液还是胶体,同学取材于生活常见材料设计了如下实验:
甲同学预先将少量碘酒溶于水,配置成碘水,并准备如图搭建实验装置。

(4)实验前,甲同学设计了如下表格以记录现象并分析结论:
(5)实际实验过程中,同学不仅观察到了如编号2所预测的实验现象,还观察到了半透膜内的淀粉溶液变蓝,从分散质粒径角度分析产生这两个现象的原因:___________ 。
(1)新冠病毒可以通过气溶胶传播,气溶胶属于胶体的一种,下列叙述错误的是________。
| A.胶体金抗原检测试纸保质期较长,体现了胶体的稳定性 |
| B.在电压作用下,带电胶体微粒可以发生电泳 |
| C.溶液呈电中性,而胶体带电,不呈电中性 |
| D.雾是气溶胶,在阳光下可以观察到丁达尔现象 |
实验室可制备
 胶体供学生探究胶体的性质,具体操作方法为:沸腾的蒸馏水中逐滴加入饱和
胶体供学生探究胶体的性质,具体操作方法为:沸腾的蒸馏水中逐滴加入饱和 溶液,继续煮沸至烧杯内液体呈均匀红褐色后停止加热。
溶液,继续煮沸至烧杯内液体呈均匀红褐色后停止加热。(2)以上反应的化学方程式为:
(3)某同学在制备过程中未使用洁净的烧杯(残留少量
 固体),加水煮沸并滴入饱和
固体),加水煮沸并滴入饱和 后,观察到产生红褐色沉淀,因为
后,观察到产生红褐色沉淀,因为在一篇关于“生活中的胶体”文章中,介绍了如何利用牛奶或淀粉等生活中常见物质制备胶体,如将少量淀粉分散在水中可得无色澄清透明的淀粉溶液。某同学对“淀粉溶液”这种说法产生了疑惑,为探究“淀粉溶液”到底是溶液还是胶体,同学取材于生活常见材料设计了如下实验:
甲同学预先将少量碘酒溶于水,配置成碘水,并准备如图搭建实验装置。

(4)实验前,甲同学设计了如下表格以记录现象并分析结论:
| 编号 | 实验现象 | 实验结论 |
| 1 | 烧杯中溶液呈 | “淀粉溶液”是溶液 |
| 2 | 烧杯中溶液呈 | “淀粉溶液”是胶体 |
(5)实际实验过程中,同学不仅观察到了如编号2所预测的实验现象,还观察到了半透膜内的淀粉溶液变蓝,从分散质粒径角度分析产生这两个现象的原因:
您最近一年使用:0次
解题方法
10 . 2023年诺贝尔化学奖授予蒙吉·巴文迪、路易斯·布鲁斯和阿列克谢·叶基莫夫,以表彰他们在“发现和开发量子点”方面做出的贡献。这些被称为量子点的粒子直径只有1~10nm,在未来,它们可以为柔性电子产品、微型传感器、更薄的太阳能电池和加密的量子通信做出贡献。下列说法不正确的是
| A.把这些被称为量子点的粒子分散到分散剂中形成的是胶体 |
| B.云是气溶胶,有色玻璃是固溶胶 |
| C.长江三角洲的形成是由于胶体的聚沉,这说明胶体不均一、不稳定 |
| D.可用半透膜分离溶液和胶体 |
您最近一年使用:0次



