解题方法
1 . 下列说法不正确 的是
A.Fe2+的价层电子轨道表示式为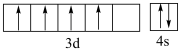 |
B.用电子式表示K2S的形成: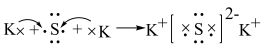 |
| C.HClO的分子的VSEPR模型为四面体形 |
D.聚己二酰己二胺的结构简式: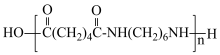 |
您最近一年使用:0次
2 . 催化热解 可同时回收
可同时回收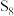 (结构为
(结构为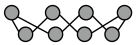 )和
)和 。下列说法正确的是
。下列说法正确的是
A.中子数为17的硫原子为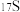 |
B. 的电子式为 的电子式为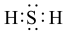 |
C.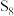 固态时为共价晶体 固态时为共价晶体 |
D. 分子中含有 分子中含有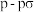 键 键 |
您最近一年使用:0次
3 . 合成氨反应的微观过程如下图所示。下列说法不正确 的是
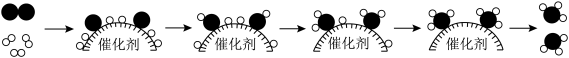
A. 的结构式为 的结构式为 |
B.在反应过程中,逐步产生NH、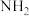 等原子团 等原子团 |
| C.在反应过程中,有非极性共价键断裂和形成 |
D.选择合适的条件,通入1mol  和3mol 和3mol  ,最终所得 ,最终所得 |
您最近一年使用:0次
解题方法
4 . 为证明卤族元素的非金属性强弱,某小组用下图所示装置进行实验(夹持仪器已略去,气密性已检查)。
已知:①溴水呈黄色,而且颜色随浓度增大而加深。
② 容易从水中转移到
容易从水中转移到 中,导致下层(
中,导致下层( 层)因溶有
层)因溶有 显紫色。
显紫色。
实验过程:
①打开弹簧夹,打开活塞a,滴加浓盐酸。
②当B和C中的溶液都变为黄色时,夹紧弹簧夹。
③当B中溶液黄色加深时关闭活塞a。
④……
(1)NaOH的电子式为___________ 。
(2)A装置中制备氯气的离子方程式为___________ ,HCl的作用是做___________ 。
(3)B装置中主要反应的化学方程式为___________ 。
(4)为验证溴的氧化性强于碘,过程④的操作和现象分别是___________ 。
(5)过程③的实验目的是___________ 。
(6)结合元素周期表,从原子结构的角度解释氯、溴、碘单质的氧化性逐渐减弱的原因:___________ 。
(7)下列事实能说明元素Y的非金属性比硫元素强的是___________ 。
a.Y单质通入 溶液中,溶液出现淡黄色浑浊
溶液中,溶液出现淡黄色浑浊
b.与 反应时,1mol Y单质得到的电子比1mol S多
反应时,1mol Y单质得到的电子比1mol S多
c.Y和S的简单氢化物受热时,前者的分解温度较高
d.Y元素的氧化物对应水化物的酸性比S强
已知:①溴水呈黄色,而且颜色随浓度增大而加深。
②
 容易从水中转移到
容易从水中转移到 中,导致下层(
中,导致下层( 层)因溶有
层)因溶有 显紫色。
显紫色。实验过程:
①打开弹簧夹,打开活塞a,滴加浓盐酸。
②当B和C中的溶液都变为黄色时,夹紧弹簧夹。
③当B中溶液黄色加深时关闭活塞a。
④……
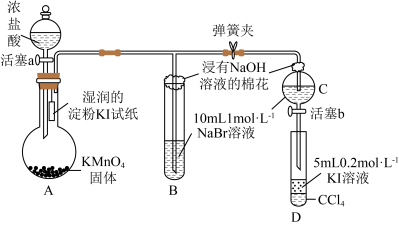
(1)NaOH的电子式为
(2)A装置中制备氯气的离子方程式为
(3)B装置中主要反应的化学方程式为
(4)为验证溴的氧化性强于碘,过程④的操作和现象分别是
(5)过程③的实验目的是
(6)结合元素周期表,从原子结构的角度解释氯、溴、碘单质的氧化性逐渐减弱的原因:
(7)下列事实能说明元素Y的非金属性比硫元素强的是
a.Y单质通入
 溶液中,溶液出现淡黄色浑浊
溶液中,溶液出现淡黄色浑浊b.与
 反应时,1mol Y单质得到的电子比1mol S多
反应时,1mol Y单质得到的电子比1mol S多c.Y和S的简单氢化物受热时,前者的分解温度较高
d.Y元素的氧化物对应水化物的酸性比S强
您最近一年使用:0次
5 . 反应CO2+NH3+H2O+NaCl=NaHCO3↓+NH4Cl是侯氏制碱法的原理。下列说法正确的是
A.H2O的电子式为: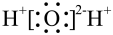 |
B.CO2的空间填充模型: |
C.中子数为20的氯原子: |
D. 的结构示意图: 的结构示意图: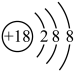 |
您最近一年使用:0次
名校
6 . 下列有关化学用语的表示正确的是
| A.N2的结构式:N=N | B.NH3的电子式: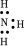 |
C.中子数为18的氯原子: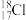 | D.氯化铵的电离方程式:NH4Cl= +Cl- +Cl- |
您最近一年使用:0次
解题方法
7 . 以乙炔为原料制备草酸(H2C2O4),反应原理为: 。下列说法正确的是
。下列说法正确的是
 。下列说法正确的是
。下列说法正确的是A.乙炔的比例模型示意图为 |
| B.草酸分子中C元素的化合价为+3 |
C.H2O的电子式为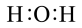 |
| D.乙炔与氢气1︰1反应产物的结构简式为CH2CH2 |
您最近一年使用:0次
名校
解题方法
8 . 下列化学用语表达正确的是
A.F原子的核外电子排布式: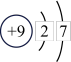 | B. 的轨道表示式: 的轨道表示式: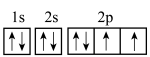 |
C. 分子的结构式: 分子的结构式: | D.Mn的简化电子排布式:[Ar]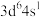 |
您最近一年使用:0次
9 . 下列化学用语正确的是
A.镁原子最外层电子云轮廓图: |
B. 的结构示意图: 的结构示意图: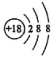 |
C. 的电子式为: 的电子式为: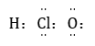 |
D.基态碳原子最外层电子的轨道表示式: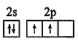 |
您最近一年使用:0次
名校
10 .  是一种漂白剂,它漂白的原理是
是一种漂白剂,它漂白的原理是 ,下列说法正确的是
,下列说法正确的是
 是一种漂白剂,它漂白的原理是
是一种漂白剂,它漂白的原理是 ,下列说法正确的是
,下列说法正确的是A. 是离子化合物 是离子化合物 | B. 的电子式为 的电子式为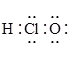 |
C. 是弱碱 是弱碱 | D.中子数为8的氧原子: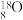 |
您最近一年使用:0次



