解题方法
1 . 第三代半导体材料氮化镓(GaN)有多种制备方法:
方法Ⅰ: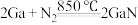
方法Ⅱ: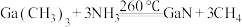
方法Ⅲ: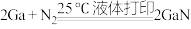
(1)基态 的核外电子排布式为
的核外电子排布式为___________ 。
(2)氨气、甲烷中心原子的杂化方式是___________ ,分子构型分别为___________ 、___________ 。氨气熔沸点高于甲烷,是因为固体、液态氨气分子中存在氢键。在固体氨中每个氨气分子与6个氨气形成氢键,请画出其氢键___________ 。
(3)方法Ⅰ比方法Ⅱ温度高的主要原因是(从结构上解释)___________ 。
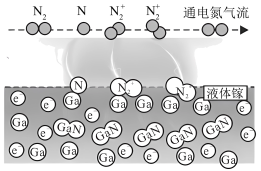
(4)方法Ⅲ中,通电氮气流中存在N、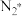 、
、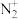 活化粒子,常温下就能与液体镓反应(如图所示)。
活化粒子,常温下就能与液体镓反应(如图所示)。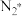 、
、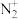 电子式分别为
电子式分别为___________ 、___________ ,1mol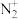 完全反应得到
完全反应得到___________ mol 。
。
(5)对高温GaN熔液慢速降温,至2950K时形成结晶。科学家展示了从中截取厚度为1.5个原子厚度的微观结构截面图(如下所示):

区域1、区域2分别为氮化镓___________ 、___________ (填“结构A”或“结构B”)的结构。
方法Ⅰ:
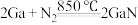
方法Ⅱ:
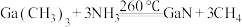
方法Ⅲ:
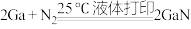
(1)基态
 的核外电子排布式为
的核外电子排布式为(2)氨气、甲烷中心原子的杂化方式是
(3)方法Ⅰ比方法Ⅱ温度高的主要原因是(从结构上解释)
(4)方法Ⅲ中,通电氮气流中存在N、
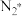 、
、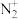 活化粒子,常温下就能与液体镓反应(如图所示)。
活化粒子,常温下就能与液体镓反应(如图所示)。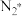 、
、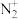 电子式分别为
电子式分别为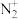 完全反应得到
完全反应得到 。
。
(5)对高温GaN熔液慢速降温,至2950K时形成结晶。科学家展示了从中截取厚度为1.5个原子厚度的微观结构截面图(如下所示):

区域1、区域2分别为氮化镓
您最近一年使用:0次
2 . CaCN2曾经直接用作肥料。在自然界中,它与水反应产生肥料,在此过程中会涉及到下面一些步骤:
第一步水解,CaCN2与H2O以1:1(物质的量比)反应,生成两种中间体A和B,它们都是含钙的离子化合物,这步反应可以描述为简单的酸碱反应。化合物A和B在热力学上不稳定,受热很容易分解。
化合物A热分解生成离子化合物C和共价化合物D,A与CO2反应,生成共价化合物D和新的离子化合物E。E热分解得到化合物C和CO2。化合物B与CO2、H2O反应生成E和新的共价化合物F,F简单水解(以1:1物质的量比),产生共价化合物G;G常用作肥料,G彻底水解生成CO2和另一种气体H。试回答下列问题:
(1)试画出CaCN2中阴离子的共振结构式与共轭结构式:___ 、___ 。
(2)试写出字母A~H所代表物质的化学式:A___ 、B___ 、C___ 、D___ 、E___ 、F___ 、G___ 、H___ 。
(3)写出该问题中描述的下列有关反应的化学方程式:
CaCN2与H2O反应:___ ;
化合物A热分解:___ ;
化合物B与CO2、H2O反应___ ;
G彻底水解生成CO2和另一种气体H:___ 。
(4)画出G的Lewis结构式:___ 。
(5)F的结构式是___ ,画出其三种异构体的结构式(不考虑三元环)并命名:___ 。
第一步水解,CaCN2与H2O以1:1(物质的量比)反应,生成两种中间体A和B,它们都是含钙的离子化合物,这步反应可以描述为简单的酸碱反应。化合物A和B在热力学上不稳定,受热很容易分解。
化合物A热分解生成离子化合物C和共价化合物D,A与CO2反应,生成共价化合物D和新的离子化合物E。E热分解得到化合物C和CO2。化合物B与CO2、H2O反应生成E和新的共价化合物F,F简单水解(以1:1物质的量比),产生共价化合物G;G常用作肥料,G彻底水解生成CO2和另一种气体H。试回答下列问题:
(1)试画出CaCN2中阴离子的共振结构式与共轭结构式:
(2)试写出字母A~H所代表物质的化学式:A
(3)写出该问题中描述的下列有关反应的化学方程式:
CaCN2与H2O反应:
化合物A热分解:
化合物B与CO2、H2O反应
G彻底水解生成CO2和另一种气体H:
(4)画出G的Lewis结构式:
(5)F的结构式是
您最近一年使用:0次
解题方法
3 . 美国和欧洲的科学家合作,在同温层发现破坏臭氧的C12O2。在该化合物中,氯的氧化数为_______ ,氧的氧化数为_______ 。Cl2O2的Lewis结构式为_______ ,该分子中所有原子_______ (填:共或不共)平面。
您最近一年使用:0次



