名校
1 . 向蔗糖(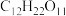 )中滴入98%的浓硫酸,蔗糖会变成疏松的“炭块”,同时产生
)中滴入98%的浓硫酸,蔗糖会变成疏松的“炭块”,同时产生 ,
, ;
; 可用酸性高锰酸钾溶液吸收。请回答下列问题:
可用酸性高锰酸钾溶液吸收。请回答下列问题:
(1)蔗糖的摩尔质量为______ 。17.1 g 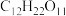 的物质的量为
的物质的量为______ 。
(2)500℃时,34.2 g蔗糖完全燃烧,产生两种气体的体积之比为______ ,其中产生 的体积(折算成标准状况下)为
的体积(折算成标准状况下)为______ L。
(3)质量分数为98%、密度为1.84 g⋅cm 的浓硫酸的物质的量浓度为
的浓硫酸的物质的量浓度为______ mol·L ;酸性高锰酸钾溶液需要用浓度为3 mol⋅L
;酸性高锰酸钾溶液需要用浓度为3 mol⋅L 的硫酸酸化,则实验室配制50 mL该浓度的硫酸需质量分数为98%的浓硫酸
的硫酸酸化,则实验室配制50 mL该浓度的硫酸需质量分数为98%的浓硫酸______ mL,需要用到的定量仪器有______ 。
(4) 被酸性高锰酸钾溶液吸收发生反应的离子方程式为
被酸性高锰酸钾溶液吸收发生反应的离子方程式为______ 。
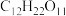 )中滴入98%的浓硫酸,蔗糖会变成疏松的“炭块”,同时产生
)中滴入98%的浓硫酸,蔗糖会变成疏松的“炭块”,同时产生 ,
, ;
; 可用酸性高锰酸钾溶液吸收。请回答下列问题:
可用酸性高锰酸钾溶液吸收。请回答下列问题:(1)蔗糖的摩尔质量为
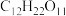 的物质的量为
的物质的量为(2)500℃时,34.2 g蔗糖完全燃烧,产生两种气体的体积之比为
 的体积(折算成标准状况下)为
的体积(折算成标准状况下)为(3)质量分数为98%、密度为1.84 g⋅cm
 的浓硫酸的物质的量浓度为
的浓硫酸的物质的量浓度为 ;酸性高锰酸钾溶液需要用浓度为3 mol⋅L
;酸性高锰酸钾溶液需要用浓度为3 mol⋅L 的硫酸酸化,则实验室配制50 mL该浓度的硫酸需质量分数为98%的浓硫酸
的硫酸酸化,则实验室配制50 mL该浓度的硫酸需质量分数为98%的浓硫酸(4)
 被酸性高锰酸钾溶液吸收发生反应的离子方程式为
被酸性高锰酸钾溶液吸收发生反应的离子方程式为
您最近一年使用:0次
名校
解题方法
2 . CO和CO2的混合气体18g,完全燃烧后测得CO2体积为11.2L(STP),则混合气体的平均摩尔质量是_______ 。
您最近一年使用:0次
解题方法
3 . 交警部门严厉打击酒后驾驶行为。80mg/100mL>血液中酒精含量≥20mg/100mL为饮酒驾驶;血液中酒精含量≥80mg/100mL为醉酒驾驶。K2Cr2O7是一种橙红色的物质,当其中的铬元素被还原成正三价铬时,颜色有明显变化。据此,当交警让司机对填充了吸附有K2Cr2O7的硅胶颗粒的装置(即酒精含量探测器)吹气,发生反应。
(1)该反应中K2Cr2O7跟_______ (写化学式)发生了反应,反应中氧化剂是_______ ;
(2)若交警测得某司机血液中酒精含量为0.01mol∙L-1,即证明司机是_______ 。(填“饮酒驾驶”或“醉酒驾驶”)
(1)该反应中K2Cr2O7跟
(2)若交警测得某司机血液中酒精含量为0.01mol∙L-1,即证明司机是
您最近一年使用:0次
名校
4 . 按要求回答下列问题
(1)金属钙在一定条件下可以与氢气化合生成CaH2(白色固体)。将该白色固体加入滴有酚酞的蒸馏水中,可以观察到有气泡生成,溶液变红。请根据以上事实书写CaH2与水反应的化学方程式,并用单线桥出电子转移方向和数目_______ 。
(2)设NA代表阿伏加德罗常数的数值,一个CO分子的质量可表示为_______ g。
(1)金属钙在一定条件下可以与氢气化合生成CaH2(白色固体)。将该白色固体加入滴有酚酞的蒸馏水中,可以观察到有气泡生成,溶液变红。请根据以上事实书写CaH2与水反应的化学方程式,并用单线桥出电子转移方向和数目
(2)设NA代表阿伏加德罗常数的数值,一个CO分子的质量可表示为
您最近一年使用:0次
名校
5 . 完成下列问题。
(1)已知某非金属元素R的简单气态氢化物的分子式为HmR,则R的化合价为_______ ,若它的最高价氧化物对应的水化物分子中有b个氧原子,则这种酸的分子式为_______ 。
(2)离子化合物A的化学式为NH5,它所有原子的最外层都符合相应的稀有气体原子的最外层结构,请回答:
①适当加热,A就分解为两种气体,其中一种是化合物,该反应的化学方程式为_______ ,所得混合气体的平均摩尔质量为_______ g/mol。
②A溶于水后的溶液中滴加紫色石蕊试液,溶液颜色为_______ 。
③有人认为A是铵盐,这种想法是否正确,说明你的理由_______ 。
(1)已知某非金属元素R的简单气态氢化物的分子式为HmR,则R的化合价为
(2)离子化合物A的化学式为NH5,它所有原子的最外层都符合相应的稀有气体原子的最外层结构,请回答:
①适当加热,A就分解为两种气体,其中一种是化合物,该反应的化学方程式为
②A溶于水后的溶液中滴加紫色石蕊试液,溶液颜色为
③有人认为A是铵盐,这种想法是否正确,说明你的理由
您最近一年使用:0次
2021-09-16更新
|
398次组卷
|
2卷引用:浙江省宁波市镇海中学2020-2021学年高一上学期期末考试化学试卷
解题方法
6 . 物质的量概念建立起物质的微粒与可观察的物理量之间的联系。
(1)碳氢化合物简称为烃,烃种类繁多,其中甲烷CH4是最简单的烃.甲烷的相对分子质量为16,故甲烷的摩尔质量为___ 。
(2)0.01mol•L-1Na2CO3溶液100mL,其中含Na+___ mol;每毫升该溶液中含有Na+__ 个;取15mL0.01mol•L-1Na2CO3溶液加水稀释到75mL,所得Na2CO3溶液浓度为__ mol•L-1。
(3)阿司匹林的分子式为C9H8O4,一个阿司匹林分子的质量是__ g。
(1)碳氢化合物简称为烃,烃种类繁多,其中甲烷CH4是最简单的烃.甲烷的相对分子质量为16,故甲烷的摩尔质量为
(2)0.01mol•L-1Na2CO3溶液100mL,其中含Na+
(3)阿司匹林的分子式为C9H8O4,一个阿司匹林分子的质量是
您最近一年使用:0次
2021-01-31更新
|
315次组卷
|
3卷引用:福建省福州市2020-2021学年高一上学期期末考试化学试题
19-20高二·浙江·期末
7 . 1.某核素 的氯化物
的氯化物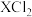 1.11g配成溶液后,需用
1.11g配成溶液后,需用 的硝酸银溶液20mL才能把氯离子完全沉淀下来,试计算:
的硝酸银溶液20mL才能把氯离子完全沉淀下来,试计算:
(1)X的质量数A______________ 。
(2)若X的核内中子数为20,求37g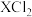 中所含质子的物质的量是
中所含质子的物质的量是______________
2.下列物质中:①酒精 ②氨气 ③硫酸钡 ④铜丝 ⑤二氧化碳 ⑥饱和食盐水 ⑦熔融氯化镁 ⑧醋酸 ⑨氢氧化钠,
(1)属于电解质的是______________ ,属于非电解质的是______________
(2)书写硫酸铁电离方程式:_______________________ 书写氯酸钾电离方程式:_______________________
 的氯化物
的氯化物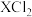 1.11g配成溶液后,需用
1.11g配成溶液后,需用 的硝酸银溶液20mL才能把氯离子完全沉淀下来,试计算:
的硝酸银溶液20mL才能把氯离子完全沉淀下来,试计算:(1)X的质量数A
(2)若X的核内中子数为20,求37g
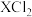 中所含质子的物质的量是
中所含质子的物质的量是2.下列物质中:①酒精 ②氨气 ③硫酸钡 ④铜丝 ⑤二氧化碳 ⑥饱和食盐水 ⑦熔融氯化镁 ⑧醋酸 ⑨氢氧化钠,
(1)属于电解质的是
(2)书写硫酸铁电离方程式:
您最近一年使用:0次
名校
8 . 补充完整下列化学计算公式:
(1)N=________ NA , N表示 ________ ;NA表示 ________ .
(2)________ =n M,n表示_________ m表示 ________ .
(3)V=________ Vm,V表示 ________ ;Vm表示 ________
(4)________ =c V,c表示 ________ ;V的单位为 ________
(1)N=
(2)
(3)V=
(4)
您最近一年使用:0次
9 . 填空:
(1)0. 5 mol NH3分子中所含氮原子数为__________ 个;
(2)1.2g RSO4中含0.01 mol R2+,则RSO4的摩尔质量是__________ ;
(3)0.1 mol·L-1的 Cu(NO3)2溶液中NO3-的物质的量浓度是__________ ;
(4)新制氯水在阳光照射下产生的无色气体是__________ ;
(5)配制100 mL 1 mol/L NaCl溶液,定容后,把容量瓶倒置摇匀后发现液面低于刻度线,补加水至刻度处,会引起所配溶液物质的量浓度__________ (选填“偏高、偏低、无影响”);
(6)实验室制备氯气时,收集氯气常采用__________ 法。
(1)0. 5 mol NH3分子中所含氮原子数为
(2)1.2g RSO4中含0.01 mol R2+,则RSO4的摩尔质量是
(3)0.1 mol·L-1的 Cu(NO3)2溶液中NO3-的物质的量浓度是
(4)新制氯水在阳光照射下产生的无色气体是
(5)配制100 mL 1 mol/L NaCl溶液,定容后,把容量瓶倒置摇匀后发现液面低于刻度线,补加水至刻度处,会引起所配溶液物质的量浓度
(6)实验室制备氯气时,收集氯气常采用
您最近一年使用:0次
名校
10 . 回答下列问题:
(1)标准状况下11.2L NH3中含_________ 个氨分子,____________ mol氢原子。
(2)等质量的SO2和SO3物质的量之比是____________ ;所含的氧原子个数之比是_______ 。
(3)4.8gCH4中所含氢原子数与_____________ g水所含氢原子数相等。
(4)含0.4mol A13+的Al2(SO4)3中所含的 的物质的量是
的物质的量是__________ 。
(5)已知16g A和20g B恰好完全反应生成0.04mol C和31.76g D,则C的摩尔质量为________ 。
(6)在一定的温度和压强下,1体积气体X2跟3体积气体Y2化合生成2体积化合物,则该化合物的化学式是__________ 。
(7)某盐混合溶液中含有离子:Na+、Mg2+、Cl﹣、 ,测得Na+、Mg2+和Cl﹣的物质的量浓度依次为:0.2mol•L﹣1、0.25mol•L﹣1、0.4mol•L﹣1,则c(
,测得Na+、Mg2+和Cl﹣的物质的量浓度依次为:0.2mol•L﹣1、0.25mol•L﹣1、0.4mol•L﹣1,则c( )=
)=________ 。
(1)标准状况下11.2L NH3中含
(2)等质量的SO2和SO3物质的量之比是
(3)4.8gCH4中所含氢原子数与
(4)含0.4mol A13+的Al2(SO4)3中所含的
 的物质的量是
的物质的量是(5)已知16g A和20g B恰好完全反应生成0.04mol C和31.76g D,则C的摩尔质量为
(6)在一定的温度和压强下,1体积气体X2跟3体积气体Y2化合生成2体积化合物,则该化合物的化学式是
(7)某盐混合溶液中含有离子:Na+、Mg2+、Cl﹣、
 ,测得Na+、Mg2+和Cl﹣的物质的量浓度依次为:0.2mol•L﹣1、0.25mol•L﹣1、0.4mol•L﹣1,则c(
,测得Na+、Mg2+和Cl﹣的物质的量浓度依次为:0.2mol•L﹣1、0.25mol•L﹣1、0.4mol•L﹣1,则c( )=
)=
您最近一年使用:0次
2016-12-13更新
|
481次组卷
|
2卷引用:江西省吉安市第三中学2022-2023学年高一上学期期末考试化学试题



