解题方法
1 . 按要求回答下列问题。
(1)15.6gNa2X含Na+的物质的量为0.4mol,则Na2X的摩尔质量为_________ ,若将上述样品溶解于水中配成200mL的溶液,则所得溶液的物质的量浓度为_______ 。
(2)除去Na2CO3粉末中混入的NaHCO3杂质用________ 方法,化学方程式为________ 。
(3)Cl2和SO2都有漂白作用,现将二者以等物质的量混合后再通入品红溶液中,品红溶液将___________ (填“褪色”或“不褪色”),反应方程式为___________ 。
(4)明矾在水中的电离方程式是___________ ,明矾的用途有___________ (写一种即可)。
(5)利用下图装置,写出除去下列气体中的杂质的方法(括号内的气体为杂质),并写出化学方程式。
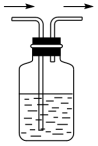
①NO(NO2):___________ ,化学方程式:___________ 。
②CO2(SO2):___________ ,化学方程式:___________ 。
(1)15.6gNa2X含Na+的物质的量为0.4mol,则Na2X的摩尔质量为
(2)除去Na2CO3粉末中混入的NaHCO3杂质用
(3)Cl2和SO2都有漂白作用,现将二者以等物质的量混合后再通入品红溶液中,品红溶液将
(4)明矾在水中的电离方程式是
(5)利用下图装置,写出除去下列气体中的杂质的方法(括号内的气体为杂质),并写出化学方程式。

①NO(NO2):
②CO2(SO2):
您最近一年使用:0次
名校
2 . 碳及其化合物在生产、生活中有广泛的用途。
(1)碳与同周期元素Q的单质化合仅能生成两种常见气态化合物,其中一种化合物R为非极性分子,则Q元素在周期表中的位置为___________ ,R的电子式为___________
(2)一定条件下,Na还原CCl4可制备金刚石,反应结束冷却至室温后,回收CCl4的实验操作名称为___________ ,除去粗产品中少量钠的试剂为___________
(3)碳还原制取金刚砂SiC,其粗产品中杂质为Si和SiO2.先将20.0gSiC粗产品加入到过量NaOH溶液中充分反应,收集到标准状况下2.24 L的氢气,过滤后得SiC固体11.4g,滤液稀释到1L。Si与NaOH溶液反应的离子方程式为___________ ,硅酸盐的物质的量浓度为___________
(1)碳与同周期元素Q的单质化合仅能生成两种常见气态化合物,其中一种化合物R为非极性分子,则Q元素在周期表中的位置为
(2)一定条件下,Na还原CCl4可制备金刚石,反应结束冷却至室温后,回收CCl4的实验操作名称为
(3)碳还原制取金刚砂SiC,其粗产品中杂质为Si和SiO2.先将20.0gSiC粗产品加入到过量NaOH溶液中充分反应,收集到标准状况下2.24 L的氢气,过滤后得SiC固体11.4g,滤液稀释到1L。Si与NaOH溶液反应的离子方程式为
您最近一年使用:0次



