名校
1 . 为验证氧化性Cl2>Fe3+>SO2,某小组用如图所示装置进行实验(夹持仪器和A中加热装置已略,气密性已检验)。
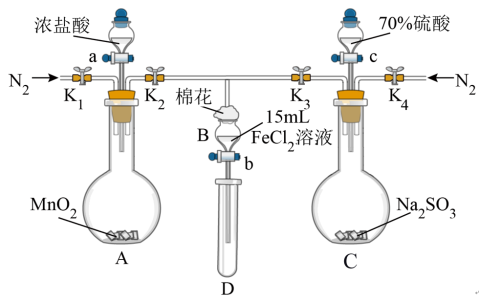
实验过程:
Ⅰ.打开弹簧夹K1~K4,通入一段时间N2,再将T型导管插入B中,继续通入N2,然后关闭K1、K3、K4。
Ⅱ.打开活塞a,滴加一定量的浓盐酸,给A加热。
Ⅲ.当B中溶液变黄时,停止加热,关闭K2。
Ⅳ.打开活塞b,使约2mL的溶液流入D试管中,检验其中的离子。
Ⅴ.打开K3和活塞c,加入70%的硫酸,一段时间后关闭K。
Ⅵ.更新试管D,重复过程Ⅳ,检验B溶液中的离子。
(1)过程Ⅰ的目的是__________________________ 。
(2)实验室在保存FeCl2溶液时为了防止FeCl2溶液变质,经常向其中加入铁粉,其原因是__________________________ 。
(3)若向第III步B中的黄色溶液中通入H2S气体,会观察到有淡黄色沉淀生成,写出该反应的化学方程式__________________________ 。
(4)若将制取的SO2通入硫酸酸化的高锰酸钾溶液可使溶液褪色,其反应的离子方程式为__________________________ 。
(5)甲、乙、丙三位同学分别完成了上述实验,结论如下表所示.他们的检测结果一定能够证明氧化性Cl2>Fe3+>SO2的是_____ (填“甲”、“乙”或“丙”)。
(6)将B中的FeCl2溶液换成100mLFeBr2溶液并向其中通入2.24LCl2(标准状况下),若溶液中有1/2的Br﹣被氧化成单质Br2,则原FeBr2溶液中FeBr2的物质的量浓度为____ 。

实验过程:
Ⅰ.打开弹簧夹K1~K4,通入一段时间N2,再将T型导管插入B中,继续通入N2,然后关闭K1、K3、K4。
Ⅱ.打开活塞a,滴加一定量的浓盐酸,给A加热。
Ⅲ.当B中溶液变黄时,停止加热,关闭K2。
Ⅳ.打开活塞b,使约2mL的溶液流入D试管中,检验其中的离子。
Ⅴ.打开K3和活塞c,加入70%的硫酸,一段时间后关闭K。
Ⅵ.更新试管D,重复过程Ⅳ,检验B溶液中的离子。
(1)过程Ⅰ的目的是
(2)实验室在保存FeCl2溶液时为了防止FeCl2溶液变质,经常向其中加入铁粉,其原因是
(3)若向第III步B中的黄色溶液中通入H2S气体,会观察到有淡黄色沉淀生成,写出该反应的化学方程式
(4)若将制取的SO2通入硫酸酸化的高锰酸钾溶液可使溶液褪色,其反应的离子方程式为
(5)甲、乙、丙三位同学分别完成了上述实验,结论如下表所示.他们的检测结果一定能够证明氧化性Cl2>Fe3+>SO2的是
| 过程Ⅳ,B溶液中含有的离子 | 过程Ⅵ,B溶液中含有的离子 | |
| 甲 | 有Fe3+无Fe2+ | 有Fe2+ |
| 乙 | 既有Fe3+又有Fe2+ | 有SO42﹣ |
| 丙 | 有Fe3+无Fe2+ | 有SO42﹣ |
您最近一年使用:0次
2019-02-12更新
|
571次组卷
|
2卷引用:【全国百强校】陕西省西安市长安区第一中学2018-2019学年高一上学期期末考试化学试题
名校
解题方法
2 . 将KCl、 、
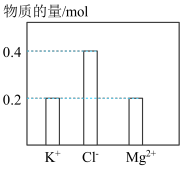
、 溶于水配成混合溶液,溶液体积为1L,部分离子物质的量如图所示,下列说法错误的是
溶于水配成混合溶液,溶液体积为1L,部分离子物质的量如图所示,下列说法错误的是
 、
、 溶于水配成混合溶液,溶液体积为1L,部分离子物质的量如图所示,下列说法错误的是
溶于水配成混合溶液,溶液体积为1L,部分离子物质的量如图所示,下列说法错误的是
A.该混合溶液中 的物质的量为0.1mol 的物质的量为0.1mol |
B.若将该混合溶液加水稀释至体积为5L,稀释后溶液中 的物质的量浓度为 的物质的量浓度为 |
C.若向该混合溶液中逐滴加入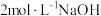 溶液至 溶液至 恰好完全沉淀,需NaOH溶液50mL 恰好完全沉淀,需NaOH溶液50mL |
D.该混合溶液中由 电离出的 电离出的 浓度为 浓度为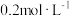 |
您最近一年使用:0次
2023-12-01更新
|
469次组卷
|
8卷引用:陕西省西安市航天中学2023~2024学年高一上学期第三次月考化学试题
名校
解题方法
3 . 下列关于2L0.5mol•L-1Na2SO4溶液的说法中正确的是
| A.Na+的物质的量为1mol |
| B.Na2SO4的摩尔质量为142g |
C.取1L溶液,溶液中SO 的物质的量为0.5mol 的物质的量为0.5mol |
| D.溶液中含氧原子数目约为4×6.02×1023 |
您最近一年使用:0次
2023-10-25更新
|
20次组卷
|
2卷引用:陕西省榆林市十校联考2023-2024学年高一上学期12月月考化学试题
4 . 下列说法中,正确的是
A. 中含有的分子数约为6.02×1023 中含有的分子数约为6.02×1023 |
B. 的体积一定是22.4L 的体积一定是22.4L |
| C.Al的摩尔质量是27g |
D.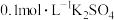 溶液中含有 溶液中含有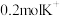 |
您最近一年使用:0次
解题方法
5 . 下列有关物质的量浓度的相关说法中错误 的是
| A.将25gCuSO4∙5H2O晶体溶于水配成100mL溶液,该溶液的物质的量浓度为1mol∙L-1 |
| B.将10mL0.1mol∙L-1NaCl溶液和90mL水混合(忽略混合后溶液体积变化),所得溶液物质的量浓度为0.01mol∙L-1 |
| C.实验室要用容量瓶配制0.2mol∙L-1的NaCl溶液950mL,应称取NaCl固体11.7g |
| D.将100mL5mol∙L-1盐酸在蒸发皿中蒸发至50mL溶液,物质的量浓度变为10mol∙L-1 |
您最近一年使用:0次
名校
6 . 设 为阿伏加德罗常数的值,下列说法错误的是
为阿伏加德罗常数的值,下列说法错误的是
 为阿伏加德罗常数的值,下列说法错误的是
为阿伏加德罗常数的值,下列说法错误的是A.1mol NaOH中含有的阴、阳离子总数是 |
B.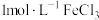 溶液中所含 溶液中所含 的数目为 的数目为 |
C.标准状况下,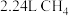 中含有氢原子的数目为 中含有氢原子的数目为 |
D.常温常压下,9.6g由 和 和 组成的混合气体中所含氧原子总数为 组成的混合气体中所含氧原子总数为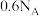 |
您最近一年使用:0次
7 . 下列说法中正确的是
A.将 加入水中配成1L溶液,则所得溶液中溶质的物质的量浓度是 加入水中配成1L溶液,则所得溶液中溶质的物质的量浓度是 |
| B.用小刀切下一小块金属钠,将剩余的钠再放回原试剂瓶 |
C.标准状况下,将 气体溶于1L水中,所得溶液中溶质的物质的量浓度是 气体溶于1L水中,所得溶液中溶质的物质的量浓度是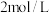 |
D.向某溶液中加入 溶液产生白色沉淀,再加稀盐酸沉淀不溶解,说明原溶液中一定含有 溶液产生白色沉淀,再加稀盐酸沉淀不溶解,说明原溶液中一定含有 |
您最近一年使用:0次
解题方法
8 . 下列关于溶液物质的量浓度的说法正确的是
| A.常温下,1 L水中溶解58.5 g NaCl,该溶液的物质的量浓度为1 mol/L |
| B.1 mol Na2O加入适量水配成1 L溶液,该溶液的物质的量浓度为1 mol/L |
| C.200 mL0.1 mol/LNaCl溶液和100 mL0.1 mol/LMgCl2溶液,Cl-的物质的量浓度相同 |
D.10 g 98%的硫酸(密度为 )与20 mL18.4 mol/L的硫酸的浓度相同 )与20 mL18.4 mol/L的硫酸的浓度相同 |
您最近一年使用:0次
2022-01-12更新
|
611次组卷
|
4卷引用: 陕西省咸阳市高新一中2023-2024学年高一上学期第二次质量检测化学试题
陕西省咸阳市高新一中2023-2024学年高一上学期第二次质量检测化学试题广西三新学术联盟2021-2022学年高一上学期期末联考化学试题重庆市缙云教育联盟2021-2022学年高三上学期第一次诊断性检测化学试题(已下线)微专题04 以物质的量为中心的计算-备战2023年高考化学一轮复习考点微专题
名校
9 . 将50 g溶质质量分数为w1,物质的量浓度为c1的浓硫酸加入到V mL水中,稀释后得到溶质质量分数为w2,物质的量浓度为c2的稀溶液。若c1=2c2,下面说法正确的是
| A.V >50 w1>2w2 | B.V <50 w1<2w2 |
| C.V <50 w1>2w2 | D.V >50 w1<2w2 |
您最近一年使用:0次
2021-12-03更新
|
189次组卷
|
2卷引用:陕西省长安区第一中学2021-2022学年高一上学期期中考试化学试题
10 . 城市立体农场无土栽培可将农业环节融入高层建筑,实现城市粮食与果蔬的自给自足。下表是某叶菜类常量元素的无土栽培营养液配方:
某兴趣小组配制和取用450mL上述浓缩500倍营养液。下列说法不正确的是
| 化合物 | 用量/(mg/L) | 浓缩250倍用量(g/L) | 浓缩500倍用量(g/L) |
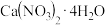 | 472 | 118 | 236 |
 | 202 | 50.5 | 101 |
 | 80 | 20 | 40 |
| A.配制该溶液所需容量瓶的规格为500mL |
| B.配制过程中所需三种物质的质量分别为118g、50.5g、20g |
| C.定容时,若俯视容量瓶刻度线,则所配溶液的浓度会偏大 |
D.配制好的溶液中, 的物质的量浓度为1 的物质的量浓度为1 |
您最近一年使用:0次
2021-11-04更新
|
99次组卷
|
2卷引用:陕西省蒲城县2021-2022学年高三上学期第一次对抗赛(期中考试)化学试题



