名校
1 . 1.76g铜镁合金完全溶解于50mL密度为1.40g/mL、质量分数为63%的浓硝酸中,得到NO2气体1792mL(标准状况),向反应后的溶液中加入适量的1.0 mol/LNaOH溶液,恰好使溶液中的金属离子全部沉淀。下列说法不正确的是
| A.该浓硝酸中HNO3的物质的量浓度是14.0 mol/L |
| B.浓硝酸在反应中表现了氧化性和酸性,且表现氧化性的硝酸的物质的量为0.08 mol |
| C.得到沉淀的质量为3.12g |
| D.加入NaOH溶液的体积是50 mL |
您最近一年使用:0次
2019-02-13更新
|
485次组卷
|
24卷引用:陕西安康市紫阳县紫阳中学2019届高三上学期入学调研考试化学试题
陕西安康市紫阳县紫阳中学2019届高三上学期入学调研考试化学试题(已下线)2014届甘肃河西五市部分普通高中高三第一次联合考试化学试卷(已下线)2013-2014北京101中学高三第三次月考理综化学试卷(已下线)2014湖南长沙市长郡中学高三上学期第四次月考化学试卷2015届宁夏银川九中高三上学期期中化学试卷(已下线)2014届北京101中学高三年级第三次月考理综化学试卷2016届河北省衡水中学高三上学期二调化学试卷2016届甘肃省张掖、嘉峪关、山丹部分高中高三上学期期中联考化学试卷2016届甘肃省河西五市部分普通高中高三上第一次联考化学试卷2016届江西万载高三第二次能力模拟冲刺理科综合化学试卷河北省邯郸市(大名县、永年区、磁县、邯山区)四县2016-2017学年高二下学期期中联考化学试题江西省南昌市第三中学2016-2017学年高一下学期5月月考化学试题河南省林州市第一中学2018届高三7月调研考试化学试题江西省上高县第二中学2018届高三第一次月考化学试题河北省衡水中学2018届高三上学期二调考试化学试题云南省临沧市第一中学2018届高三上学期第七次月考化学试题江西省樟树中学2017-2018学年高一下学期第三次月考化学试题【校级联考】安徽省江南片2019届高三上学期入学摸底考试化学试题福建省泉州第五中学2019届高三入学调研考试化学试题甘肃省武威第一中学2019届高三上学期期末考试化学试题(已下线)专题1.2 物质的量浓度(练)-《2020年高考一轮复习讲练测》安徽省肥东县高级中学2021届高三上学期第二次月考化学试题安徽省滁州市定远县重点中学2021届高三上学期11月质量检测化学试题宁夏银川一中2021-2022学年高一上学期期末考试化学试题
2 . 向100mL稀硫酸和硝酸铁的混合溶液中加入铁粉,溶液中的Fe2+浓度如图所示(不考虑溶液体积的变化):
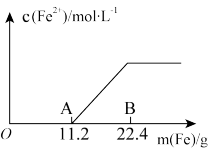
(1)OA段反应的离子方程式为___ ;AB段反应的离子方程式为__ ;由此推出混合液中存在微粒氧化性由大到小的关系是___ 。
(2)原溶液中H2SO4与Fe(NO3)3的物质的量之比为___
(3)B点对应溶液中Fe2+物质的量浓度为__ mol∙L-1; 的物质的量浓度为
的物质的量浓度为__ mol·L-1。

(1)OA段反应的离子方程式为
(2)原溶液中H2SO4与Fe(NO3)3的物质的量之比为
(3)B点对应溶液中Fe2+物质的量浓度为
 的物质的量浓度为
的物质的量浓度为
您最近一年使用:0次
名校
3 . 为验证氧化性Cl2>Fe3+>SO2,某小组用如图所示装置进行实验(夹持仪器和A中加热装置已略,气密性已检验)。
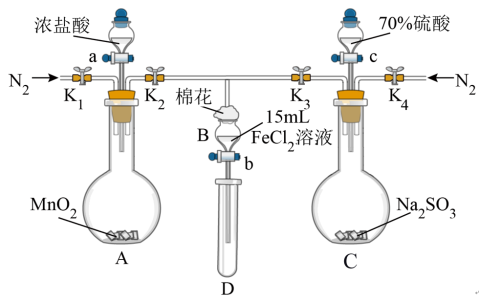
实验过程:
Ⅰ.打开弹簧夹K1~K4,通入一段时间N2,再将T型导管插入B中,继续通入N2,然后关闭K1、K3、K4。
Ⅱ.打开活塞a,滴加一定量的浓盐酸,给A加热。
Ⅲ.当B中溶液变黄时,停止加热,关闭K2。
Ⅳ.打开活塞b,使约2mL的溶液流入D试管中,检验其中的离子。
Ⅴ.打开K3和活塞c,加入70%的硫酸,一段时间后关闭K。
Ⅵ.更新试管D,重复过程Ⅳ,检验B溶液中的离子。
(1)过程Ⅰ的目的是__________________________ 。
(2)实验室在保存FeCl2溶液时为了防止FeCl2溶液变质,经常向其中加入铁粉,其原因是__________________________ 。
(3)若向第III步B中的黄色溶液中通入H2S气体,会观察到有淡黄色沉淀生成,写出该反应的化学方程式__________________________ 。
(4)若将制取的SO2通入硫酸酸化的高锰酸钾溶液可使溶液褪色,其反应的离子方程式为__________________________ 。
(5)甲、乙、丙三位同学分别完成了上述实验,结论如下表所示.他们的检测结果一定能够证明氧化性Cl2>Fe3+>SO2的是_____ (填“甲”、“乙”或“丙”)。
(6)将B中的FeCl2溶液换成100mLFeBr2溶液并向其中通入2.24LCl2(标准状况下),若溶液中有1/2的Br﹣被氧化成单质Br2,则原FeBr2溶液中FeBr2的物质的量浓度为____ 。

实验过程:
Ⅰ.打开弹簧夹K1~K4,通入一段时间N2,再将T型导管插入B中,继续通入N2,然后关闭K1、K3、K4。
Ⅱ.打开活塞a,滴加一定量的浓盐酸,给A加热。
Ⅲ.当B中溶液变黄时,停止加热,关闭K2。
Ⅳ.打开活塞b,使约2mL的溶液流入D试管中,检验其中的离子。
Ⅴ.打开K3和活塞c,加入70%的硫酸,一段时间后关闭K。
Ⅵ.更新试管D,重复过程Ⅳ,检验B溶液中的离子。
(1)过程Ⅰ的目的是
(2)实验室在保存FeCl2溶液时为了防止FeCl2溶液变质,经常向其中加入铁粉,其原因是
(3)若向第III步B中的黄色溶液中通入H2S气体,会观察到有淡黄色沉淀生成,写出该反应的化学方程式
(4)若将制取的SO2通入硫酸酸化的高锰酸钾溶液可使溶液褪色,其反应的离子方程式为
(5)甲、乙、丙三位同学分别完成了上述实验,结论如下表所示.他们的检测结果一定能够证明氧化性Cl2>Fe3+>SO2的是
| 过程Ⅳ,B溶液中含有的离子 | 过程Ⅵ,B溶液中含有的离子 | |
| 甲 | 有Fe3+无Fe2+ | 有Fe2+ |
| 乙 | 既有Fe3+又有Fe2+ | 有SO42﹣ |
| 丙 | 有Fe3+无Fe2+ | 有SO42﹣ |
您最近一年使用:0次
2019-02-12更新
|
571次组卷
|
2卷引用:【全国百强校】陕西省西安市长安区第一中学2018-2019学年高一上学期期末考试化学试题
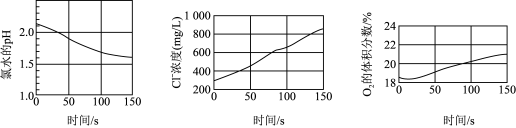
4 . 某兴趣小组利用数字化实验测定光照过程中氯水的 、氯水中氯离子的浓度、广口瓶中氧气的体积分数三者的变化,实验结果如图所示。下列说法正确的是
、氯水中氯离子的浓度、广口瓶中氧气的体积分数三者的变化,实验结果如图所示。下列说法正确的是
 、氯水中氯离子的浓度、广口瓶中氧气的体积分数三者的变化,实验结果如图所示。下列说法正确的是
、氯水中氯离子的浓度、广口瓶中氧气的体积分数三者的变化,实验结果如图所示。下列说法正确的是
A.氯水中存在自由移动的离子,能导电,但 属于非电解质 属于非电解质 |
B.氯水的 值随光照时间增加而减少,是因为次氯酸见光分解为酸性更强的酸 值随光照时间增加而减少,是因为次氯酸见光分解为酸性更强的酸 |
C.光照过程中 体积分数逐渐增加,说明发生了氧化还原反应,其中 体积分数逐渐增加,说明发生了氧化还原反应,其中 为还原产物 为还原产物 |
D.由图可知,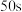 时 时 浓度约为 浓度约为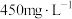 ,计算可知氯水中 ,计算可知氯水中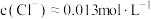 |
您最近一年使用:0次



