碳及其化合物在生产、生活中有广泛的用途。
(1)碳与同周期元素Q的单质化合仅能生成两种常见气态化合物,其中一种化合物R为非极性分子,则Q元素在周期表中的位置为___________ ,R的电子式为___________
(2)一定条件下,Na还原CCl4可制备金刚石,反应结束冷却至室温后,回收CCl4的实验操作名称为___________ ,除去粗产品中少量钠的试剂为___________
(3)碳还原制取金刚砂SiC,其粗产品中杂质为Si和SiO2.先将20.0gSiC粗产品加入到过量NaOH溶液中充分反应,收集到标准状况下2.24 L的氢气,过滤后得SiC固体11.4g,滤液稀释到1L。Si与NaOH溶液反应的离子方程式为___________ ,硅酸盐的物质的量浓度为___________
(1)碳与同周期元素Q的单质化合仅能生成两种常见气态化合物,其中一种化合物R为非极性分子,则Q元素在周期表中的位置为
(2)一定条件下,Na还原CCl4可制备金刚石,反应结束冷却至室温后,回收CCl4的实验操作名称为
(3)碳还原制取金刚砂SiC,其粗产品中杂质为Si和SiO2.先将20.0gSiC粗产品加入到过量NaOH溶液中充分反应,收集到标准状况下2.24 L的氢气,过滤后得SiC固体11.4g,滤液稀释到1L。Si与NaOH溶液反应的离子方程式为
更新时间:2020-12-15 18:49:34
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】某液体化合物X2Y4,常用做火箭燃料。16 g X2Y4在一定量的O2中恰好完全燃烧,反应方程式为X2Y4(l)+O2(g)=X2(g)+2Y2O(l)。冷却后标准状况下测得生成物的体积为11.2 L,其密度为1.25 g·L-1,则:
(1)反应前O2的体积V(O2)为___________ 。
(2)X2的摩尔质量为___________ 。
(3)Y元素的名称是___________ 。
(1)反应前O2的体积V(O2)为
(2)X2的摩尔质量为
(3)Y元素的名称是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】“7•20”特大洪灾过后,饮用水的消毒杀菌成为抑制大规模传染性疾病爆发的有效措施之一。“84”消毒液、漂白粉和ClO2等都是有效的消杀试剂。
(1)用化学方程式表示氯气与烧碱溶液制备“84”消毒液的原理____ ,标况下56L氯气完全被吸收,需要____ L1mol/L的NaOH溶液。
(2)使用漂白粉漂白,只需取适量漂白粉溶于水即可,漂白原理用化学方程式表示为_____ 。
(3)漂白粉的保存要注意密封,为了判断一份儿久置的漂白粉是①没有失效②部分失效③完全失效。某化学兴趣小组设计实验进行验证。
已知:Ca(ClO)2溶液呈碱性;Ca(ClO)2+4HCl(浓)=CaCl2+2Cl2↑+2H2O;Ca(ClO)2+2HCl(稀)=CaCl2+2HClO
a.甲同学取适量漂白粉样品,滴加浓盐酸,将产生的气体直接通入澄清石灰水中,没有发现石灰水变浑浊。由此,判断结论为①,你是否同意他的结论____ (填“同意”或“不同意”),若不同意,你认为的结论是____ (若同意,此空不用填)
A.② B.③ C.①或② D.①②③均有可能
b.乙同学改用滴加稀盐酸,发现产生大量气泡,将气体通入澄清石灰水中,石灰水变浑浊;他又取少量漂白粉样品配成溶液,滴在pH试纸上,最终试纸变白。据此你得出的结论是_____ (从①②③中选填)。
(4)目前普遍使用ClO2代替Cl2及次氯酸盐作为广谱抗菌消毒剂,因为它安全、低毒,高效。其摩尔质量为_____ 。ClO2还可以将剧毒的NaCN转化为无毒物质除去,产物是氯化钠和两种常见气体。试写出该反应的化学方程式_____ 。
(1)用化学方程式表示氯气与烧碱溶液制备“84”消毒液的原理
(2)使用漂白粉漂白,只需取适量漂白粉溶于水即可,漂白原理用化学方程式表示为
(3)漂白粉的保存要注意密封,为了判断一份儿久置的漂白粉是①没有失效②部分失效③完全失效。某化学兴趣小组设计实验进行验证。
已知:Ca(ClO)2溶液呈碱性;Ca(ClO)2+4HCl(浓)=CaCl2+2Cl2↑+2H2O;Ca(ClO)2+2HCl(稀)=CaCl2+2HClO
a.甲同学取适量漂白粉样品,滴加浓盐酸,将产生的气体直接通入澄清石灰水中,没有发现石灰水变浑浊。由此,判断结论为①,你是否同意他的结论
A.② B.③ C.①或② D.①②③均有可能
b.乙同学改用滴加稀盐酸,发现产生大量气泡,将气体通入澄清石灰水中,石灰水变浑浊;他又取少量漂白粉样品配成溶液,滴在pH试纸上,最终试纸变白。据此你得出的结论是
(4)目前普遍使用ClO2代替Cl2及次氯酸盐作为广谱抗菌消毒剂,因为它安全、低毒,高效。其摩尔质量为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】单宁酸 -硫酸体系中,低品位软锰矿(
-硫酸体系中,低品位软锰矿( 质量分数为29%)中的Mn(Ⅳ)可被还原为
质量分数为29%)中的Mn(Ⅳ)可被还原为 而浸出。其浸出过程如图所示。
而浸出。其浸出过程如图所示。 完全水解,生成的没食子酸和葡萄糖物质的量之比为
完全水解,生成的没食子酸和葡萄糖物质的量之比为___________ 。
(2)写出葡萄糖还原 生成
生成 的离子反应方程式:
的离子反应方程式:________________ 。
(3)浸出前后软锰矿与浸取渣的X-射线衍射图如图所示,衍射峰的强度能一定程度反映晶体的质量分数等信息。指出图中 对应衍射峰强度变化的原因:
对应衍射峰强度变化的原因:____________ 。
准确称取 软锰矿试样,加入一定量硫酸和单宁酸,水浴加热并充分搅拌,一段时间后过滤.将滤液冷却后加水定容至2L,量取20.00mL溶液于锥形瓶中,向锥形瓶中加入足量磷酸作稳定剂,再加入2mL高氯酸,边加边摇动,使
软锰矿试样,加入一定量硫酸和单宁酸,水浴加热并充分搅拌,一段时间后过滤.将滤液冷却后加水定容至2L,量取20.00mL溶液于锥形瓶中,向锥形瓶中加入足量磷酸作稳定剂,再加入2mL高氯酸,边加边摇动,使 完全氧化为Mn(Ⅲ),加热溶液至无气体产生。冷却后用浓度为
完全氧化为Mn(Ⅲ),加热溶液至无气体产生。冷却后用浓度为 的
的 溶液滴定至终点,消耗
溶液滴定至终点,消耗 溶液的体积为
溶液的体积为 。
。
①实验室现配 溶液的浓度与计算值存在误差,为提高测量结果的精确度,滴定前需要对现配
溶液的浓度与计算值存在误差,为提高测量结果的精确度,滴定前需要对现配 溶液进行的补充实验是
溶液进行的补充实验是_________ 。
② 完全氧化后加热溶液的目的是
完全氧化后加热溶液的目的是____________ 。
③计算该条件下软锰矿中锰元素的浸出率
____________ 。[ 。写出计算过程]
。写出计算过程]
(5)90℃下,控制单宁酸用量和反应时间相同,测得 对锰元素浸出率的影响如图所示。
对锰元素浸出率的影响如图所示。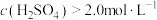 时,锰元素浸出率降低的可能原因是
时,锰元素浸出率降低的可能原因是___________ 。
 -硫酸体系中,低品位软锰矿(
-硫酸体系中,低品位软锰矿( 质量分数为29%)中的Mn(Ⅳ)可被还原为
质量分数为29%)中的Mn(Ⅳ)可被还原为 而浸出。其浸出过程如图所示。
而浸出。其浸出过程如图所示。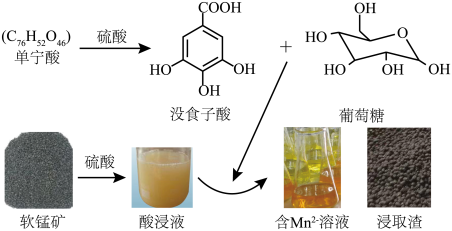
 完全水解,生成的没食子酸和葡萄糖物质的量之比为
完全水解,生成的没食子酸和葡萄糖物质的量之比为(2)写出葡萄糖还原
 生成
生成 的离子反应方程式:
的离子反应方程式:(3)浸出前后软锰矿与浸取渣的X-射线衍射图如图所示,衍射峰的强度能一定程度反映晶体的质量分数等信息。指出图中
 对应衍射峰强度变化的原因:
对应衍射峰强度变化的原因: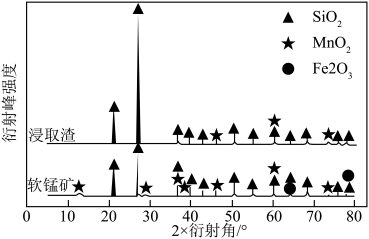
准确称取
 软锰矿试样,加入一定量硫酸和单宁酸,水浴加热并充分搅拌,一段时间后过滤.将滤液冷却后加水定容至2L,量取20.00mL溶液于锥形瓶中,向锥形瓶中加入足量磷酸作稳定剂,再加入2mL高氯酸,边加边摇动,使
软锰矿试样,加入一定量硫酸和单宁酸,水浴加热并充分搅拌,一段时间后过滤.将滤液冷却后加水定容至2L,量取20.00mL溶液于锥形瓶中,向锥形瓶中加入足量磷酸作稳定剂,再加入2mL高氯酸,边加边摇动,使 完全氧化为Mn(Ⅲ),加热溶液至无气体产生。冷却后用浓度为
完全氧化为Mn(Ⅲ),加热溶液至无气体产生。冷却后用浓度为 的
的 溶液滴定至终点,消耗
溶液滴定至终点,消耗 溶液的体积为
溶液的体积为 。
。①实验室现配
 溶液的浓度与计算值存在误差,为提高测量结果的精确度,滴定前需要对现配
溶液的浓度与计算值存在误差,为提高测量结果的精确度,滴定前需要对现配 溶液进行的补充实验是
溶液进行的补充实验是②
 完全氧化后加热溶液的目的是
完全氧化后加热溶液的目的是③计算该条件下软锰矿中锰元素的浸出率

 。写出计算过程]
。写出计算过程](5)90℃下,控制单宁酸用量和反应时间相同,测得
 对锰元素浸出率的影响如图所示。
对锰元素浸出率的影响如图所示。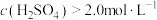 时,锰元素浸出率降低的可能原因是
时,锰元素浸出率降低的可能原因是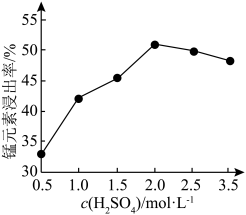
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】回答下列问题:
Ⅰ:在标准状况下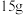
 与
与 的混合气体,体积为
的混合气体,体积为 。则:
。则:
(1)混合气体的平均摩尔质量是___________ 。
(2) 和
和 的体积之比是
的体积之比是___________ 。
(3) 和
和 的质量之比是
的质量之比是___________ 。
Ⅱ:将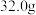
 固体溶于水配成
固体溶于水配成 溶液,其密度为
溶液,其密度为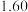
 ,试计算:
,试计算:
(4)该溶液中 的物质的量浓度为
的物质的量浓度为___________ 。
(5)该溶液中 的质量分数为
的质量分数为___________ 。
(6)从该溶液中取出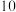
 ,含
,含 的质量为
的质量为___________ 。
(7)将取出的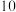
 溶液加水稀释到
溶液加水稀释到
 ,稀释后溶液中
,稀释后溶液中 的物质的量浓度为
的物质的量浓度为___________ 。
Ⅰ:在标准状况下
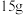
 与
与 的混合气体,体积为
的混合气体,体积为 。则:
。则:(1)混合气体的平均摩尔质量是
(2)
 和
和 的体积之比是
的体积之比是(3)
 和
和 的质量之比是
的质量之比是Ⅱ:将
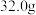
 固体溶于水配成
固体溶于水配成 溶液,其密度为
溶液,其密度为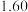
 ,试计算:
,试计算:(4)该溶液中
 的物质的量浓度为
的物质的量浓度为(5)该溶液中
 的质量分数为
的质量分数为(6)从该溶液中取出
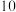
 ,含
,含 的质量为
的质量为(7)将取出的
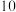
 溶液加水稀释到
溶液加水稀释到
 ,稀释后溶液中
,稀释后溶液中 的物质的量浓度为
的物质的量浓度为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】物质的量是高中化学常用的物理量,请完成以下有关计算:
(1)0. 6 g H2中含有氢原子的物质的量为_________ mol。
(2)标准状况下,含有相同氧原子数的CO和CO2 的体积之比为____________ 。
(3)100mL硫酸钠溶液中n(Na+)=0.2mol,则其中c(SO42-)=_____________ 。
(4)6.72 L(标准状况)CO 与一定量的Fe2O3恰好完全反应,生成Fe的质量为____________ g。
(1)0. 6 g H2中含有氢原子的物质的量为
(2)标准状况下,含有相同氧原子数的CO和CO2 的体积之比为
(3)100mL硫酸钠溶液中n(Na+)=0.2mol,则其中c(SO42-)=
(4)6.72 L(标准状况)CO 与一定量的Fe2O3恰好完全反应,生成Fe的质量为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】以黄铁矿(主要成分 )为原料生产硫酸,并将产出的炉渣和尾气进行资源综合利用,减轻对环境的污染,其中一种流程如图所示。
)为原料生产硫酸,并将产出的炉渣和尾气进行资源综合利用,减轻对环境的污染,其中一种流程如图所示。
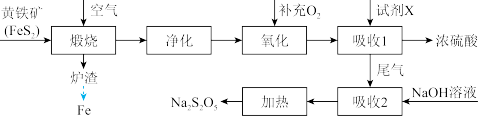
(1) 中铁元素的化合价为
中铁元素的化合价为___________ 。
(2)黄铁矿( )在空气中煅烧的化学方程式为
)在空气中煅烧的化学方程式为___________ 。
(3)工业上,吸收 时宜选用的试剂X为98.3%的浓硫酸,目的是
时宜选用的试剂X为98.3%的浓硫酸,目的是___________ 。
(4)因为 (焦亚硫酸钠)具有还原性,导致商品
(焦亚硫酸钠)具有还原性,导致商品 方中不可避免地存在
方中不可避免地存在 。检验其中含有
。检验其中含有 的方法是
的方法是___________ 。
(5)某化学实验小组取1.0g黄铁矿样品在空气中充分灼烧(假设杂质不参加反应),生成的 气体恰好被
气体恰好被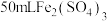 ,溶液完全吸收,在所得溶液中加入足量
,溶液完全吸收,在所得溶液中加入足量 溶液充分反应后,过滤、洗涤、干燥得9.32g固体。
溶液充分反应后,过滤、洗涤、干燥得9.32g固体。
①原 溶液的物质的量浓度为
溶液的物质的量浓度为___________ ,黄铁矿中 的质量分数为
的质量分数为___________ 。
②工业上煅烧10t上述黄铁矿,产生的 经催化氧化制硫酸,理论上可制得98%的浓硫酸
经催化氧化制硫酸,理论上可制得98%的浓硫酸___________ t。
 )为原料生产硫酸,并将产出的炉渣和尾气进行资源综合利用,减轻对环境的污染,其中一种流程如图所示。
)为原料生产硫酸,并将产出的炉渣和尾气进行资源综合利用,减轻对环境的污染,其中一种流程如图所示。
(1)
 中铁元素的化合价为
中铁元素的化合价为(2)黄铁矿(
 )在空气中煅烧的化学方程式为
)在空气中煅烧的化学方程式为(3)工业上,吸收
 时宜选用的试剂X为98.3%的浓硫酸,目的是
时宜选用的试剂X为98.3%的浓硫酸,目的是(4)因为
 (焦亚硫酸钠)具有还原性,导致商品
(焦亚硫酸钠)具有还原性,导致商品 方中不可避免地存在
方中不可避免地存在 。检验其中含有
。检验其中含有 的方法是
的方法是(5)某化学实验小组取1.0g黄铁矿样品在空气中充分灼烧(假设杂质不参加反应),生成的
 气体恰好被
气体恰好被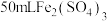 ,溶液完全吸收,在所得溶液中加入足量
,溶液完全吸收,在所得溶液中加入足量 溶液充分反应后,过滤、洗涤、干燥得9.32g固体。
溶液充分反应后,过滤、洗涤、干燥得9.32g固体。①原
 溶液的物质的量浓度为
溶液的物质的量浓度为 的质量分数为
的质量分数为②工业上煅烧10t上述黄铁矿,产生的
 经催化氧化制硫酸,理论上可制得98%的浓硫酸
经催化氧化制硫酸,理论上可制得98%的浓硫酸
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】下图是元素周期表的一部分,表中所列字母a、b、c、d、e、f、g、h分别代表某种化学元素。请依据这8种元素回答下列问题。
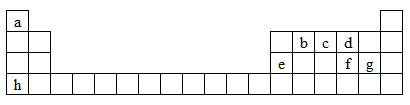
(1)上述8种元素的单质中常温下为气态,且密度最小的是______ (填化学式)。
(2)f元素的原子结构示意图为_______ 。
(3)c的最高价氧化物对应水化物的化学式为______ 。
(4)hg的电子式为_______ 。
(5)b、c、d三种元素的最简单氢化物的沸点由高到低的顺序是______ (填化学式)。
(6)元素e的单质与h的最高价氧化物对应的水化物反应的化学方程式为__________ 。
(7)f元素的最简单氢化物的水溶液显____ 性(填“酸”或“碱”),请写出该氢化物久置在空气中变质的化学方程式________ 。
(8)gd-常用作消毒剂,单质砷(As)在碱性溶液中可被gd-氧化为AsO43-,该反应的离子方程式为__________ 。

(1)上述8种元素的单质中常温下为气态,且密度最小的是
(2)f元素的原子结构示意图为
(3)c的最高价氧化物对应水化物的化学式为
(4)hg的电子式为
(5)b、c、d三种元素的最简单氢化物的沸点由高到低的顺序是
(6)元素e的单质与h的最高价氧化物对应的水化物反应的化学方程式为
(7)f元素的最简单氢化物的水溶液显
(8)gd-常用作消毒剂,单质砷(As)在碱性溶液中可被gd-氧化为AsO43-,该反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】如图是某粒子的结构示意图,试回答:
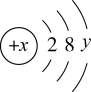
(1)当x-y=10时,该粒子为________ (填“原子”、“阳离子”或“阴离子”)。
(2)当y=8时,该粒子可能是(写微粒符号):______ 、______ 、_____ 、_____ 、_____ ;按离子半径从大到小顺序排列上述离子:____________ 。
(3)写出y=3的元素最高价氧化物对应的水化物与NaOH溶液发生反应的离子方程式______________ 。

(1)当x-y=10时,该粒子为
(2)当y=8时,该粒子可能是(写微粒符号):
(3)写出y=3的元素最高价氧化物对应的水化物与NaOH溶液发生反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】X、Y、Z、W是元素周期表前四周期中的四种常见元素,其相关信息如下表:
(1)Y位于元素周期表第________ 周期第________ 族,Y和Z的最高价氧化物对应的水化物的酸性较强的是________ (写化学式)。
(2)W的基态原子核外电子排布式是___________________________________ 。
(3)W2Y在空气中煅烧生成W2O的化学方程式是________________________ 。
| 元素 | 相关信息 |
| X | X的基态原子核外3个能级上有电子,且每个能级上的电子数相等 |
| Y | 常温常压下,Y单质是淡黄色固体,常在火山口附近沉积 |
| Z | Z和Y同周期,Z的电负性大于Y |
| W | W的一种核素的质量数为63,中子数为34 |
(1)Y位于元素周期表第
(2)W的基态原子核外电子排布式是
(3)W2Y在空气中煅烧生成W2O的化学方程式是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】软锰矿的主要成分是MnO2,其悬浊液可吸收烟气中的SO2,所得酸性浸出液又可用于制备高纯硫酸锰,其一种工艺流程如下图所示。已知金属单质的活动性顺序为Al>Mn>Fe>Ni。回答下列问题:
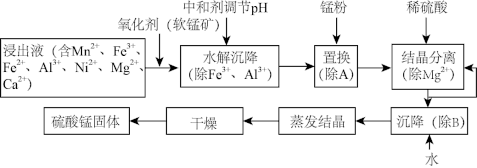
“结晶分离”中的部分物质的溶解度曲线如下图所示。结晶与过滤过程中,体系温度均应维持在___________ (填“27”“60”或“70”)℃。
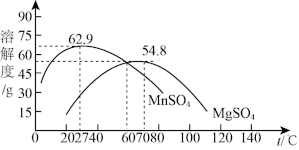

“结晶分离”中的部分物质的溶解度曲线如下图所示。结晶与过滤过程中,体系温度均应维持在

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】现有下列物质:①NaHCO3 ②Na2CO3 ③Al2O3 ④Fe(OH)3 ⑤Al(OH)3 ⑥CO2 ⑦FeCl3 ⑧FeCl2 ⑨MgCl2 ⑩N2 ⑪Na2SO4·10 H2O
(1)其中既能跟稀H2SO4反应,又能跟NaOH溶液反应的是______________ (填序号),
(2)除去固体②中的固体①的方法是_______________ ;
(3)在同温同压下,测得⑩与⑥混合气体对氢气的相对密度为18,⑩的⑥体积之比为__________ ;
(4)欲配制250 mL0. 1 mol/L的Na2SO4溶液需要称量⑪的质量为________ g ;
(5)在①④⑤⑧中可以通过化合反应得到的物质有___________ (填序号);
(6)要除去⑦溶液中的少量⑧,可行的办法是( ) 。
(1)其中既能跟稀H2SO4反应,又能跟NaOH溶液反应的是
(2)除去固体②中的固体①的方法是
(3)在同温同压下,测得⑩与⑥混合气体对氢气的相对密度为18,⑩的⑥体积之比为
(4)欲配制250 mL0. 1 mol/L的Na2SO4溶液需要称量⑪的质量为
(5)在①④⑤⑧中可以通过化合反应得到的物质有
(6)要除去⑦溶液中的少量⑧,可行的办法是
| A.滴入KSCN溶液 | B.加入氯水 | C.加入铜粉 | D.加入铁粉 |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】某化学小组对当地化工厂排出的废水成分进行研究,经检测其中含有大量 、
、 、
、 、
、 、
、 。除去废水样品中的
。除去废水样品中的 和
和 ,回收NaCl、
,回收NaCl、 的实验流程如下。
的实验流程如下。
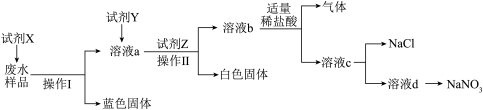
回答下列问题:
(1)经检测,该废水能使蓝色石蕊试纸变红,则废水呈_______ 性(填“酸”、“碱”或“中”)。
(2)试剂X为_______ ;加入试剂Z发生反应的离子方程式为_______ ;向“溶液b”中加入盐酸的作用是_______ 。
(3)下列有关“操作I”的说法正确的是_______(填编号)。
(4)为测定产品NaCl的纯度,称取mg产品溶于水配制成100mL溶液,然后取20mL溶液于试管中,滴加 溶液,当观察到溶液中不再有白色沉淀产生时,恰好消耗VmL
溶液,当观察到溶液中不再有白色沉淀产生时,恰好消耗VmL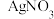 溶液。NaCl样品的纯度为
溶液。NaCl样品的纯度为_______ (用含有m、V的式子表示)。
 、
、 、
、 、
、 、
、 。除去废水样品中的
。除去废水样品中的 和
和 ,回收NaCl、
,回收NaCl、 的实验流程如下。
的实验流程如下。
回答下列问题:
(1)经检测,该废水能使蓝色石蕊试纸变红,则废水呈
(2)试剂X为
(3)下列有关“操作I”的说法正确的是_______(填编号)。
| A.需要的玻璃仪器只有烧杯和漏斗 |
B.用“操作I”装置提纯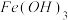 胶体 胶体 |
| C.为加快“操作I”速度,可用玻璃棒搅拌 |
| D.若溶液a仍混浊,需重复进行“操作I” |
 溶液,当观察到溶液中不再有白色沉淀产生时,恰好消耗VmL
溶液,当观察到溶液中不再有白色沉淀产生时,恰好消耗VmL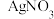 溶液。NaCl样品的纯度为
溶液。NaCl样品的纯度为
您最近一年使用:0次



