解题方法
1 . 下图为实验室某浓盐酸试剂瓶上的标签的有关内容,试根据标签上的有关数据回答下列问题:
(1)该浓盐酸中 的物质的量浓度为
的物质的量浓度为_______  。
。
(2)取用任意体积的该盐酸时,下列物理量中不随所取体积的多少而变化的是_______(填字母)。
(3)某学生欲用上述浓盐酸和蒸馏水配制 物质的量浓度为
物质的量浓度为 的稀盐酸。
的稀盐酸。
①该学生需要量取_______  上述浓盐酸进行配制(注:保留1位小数)。
上述浓盐酸进行配制(注:保留1位小数)。
②在配制过程中,下列实验操作对所配制的稀盐酸的物质的量浓度有何影响?(在横线上填“偏高”、“偏低”或“无影响”)。
I.用量筒量取浓盐酸时俯视观察凹液面_______ 。
II.定容后经振荡、摇匀、静置,发现液面下降,再加适量的蒸馏水_______ 。
III.定容时,俯视读数,所得溶液的浓度_______ 。
| 盐酸 分子式:  相对分子质量:36.5 密度:   的质量分数:36.5% 的质量分数:36.5% |
 的物质的量浓度为
的物质的量浓度为 。
。(2)取用任意体积的该盐酸时,下列物理量中不随所取体积的多少而变化的是_______(填字母)。
A.溶液中 的物质的量 的物质的量 | B.溶液的浓度 |
C.溶液中 的数目 的数目 | D.溶液的密度 |
 物质的量浓度为
物质的量浓度为 的稀盐酸。
的稀盐酸。①该学生需要量取
 上述浓盐酸进行配制(注:保留1位小数)。
上述浓盐酸进行配制(注:保留1位小数)。②在配制过程中,下列实验操作对所配制的稀盐酸的物质的量浓度有何影响?(在横线上填“偏高”、“偏低”或“无影响”)。
I.用量筒量取浓盐酸时俯视观察凹液面
II.定容后经振荡、摇匀、静置,发现液面下降,再加适量的蒸馏水
III.定容时,俯视读数,所得溶液的浓度
您最近一年使用:0次
解题方法
2 . 将5mol·L-1的Mg(NO3)2溶液amL稀释至bmL,稀释后溶液中NO 的物质的量浓度
的物质的量浓度
 的物质的量浓度
的物质的量浓度| A.5a/bmol·L-1 | B.10a/bmol·L-1 | C.b/5amol·L-1 | D.10a/(a+b)mol·L-1 |
您最近一年使用:0次
解题方法
3 . 下列溶液中Cl-物质的量浓度与100mL1mol·L-1MgCl2溶液中Cl-物质的量浓度相等的是
| A.350mL2mol·L-1NaCl溶液 | B.50mL2mol·L-1CaCl2溶液 |
| C.150mL2mol·L-1KClO3溶液 | D.75mL1mol·L-1AlCl3溶液 |
您最近一年使用:0次
4 . 物质的量是高中化学常用的物理量,请完成以下有关计算(设阿伏加德罗常数的值为NA):
(1)在标准状况下,0.5molO2的体积为_______ L。
(2)将0.2moLMgCl2固体溶于水配成400mL溶液,MgCl2溶液的物质的量浓度为_______ 。
(3)0.2molCH4含有_______ NA个氢原子。
(4)49g 的物质的量是
的物质的量是_______ mol。
(5)标准状况下,2gH2的体积是_______ L。
(6)等物质的量的 和
和 的质量之比为
的质量之比为_______ 。
(7)标准状况下6.72L某气体质量13.2g,该物质的摩尔质量为_______ 。
(1)在标准状况下,0.5molO2的体积为
(2)将0.2moLMgCl2固体溶于水配成400mL溶液,MgCl2溶液的物质的量浓度为
(3)0.2molCH4含有
(4)49g
 的物质的量是
的物质的量是(5)标准状况下,2gH2的体积是
(6)等物质的量的
 和
和 的质量之比为
的质量之比为(7)标准状况下6.72L某气体质量13.2g,该物质的摩尔质量为
您最近一年使用:0次
名校
5 . 下列关于物质的量浓度表述正确的是
A.将7.8g  溶于水,配成100g溶液,所得溶液质量分数为7.8% 溶于水,配成100g溶液,所得溶液质量分数为7.8% |
B.质量分数为3.65%的200g盐酸溶液中,含 分子的数目为 分子的数目为 |
C.将25g胆矾( )溶于75克水中,可得到质量分数为16% )溶于75克水中,可得到质量分数为16% 的溶液 的溶液 |
D.将7.1g  通入水中,完全溶于水得到100g溶液,理论上可获得3.65%的盐酸溶液 通入水中,完全溶于水得到100g溶液,理论上可获得3.65%的盐酸溶液 |
您最近一年使用:0次
名校
解题方法
6 . 计算题
(1)一定量的质量分数为10%的氢氧化钠溶液,若将其蒸发掉100g水,其质量分数恰好变为20%,溶液体积变为80mL,则浓缩后的氢氧化钠溶液物质的量浓度为___________ mol/L。
(2)如果ag某气体中含有的分子数为b,则cg该气体在标准状况下的体积是___________ L。(用含字母的式子表示,NA表示阿伏伽德罗常数)
(3)有8gNa2O、Na2O2、Na2CO3、NaOH的混合物与200g质量分数为3.65%的盐酸恰好反应,最终得NaCl固体质量为___________ g。
(4)在VL硫酸铁溶液中,含有agFe3+,取出 L溶液,则取出的
L溶液,则取出的 L溶液中,SO
L溶液中,SO 的物质的量浓度为
的物质的量浓度为___________ mol/L。
(1)一定量的质量分数为10%的氢氧化钠溶液,若将其蒸发掉100g水,其质量分数恰好变为20%,溶液体积变为80mL,则浓缩后的氢氧化钠溶液物质的量浓度为
(2)如果ag某气体中含有的分子数为b,则cg该气体在标准状况下的体积是
(3)有8gNa2O、Na2O2、Na2CO3、NaOH的混合物与200g质量分数为3.65%的盐酸恰好反应,最终得NaCl固体质量为
(4)在VL硫酸铁溶液中,含有agFe3+,取出
 L溶液,则取出的
L溶液,则取出的 L溶液中,SO
L溶液中,SO 的物质的量浓度为
的物质的量浓度为
您最近一年使用:0次
名校
解题方法
7 . 某市售盐酸的质量分数为36.5%,密度为1.2g·cm-3,该盐酸中溶质的物质的量浓度是
| A.0.5mol·L-1 | B.3mol·L-1 | C.8.4mol·L-1 | D.12.0mol·L-1 |
您最近一年使用:0次
名校
解题方法
8 . 将物质的量浓度为2cmol/L、质量分数为a%的硫酸溶液,加水稀释至物质的量浓度为cmol/L,质量分数变为b%。则a、b之间的大小关系为(已知:硫酸溶液的浓度越大密度越大)
| A.a=2b | B.2b>a | C.a>2b | D.不能比较 |
您最近一年使用:0次
名校
9 . 回答下列问题:
(1)在标准状况下,1.7g氨气所占的体积约为_______ L,它与_______ 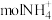 含有相同数目的电子。
含有相同数目的电子。
(2)某气态氧化物化学式为 ,在标准状况下,1.28g该氧化物的体积为448mL,则该氧化物中R的相对原子质量为
,在标准状况下,1.28g该氧化物的体积为448mL,则该氧化物中R的相对原子质量为_______ 。
(3)同温同压下, 与氦气的密度之比为
与氦气的密度之比为_______ ,若质量相同,两种气体的体积比为_______ 。
(4)在标准状况下,将A气体VL(摩尔质量是 )溶于0.5L水中,所得溶液的密度为
)溶于0.5L水中,所得溶液的密度为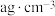 ,则此溶液的物质的量浓度为
,则此溶液的物质的量浓度为_______ 。
(5)现有含 和
和 的混合溶液200mL,其中
的混合溶液200mL,其中 物质的量浓度为
物质的量浓度为 ,
, 物质的量浓度为
物质的量浓度为 ,若向此溶液中加入一定量浓硫酸,使其配成
,若向此溶液中加入一定量浓硫酸,使其配成 和
和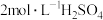 的混合溶液。请问最终所得混合溶液的体积是
的混合溶液。请问最终所得混合溶液的体积是_______ mL,需加入密度为 、质量分数为98%的浓硫酸
、质量分数为98%的浓硫酸_______ mL(保留到小数点后1位)。
(1)在标准状况下,1.7g氨气所占的体积约为
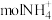 含有相同数目的电子。
含有相同数目的电子。(2)某气态氧化物化学式为
 ,在标准状况下,1.28g该氧化物的体积为448mL,则该氧化物中R的相对原子质量为
,在标准状况下,1.28g该氧化物的体积为448mL,则该氧化物中R的相对原子质量为(3)同温同压下,
 与氦气的密度之比为
与氦气的密度之比为(4)在标准状况下,将A气体VL(摩尔质量是
 )溶于0.5L水中,所得溶液的密度为
)溶于0.5L水中,所得溶液的密度为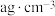 ,则此溶液的物质的量浓度为
,则此溶液的物质的量浓度为(5)现有含
 和
和 的混合溶液200mL,其中
的混合溶液200mL,其中 物质的量浓度为
物质的量浓度为 ,
, 物质的量浓度为
物质的量浓度为 ,若向此溶液中加入一定量浓硫酸,使其配成
,若向此溶液中加入一定量浓硫酸,使其配成 和
和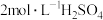 的混合溶液。请问最终所得混合溶液的体积是
的混合溶液。请问最终所得混合溶液的体积是 、质量分数为98%的浓硫酸
、质量分数为98%的浓硫酸
您最近一年使用:0次
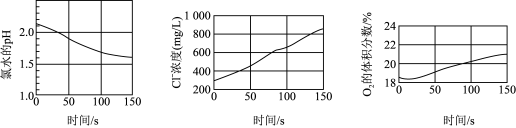
10 . 某兴趣小组利用数字化实验测定光照过程中氯水的 、氯水中氯离子的浓度、广口瓶中氧气的体积分数三者的变化,实验结果如图所示。下列说法正确的是
、氯水中氯离子的浓度、广口瓶中氧气的体积分数三者的变化,实验结果如图所示。下列说法正确的是
 、氯水中氯离子的浓度、广口瓶中氧气的体积分数三者的变化,实验结果如图所示。下列说法正确的是
、氯水中氯离子的浓度、广口瓶中氧气的体积分数三者的变化,实验结果如图所示。下列说法正确的是
A.氯水中存在自由移动的离子,能导电,但 属于非电解质 属于非电解质 |
B.氯水的 值随光照时间增加而减少,是因为次氯酸见光分解为酸性更强的酸 值随光照时间增加而减少,是因为次氯酸见光分解为酸性更强的酸 |
C.光照过程中 体积分数逐渐增加,说明发生了氧化还原反应,其中 体积分数逐渐增加,说明发生了氧化还原反应,其中 为还原产物 为还原产物 |
D.由图可知,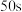 时 时 浓度约为 浓度约为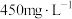 ,计算可知氯水中 ,计算可知氯水中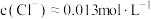 |
您最近一年使用:0次



