回答下列问题:
(1)在标准状况下,1.7g氨气所占的体积约为_______ L,它与_______ 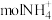 含有相同数目的电子。
含有相同数目的电子。
(2)某气态氧化物化学式为 ,在标准状况下,1.28g该氧化物的体积为448mL,则该氧化物中R的相对原子质量为
,在标准状况下,1.28g该氧化物的体积为448mL,则该氧化物中R的相对原子质量为_______ 。
(3)同温同压下, 与氦气的密度之比为
与氦气的密度之比为_______ ,若质量相同,两种气体的体积比为_______ 。
(4)在标准状况下,将A气体VL(摩尔质量是 )溶于0.5L水中,所得溶液的密度为
)溶于0.5L水中,所得溶液的密度为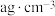 ,则此溶液的物质的量浓度为
,则此溶液的物质的量浓度为_______ 。
(5)现有含 和
和 的混合溶液200mL,其中
的混合溶液200mL,其中 物质的量浓度为
物质的量浓度为 ,
, 物质的量浓度为
物质的量浓度为 ,若向此溶液中加入一定量浓硫酸,使其配成
,若向此溶液中加入一定量浓硫酸,使其配成 和
和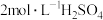 的混合溶液。请问最终所得混合溶液的体积是
的混合溶液。请问最终所得混合溶液的体积是_______ mL,需加入密度为 、质量分数为98%的浓硫酸
、质量分数为98%的浓硫酸_______ mL(保留到小数点后1位)。
(1)在标准状况下,1.7g氨气所占的体积约为
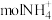 含有相同数目的电子。
含有相同数目的电子。(2)某气态氧化物化学式为
 ,在标准状况下,1.28g该氧化物的体积为448mL,则该氧化物中R的相对原子质量为
,在标准状况下,1.28g该氧化物的体积为448mL,则该氧化物中R的相对原子质量为(3)同温同压下,
 与氦气的密度之比为
与氦气的密度之比为(4)在标准状况下,将A气体VL(摩尔质量是
 )溶于0.5L水中,所得溶液的密度为
)溶于0.5L水中,所得溶液的密度为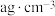 ,则此溶液的物质的量浓度为
,则此溶液的物质的量浓度为(5)现有含
 和
和 的混合溶液200mL,其中
的混合溶液200mL,其中 物质的量浓度为
物质的量浓度为 ,
, 物质的量浓度为
物质的量浓度为 ,若向此溶液中加入一定量浓硫酸,使其配成
,若向此溶液中加入一定量浓硫酸,使其配成 和
和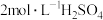 的混合溶液。请问最终所得混合溶液的体积是
的混合溶液。请问最终所得混合溶液的体积是 、质量分数为98%的浓硫酸
、质量分数为98%的浓硫酸
更新时间:2023-12-25 13:01:32
|
相似题推荐
计算题
|
适中
(0.65)
【推荐1】用100 g 9.8% H2SO4溶液和足量金属Zn反应,可以得到标准状况下气体_______ 升?(要求有简要步骤)
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】(1)标准状况下,5.1g NH3与_______ L H2S气体含有的氢原子数相同。
(2)5mol的CO2与6mol的SO3的原子数之比是__________ 。
(3)常温常压下22.4LCO2中分子个数_____ 64克SO2的分子个数(填“>、<或=”)
(4)标准状况下,NH3与CH4组成的混合气体的平均密度为0.75g/L,该混合气体的平均摩尔质量为_________________ ,NH3的体积分数为______________ .
(2)5mol的CO2与6mol的SO3的原子数之比是
(3)常温常压下22.4LCO2中分子个数
(4)标准状况下,NH3与CH4组成的混合气体的平均密度为0.75g/L,该混合气体的平均摩尔质量为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐3】回答下列问题:
(1)3.6gH2O的物质的量是_______ ,含有氢原子的数目是_______ 。
(2)1.5molCO2和_______ gCH4在标准状况下占有相同的体积,其体积为_______ 。
(3)100mL气体A2跟50mL气体B2恰好完全反应生成100mL气体C(体积均在相同条件下测定)则C的化学式为_______ 。
(4)标准状况下,一烧瓶HCl气体倒扣在水槽中,假设溶液没有损失,则所得溶液的物质的量浓度为_______ 。
(5)将4gNaOH溶解在10mL水中,再稀释成1L,从中取出10mL,这10mL溶液的物质的量浓度为_______ 。
(1)3.6gH2O的物质的量是
(2)1.5molCO2和
(3)100mL气体A2跟50mL气体B2恰好完全反应生成100mL气体C(体积均在相同条件下测定)则C的化学式为
(4)标准状况下,一烧瓶HCl气体倒扣在水槽中,假设溶液没有损失,则所得溶液的物质的量浓度为
(5)将4gNaOH溶解在10mL水中,再稀释成1L,从中取出10mL,这10mL溶液的物质的量浓度为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐1】(1)在标准状况下,5.6L A气体的质量是15g,则A的摩尔质量为___ 。
(2)一定量的液态化合物XY2,在一定量的O2中恰好完全燃烧,反应方程式为:XY2(液)+ 3O2(气)= XO2(气)+2YO2(气),冷却后,在标准状况下测得生成物的体积是672mL,密度是2.56g/L,则:
①反应前O2的体积是______ 。
②化合物XY2的摩尔质量是____ 。
③若XY2分子中X、Y两元素的质量之比为3:16,则X、Y两元素分别是_____ 和_____ 。(写元素符号)
(2)一定量的液态化合物XY2,在一定量的O2中恰好完全燃烧,反应方程式为:XY2(液)+ 3O2(气)= XO2(气)+2YO2(气),冷却后,在标准状况下测得生成物的体积是672mL,密度是2.56g/L,则:
①反应前O2的体积是
②化合物XY2的摩尔质量是
③若XY2分子中X、Y两元素的质量之比为3:16,则X、Y两元素分别是
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】NH3和Cl2可快速反应:2NH3+3Cl2→N2+6HCl。有标况下100LNH3和Cl2混合气体,充分反应后的混合气体中N2占混合气体的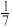 ,则N2的物质的量可能为
,则N2的物质的量可能为
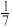 ,则N2的物质的量可能为
,则N2的物质的量可能为| A.0.263mol | B.0.483mol | C.0.526mol | D.0.663mol |
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐3】完成下列填空:
(1)1.204×1024个氯气分子的物质的量是_______ ,0.5mol的 中含有的电子数为
中含有的电子数为_______ 。
(2)同温同压下,同体积的甲烷(CH4)和CO2物质的量之比为_______ ,密度之比为_______ 。
(3)3.1gNa2X含有Na+0.1mol,则Na2X的摩尔质量为_______ ,X的相对原子质量为_______ 。
(4)在标准状况下,CO和CO2的混合气体共6.72L,质量为12g,则混合气体的平均摩尔质量为_______ 。
(1)1.204×1024个氯气分子的物质的量是
 中含有的电子数为
中含有的电子数为(2)同温同压下,同体积的甲烷(CH4)和CO2物质的量之比为
(3)3.1gNa2X含有Na+0.1mol,则Na2X的摩尔质量为
(4)在标准状况下,CO和CO2的混合气体共6.72L,质量为12g,则混合气体的平均摩尔质量为
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】2mol CO2中含有________ mol O原子,含有____________ 个CO2分子,质量为_________ g ;
CO2的摩尔质量是_______________ ,在标准状况下的密度是______________ ,同温同压条件下该气体与氢气的密度之比是______________ 。
CO2的摩尔质量是
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】向含0.02mol Al3+的明矾溶液中逐滴加入0.2mol/L的Ba(OH)2溶液时,测得产生沉淀的质量m和逐滴加入Ba(OH)2溶液的体积V的关系如下图,试填写空白:
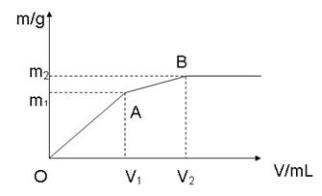
(1)写出OA段反应的离子方程式:OA_______________________ ;
(2)m1=________________ V1=_______________ ;m2=_______________ V2=_________________

(1)写出OA段反应的离子方程式:OA
(2)m1=
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】根据所学知识,回答下列问题:
(1)常温常压下,HCl气体溶于水形成的盐酸溶液,其溶质质量分数为
 ,密度为
,密度为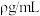 ,该溶液浓度为
,该溶液浓度为 。
。(2)“可燃冰”是由水和甲烷在一定条件下形成的类冰结晶化合物.
 “可燃冰”(
“可燃冰”( )的物质的量与
)的物质的量与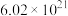 个水分子的物质的量相等,则该“可燃冰”的摩尔质量为
个水分子的物质的量相等,则该“可燃冰”的摩尔质量为(3)过氧化钠可用作呼吸面罩供氧剂,其原理可用方程式
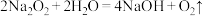 ,
,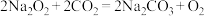 表示。若生成标况下
表示。若生成标况下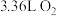 ,转移电子的数目为
,转移电子的数目为(4)现有
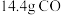 和
和 的混合气体,在标准状况下所占的体积约为
的混合气体,在标准状况下所占的体积约为 。将混合气体依次通过如图装置,最后收集在气球中,气球中收集到的气体在标况下的体积为
。将混合气体依次通过如图装置,最后收集在气球中,气球中收集到的气体在标况下的体积为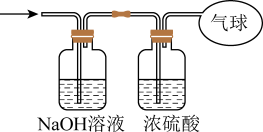
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】完成下列填空:
(1)某市售的浓氨水, 的质量分数为
的质量分数为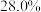 ,密度为
,密度为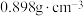 ,则该氨水的物质的量浓度为
,则该氨水的物质的量浓度为___________ 。
(2)已知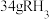 气体中含有
气体中含有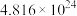 个原子,则该气体的摩尔质量为
个原子,则该气体的摩尔质量为___________ 。
(3)质量为___________  的
的 所含的电子的物质的量为
所含的电子的物质的量为 。
。
(4)质量比为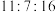 的
的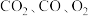 ,其物质的量之比为
,其物质的量之比为___________ 。
(5)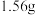 某金属与足量盐酸完全反应,生成
某金属与足量盐酸完全反应,生成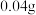 氢气,生成氯化物中金属显
氢气,生成氯化物中金属显 价,则该金属的摩尔质量为
价,则该金属的摩尔质量为___________ 。(写出计算过程)
(1)某市售的浓氨水,
 的质量分数为
的质量分数为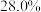 ,密度为
,密度为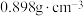 ,则该氨水的物质的量浓度为
,则该氨水的物质的量浓度为(2)已知
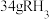 气体中含有
气体中含有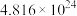 个原子,则该气体的摩尔质量为
个原子,则该气体的摩尔质量为(3)质量为
 的
的 所含的电子的物质的量为
所含的电子的物质的量为 。
。(4)质量比为
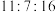 的
的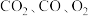 ,其物质的量之比为
,其物质的量之比为(5)
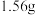 某金属与足量盐酸完全反应,生成
某金属与足量盐酸完全反应,生成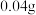 氢气,生成氯化物中金属显
氢气,生成氯化物中金属显 价,则该金属的摩尔质量为
价,则该金属的摩尔质量为
您最近一年使用:0次