1 . 标准状况下,现有①6.72L ;②
;② 个HCl分子;③7.2g
个HCl分子;③7.2g ;④0.2mol
;④0.2mol ,对这四种气体的关系有以下四种表述,其中
,对这四种气体的关系有以下四种表述,其中不 正确的是
 ;②
;② 个HCl分子;③7.2g
个HCl分子;③7.2g ;④0.2mol
;④0.2mol ,对这四种气体的关系有以下四种表述,其中
,对这四种气体的关系有以下四种表述,其中| A.物质的量:②>③>①>④ | B.体积:②>③>①>④ |
| C.氢原子个数:①>③>④>② | D.质量:②>③>①>④ |
您最近一年使用:0次
2022-10-11更新
|
918次组卷
|
8卷引用:黑龙江省哈尔滨师范大学附属中学2023-2024学年高一下学期开学摸底考试化学试卷
名校
2 . 回答下列问题
(1)在标准状况下,测得 某气体的体积为
某气体的体积为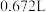 ,该气体的摩尔质量为
,该气体的摩尔质量为_______ 。
(2)将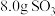 溶于水配成
溶于水配成 溶液,则所得溶液的物质的量浓度为
溶液,则所得溶液的物质的量浓度为_______ 。
(3) 溶液和
溶液和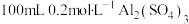 溶液混合后(混合体积变化忽略不计),溶液中
溶液混合后(混合体积变化忽略不计),溶液中 的物质的量浓度为
的物质的量浓度为_______ 。
(4)设 为阿伏加德罗常数的数值,如果
为阿伏加德罗常数的数值,如果 氧气中含有的分子数为b,则
氧气中含有的分子数为b,则 氧气在标准状况下的体积约是
氧气在标准状况下的体积约是_______ (用含 的式子表示)
的式子表示)
(5)标准状况下,将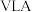 气体(摩尔质量为
气体(摩尔质量为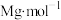 )全部溶于
)全部溶于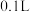 水(水的密度为
水(水的密度为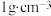 )中(假设气体与水不反应),所得溶液的密度为
)中(假设气体与水不反应),所得溶液的密度为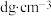 ,则此溶液的物质的量浓度为
,则此溶液的物质的量浓度为_______ 。
(6)某盐混合溶液中含有离子: ,测得
,测得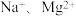 和
和 的物质的量浓度依次为:
的物质的量浓度依次为: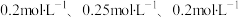 ,则
,则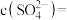
_______ 。
(1)在标准状况下,测得
 某气体的体积为
某气体的体积为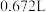 ,该气体的摩尔质量为
,该气体的摩尔质量为(2)将
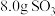 溶于水配成
溶于水配成 溶液,则所得溶液的物质的量浓度为
溶液,则所得溶液的物质的量浓度为(3)
 溶液和
溶液和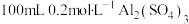 溶液混合后(混合体积变化忽略不计),溶液中
溶液混合后(混合体积变化忽略不计),溶液中 的物质的量浓度为
的物质的量浓度为(4)设
 为阿伏加德罗常数的数值,如果
为阿伏加德罗常数的数值,如果 氧气中含有的分子数为b,则
氧气中含有的分子数为b,则 氧气在标准状况下的体积约是
氧气在标准状况下的体积约是 的式子表示)
的式子表示)(5)标准状况下,将
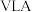 气体(摩尔质量为
气体(摩尔质量为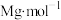 )全部溶于
)全部溶于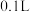 水(水的密度为
水(水的密度为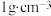 )中(假设气体与水不反应),所得溶液的密度为
)中(假设气体与水不反应),所得溶液的密度为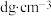 ,则此溶液的物质的量浓度为
,则此溶液的物质的量浓度为(6)某盐混合溶液中含有离子:
 ,测得
,测得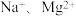 和
和 的物质的量浓度依次为:
的物质的量浓度依次为: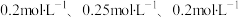 ,则
,则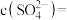
您最近一年使用:0次
2022-10-09更新
|
380次组卷
|
2卷引用:四川省泸州市泸县第四中学2023-2024学年高一下学期开学化学试题
名校
3 . 若NA表示阿伏加德罗常数的值,下列叙述正确的是
①标准状况下,2.24 L苯(C6H6,一种有机溶剂)含碳原子数为0.6NA
②标准状况下,a L氧气和氮气的混合气体中含有的分子数约为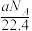
③1 mol/LMg(NO3)2溶液中含有 的数目为2NA
的数目为2NA
④同温同压下,体积相同的氢气和氩气所含的原子数相等
⑤46 gNO2和N2O4混合气体中含有原子数为3NA
⑥1 L0.5 mol/LNa2SO4溶液中,含有的氧原子总数为2NA
①标准状况下,2.24 L苯(C6H6,一种有机溶剂)含碳原子数为0.6NA
②标准状况下,a L氧气和氮气的混合气体中含有的分子数约为
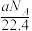
③1 mol/LMg(NO3)2溶液中含有
 的数目为2NA
的数目为2NA④同温同压下,体积相同的氢气和氩气所含的原子数相等
⑤46 gNO2和N2O4混合气体中含有原子数为3NA
⑥1 L0.5 mol/LNa2SO4溶液中,含有的氧原子总数为2NA
| A.②③⑤ | B.②⑤ | C.②⑥ | D.②⑤⑥ |
您最近一年使用:0次
2022-10-09更新
|
282次组卷
|
2卷引用:江苏省苏州市第三中学2023-2024学年高一上学期12月月考化学试题
4 . 设NA为阿伏加德罗常数的值,标准状况下某O2和N2的混合气体mg含有b个分子,则ng该混合气体在相同状况下所占的体积应是
A.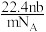 L L | B.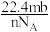 L L |
C.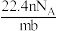 L L | D. |
您最近一年使用:0次
2022-07-08更新
|
555次组卷
|
12卷引用:北京市首都师范大学附属中学2023-2024学年高一下学期开学化学试题
北京市首都师范大学附属中学2023-2024学年高一下学期开学化学试题北京市首都师范大学附属中学2023-2024学年高一下学期3月月考化学(选考)试题上海市南洋模范中学2021-2022学年高一上学期期中考试化学试题河北省邢台市第一中学2021-2022学年高一上学期第三次月考化学试题上海外国语大学附属外国语学校松江云间中学2021-2022学年高一上学期10月测试化学试题甘肃省兰州市第一中学2021-2022学年高一上学期期中考试化学试题湖北省华中师范大学第一附属中学2022-2023学年高一上学期新生入学测试化学试题四川省内江市第六中学2022-2023学年高一上学期第一次月考(创新班)化学试题四川省凉山宁南中学2020-2021学年高一上学期第一次月考化学试题云南省师范大学附属中学2023-2024学年高一上学期入学考化学试题天津市耀华中学2023-2024学年高一上学期11月期中考试化学试题(已下线)考点02 物质的量 气体摩尔体积-备战2023年高考化学一轮复习考点帮(全国通用)
名校
5 . 聚合硫酸铁[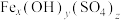 ]是高效水处理剂。以废铁屑(主要成分为铁,杂质为C、Si等)及硫酸为原料,制备聚合硫酸铁的工艺流程如下:
]是高效水处理剂。以废铁屑(主要成分为铁,杂质为C、Si等)及硫酸为原料,制备聚合硫酸铁的工艺流程如下:_______ (一种即可)。
(2)写出反应Ⅰ中生成 的离子方程式为
的离子方程式为_______ 。
(3)已知 溶液脱除空气中
溶液脱除空气中 并再生的原理如图所示。
并再生的原理如图所示。_______ 。
(4)聚合硫酸铁[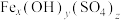 ]的组成可通过下列实验测定:
]的组成可通过下列实验测定:
①称取一定质量的聚合硫酸铁溶于稀盐酸中,往所得溶液中滴加 溶液至沉淀完全,过滤、洗涤、干燥至恒重,得到白色固体11.65g;
溶液至沉淀完全,过滤、洗涤、干燥至恒重,得到白色固体11.65g;
②另称取与①等质量的聚合硫酸铁溶于稀硫酸中,加入足量铜粉,充分反应后过滤、洗涤,将滤液和洗涤液合并配成250.00mL溶液A;
③准确量取25.00mL溶液A,用 的
的 溶液滴定至终点,消耗
溶液滴定至终点,消耗 溶液8.00mL。该步反应为:
溶液8.00mL。该步反应为: (未配平)。
(未配平)。
通过计算确定该聚合硫酸铁的化学式A_______ (写出计算过程)。
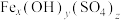 ]是高效水处理剂。以废铁屑(主要成分为铁,杂质为C、Si等)及硫酸为原料,制备聚合硫酸铁的工艺流程如下:
]是高效水处理剂。以废铁屑(主要成分为铁,杂质为C、Si等)及硫酸为原料,制备聚合硫酸铁的工艺流程如下:
(2)写出反应Ⅰ中生成
 的离子方程式为
的离子方程式为(3)已知
 溶液脱除空气中
溶液脱除空气中 并再生的原理如图所示。
并再生的原理如图所示。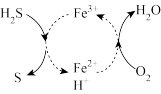
(4)聚合硫酸铁[
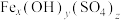 ]的组成可通过下列实验测定:
]的组成可通过下列实验测定:①称取一定质量的聚合硫酸铁溶于稀盐酸中,往所得溶液中滴加
 溶液至沉淀完全,过滤、洗涤、干燥至恒重,得到白色固体11.65g;
溶液至沉淀完全,过滤、洗涤、干燥至恒重,得到白色固体11.65g;②另称取与①等质量的聚合硫酸铁溶于稀硫酸中,加入足量铜粉,充分反应后过滤、洗涤,将滤液和洗涤液合并配成250.00mL溶液A;
③准确量取25.00mL溶液A,用
 的
的 溶液滴定至终点,消耗
溶液滴定至终点,消耗 溶液8.00mL。该步反应为:
溶液8.00mL。该步反应为: (未配平)。
(未配平)。通过计算确定该聚合硫酸铁的化学式A
您最近一年使用:0次
2022-06-28更新
|
405次组卷
|
3卷引用:专题04 金属与人类文明-【好题汇编】备战2023-2024学年高一化学下学期期末真题分类汇编(江苏专用)
(已下线)专题04 金属与人类文明-【好题汇编】备战2023-2024学年高一化学下学期期末真题分类汇编(江苏专用)江苏省盐城市2021-2022学年高一下学期期终考试化学试题江苏省常州高级中学2022-2023学年高一下学期期末质量检查化学试题
6 . 设NA为阿伏加德罗常数的值,下列说法不正确的是
| A.0.2g H2中含有的质子数为0.2NA |
| B.4.6g C2H5OH中含有的氢原子数为0.6NA |
| C.在常温、常压下,1.12L CO2含有的分子数为0.05NA |
| D.在标准状况下,2.24L CH4中含有的共价键数为0.4NA |
您最近一年使用:0次
2022-05-26更新
|
299次组卷
|
2卷引用:湖南省高中2023-2024学年高一下学期学业水平考试复习化学压轴卷
名校
7 . NA为阿伏加德罗常数的值,下列有关叙述正确的是
| A.常温常压下,3.6 g D2O与H218O组成的体系中含有中子数2NA |
| B.标准状况下,11.2 L氖气中所含电子数为0.5NA |
| C.某电池的总反应为Fe+2Fe3+=3Fe2+,当有5.6 g Fe溶解时电路中有0.3NA电子通过 |
D.32 g环状S8(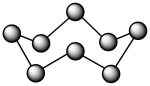 )分子中含有的S—S键数为NA )分子中含有的S—S键数为NA |
您最近一年使用:0次
2022-05-12更新
|
277次组卷
|
5卷引用:河南省南阳市镇平县第一高级中学2023-2024学年高一下学期3月月考化学试题
8 . NA为阿伏加德罗常数。下列说法错误的是
| A.在标准状况下22.4L氩气含有的质子数为18NA |
B.月球土壤中吸附着大量的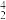 He, He,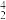 He与 He与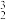 He互为同位素 He互为同位素 |
| C.1molD2O与1molH2O中含有的质子数之比为5:4 |
| D.质量为2.3g的钠离子所含电子数为NA |
您最近一年使用:0次
2022-04-30更新
|
269次组卷
|
3卷引用:辽宁省朝阳市2023-2024学年高一上学期1月期末化学试题
辽宁省朝阳市2023-2024学年高一上学期1月期末化学试题山东省日照市2021-2022学年高一下学期期中校际联考化学试题(已下线)第09练 原子结构与元素周期表-2023年高考化学一轮复习小题多维练(全国通用)
名校
解题方法
9 . 设NA为阿伏加德罗常数的值。下列说法正确的是
| A.标准状况下,2.24 L SO2中含有的质子数为3.2NA |
| B.2 L0.5 mol/L氨水中含有OH-的数目为NA |
| C.在加热条件下,64 g铜与足量硫粉完全反应转移电子数为2 NA |
| D.7.8 g Na2O2固体中含有的阴离子数目为0.2 NA |
您最近一年使用:0次
2022-04-27更新
|
1184次组卷
|
7卷引用:广东省佛山市南海区南海中学分校2023-2024学年高一下学期4月月考化学试题
10 . 设 表示阿伏加德罗常数的值。下列叙述正确的是
表示阿伏加德罗常数的值。下列叙述正确的是
 表示阿伏加德罗常数的值。下列叙述正确的是
表示阿伏加德罗常数的值。下列叙述正确的是A.在常温常压下,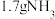 含有的原子数为 含有的原子数为 |
B.标准状况下,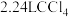 含有的共价键数为 含有的共价键数为 |
C.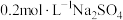 溶液中, 溶液中, 的数目为 的数目为 |
D.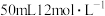 盐酸与足量 盐酸与足量 共热,转移的电子数为 共热,转移的电子数为 |
您最近一年使用:0次
2022-04-19更新
|
1958次组卷
|
14卷引用:安徽省淮北市第一中学2023-2024学年高一下学期开学考试 化学试卷
安徽省淮北市第一中学2023-2024学年高一下学期开学考试 化学试卷人教版(2019)高一必修第一册 全书综合训练(二)湖北省沙洋县沙洋中学2020-2021学年高一下学期3月月考化学试题河南省兰考县第一高级中学2021-2022学年高一上学期期末考试化学试题河南省焦作市武陟县第一中学东校区2021-2022学年高一下学期4月月考化学试题 重庆市万州第二高级中学2022-2023学年高一上学期12月线上考试化学试题吉林省长春市东北师大附属中学2022-2023学年高一上学期期末考试化学试题吉林省东北师范大学附属中学2022-2023学年高一上学期1月期末考试化学试题安徽省马鞍山市第二十二中学2022-2023学年高一下学期2月月考化学试题(已下线)专题05 物质的量-【好题汇编】备战2023-2024学年高一化学上学期期末真题分类汇编(人教版2019必修第一册)吉林省“BEST合作体”2023-2024学年高一上学期期末考试化学试题安徽省舒城中学2021-2022学年高二上学期第一次月考化学试题(已下线)专题02 NA及其应用—2022年高考化学二轮复习讲练测(全国版)-测试河南省温县第一高级中学2021-2022学年高二上学期开学考试化学试题



