1 . 标准状况下,下列物质所占体积最大的是
A.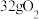 | B.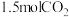 | C. | D.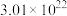 个 个 |
您最近一年使用:0次
名校
2 . NA为阿伏加德罗常数的值,下列说法正确的是
| A.100ml 12mol/L浓盐酸和足量MnO2反应转移电子数为0.6NA |
| B.18gD2O和18gH218O中含有的质子数均为10NA |
| C.78g Na2O2和Na2S的混合物中阴阳离子总数为3NA |
| D.11.2L N2含有的分子数为0.5NA |
您最近一年使用:0次
解题方法
3 . 计算题本题要求写计算过程。
(1)计算出 的物质的量为
的物质的量为___________ 。
(2)配置 溶液,需要NaOH是多少?
溶液,需要NaOH是多少?___________
(1)计算出
 的物质的量为
的物质的量为(2)配置
 溶液,需要NaOH是多少?
溶液,需要NaOH是多少?
您最近一年使用:0次
名校
4 . 设 代表阿伏加德罗常数的值,下列说法正确的是
代表阿伏加德罗常数的值,下列说法正确的是
 代表阿伏加德罗常数的值,下列说法正确的是
代表阿伏加德罗常数的值,下列说法正确的是A.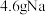 和 和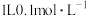 盐酸反应,转移的电子数为 盐酸反应,转移的电子数为 |
B. 个 个 分子在标准状况下的体积约为 分子在标准状况下的体积约为 |
C.常温常压下, 由 由 与 与 组成的混合气体中含有的氧原子总数为 组成的混合气体中含有的氧原子总数为 |
D. 质量分数为 质量分数为 的乙醇 的乙醇 水溶液中含氧原子数目为 水溶液中含氧原子数目为 |
您最近一年使用:0次
5 . 在体积相同的三个密闭容器中分别充入Ne、H2、O2三种气体,当它们的温度与密度都相同时,这三种气体的分子数(N)从大到小的顺序是
A. | B.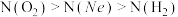 |
C.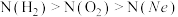 | D.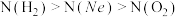 |
您最近一年使用:0次
6 . 某些盐在溶液中结晶时,析出的晶体是结晶水合物。下表记录t℃的4份相同的硫酸铜溶液中加入的无水硫酸铜的质量以及析出的硫酸铜晶体(CuSO4·5H2O)的质量(温度维持不变)的实验数据:
当加入4.6g无水硫酸铜时,析出硫酸铜晶体的质量为
| 硫酸铜溶液 | I | II | III | IV |
| 加入的无水硫酸铜(g) | 2.5 | 4.0 | 6.0 | 8.0 |
| 析出的硫酸铜晶体(g) | 0.1 | 2.8 | 6.4 | 10.0 |
| A.3.42g | B.3.88g | C.6.82g | D.2.56g |
您最近一年使用:0次
解题方法
7 . 质量为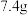 的
的 、
、 、
、 组成的固体混合物溶于水配成
组成的固体混合物溶于水配成 溶液,其中
溶液,其中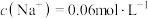 。若把等质量的固体混合物加热至恒重,残留固体的质量是
。若把等质量的固体混合物加热至恒重,残留固体的质量是
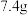 的
的 、
、 、
、 组成的固体混合物溶于水配成
组成的固体混合物溶于水配成 溶液,其中
溶液,其中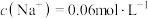 。若把等质量的固体混合物加热至恒重,残留固体的质量是
。若把等质量的固体混合物加热至恒重,残留固体的质量是A.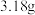 | B.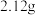 | C.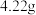 | D. |
您最近一年使用:0次
8 . 4.6g金属钠与足量的H2O反应,回答下列问题:
(1)钠的物质的量是________ ?
(2)钠与水反应生成H2的质量是________ ?
(3)钠与水反应生成H2的体积是________ (标准状况下)?
(4)如果生成溶液的体积是0.5L,求溶液的物质的量浓度是________ ?
(5)该反应中转移的电子数是________ ?
(1)钠的物质的量是
(2)钠与水反应生成H2的质量是
(3)钠与水反应生成H2的体积是
(4)如果生成溶液的体积是0.5L,求溶液的物质的量浓度是
(5)该反应中转移的电子数是
您最近一年使用:0次
9 . 下列物质中,所含分子数最多的是
| A.0.8mol氦气 | B.标况下,4.48 L二氧化硫 |
| C.3.01×1023个甲烷分子 | D.16 g臭氧 |
您最近一年使用:0次
10 . 已知3.01×1022个X2气体分子的质量为1.6 g,则X的相对原子质量为
| A.16 | B.32 | C.64 | D.96 |
您最近一年使用:0次



