名校
解题方法
1 . 棉花与混酸(硝酸和硫酸)反应可制备火棉,用于炸药,其爆炸威力强于黑火药。火棉爆炸反应方程式为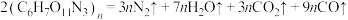 。下列说法错误的是
。下列说法错误的是
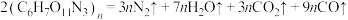 。下列说法错误的是
。下列说法错误的是| A.棉花的主要成分是纤维素 | B. 的电子式为 的电子式为 |
C.反应后混合气体的平均摩尔质量为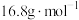 | D. 的空间结构为直线形 的空间结构为直线形 |
您最近一年使用:0次
2 . 下列关于1molHCl的说法中,错误的是(NA表示阿伏加德罗常数的值)
| A.质量为36.5g |
| B.含氢原子数为NA |
| C.体积约为22.4L |
| D.溶于水后,所得1L溶液的物质的量浓度为1mol/L |
您最近一年使用:0次
3 . NA表示阿伏加德罗常数的值。下列叙述正确的是
| A.0.1molFeCl3完全水解转化为氢氧化铁胶体,生成0.1NA个胶粒 |
| B.标准状况下,80gSO3中氧原子数为3NA |
| C.1mol Cl2通入足量水充分反应,转移的电子数为NA |
| D.1 L 1 mol·L−1 NaCl溶液含有28NA个电子 |
您最近一年使用:0次
解题方法
4 . 按要求完成下列填空:
(1)O2-的结构示意图是_______ ;NH3的电子式是_______ 。
(2)CH4分子的空间结构为_______ ;黄铁矿的化学式是_______ 。
(3)下列给定的物质中:①NaCl晶体;②CH3COOH;③镁条;④氨气;⑤液态的HCl。属于非电解质的是_______ (填编号)。
(4)胆矾晶体遇浓硫酸变白,体现了浓硫酸的_______ 性。
(5)若ag某气体中含有的分子数为b,则cg该气体在标准状况下的体积是_______ L(设NA为阿伏加德罗常数的值)。
(1)O2-的结构示意图是
(2)CH4分子的空间结构为
(3)下列给定的物质中:①NaCl晶体;②CH3COOH;③镁条;④氨气;⑤液态的HCl。属于非电解质的是
(4)胆矾晶体遇浓硫酸变白,体现了浓硫酸的
(5)若ag某气体中含有的分子数为b,则cg该气体在标准状况下的体积是
您最近一年使用:0次
5 . 在标准状况下①6.72LC2H6 ②3.01×1023个NH3分子 ③13.6gH2S ④0.6molH2O,下列对这四种气体关系从大到小的表达正确的是
| A.物质的量:③>①>④>② | B.原子数:①>②>④>③ |
| C.体积:④>②>③>① | D.质量:④>③>①>② |
您最近一年使用:0次
名校
6 . 下列物质所含分子数最多的是
A.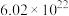 个 个 | B. | C. | D.标准状况下 |
您最近一年使用:0次
名校
7 . 在二氧化碳合成高能量长链食物分子过程中, 、
、 和CO组成的混合气体在同温同压下与氮气的密度相同,此时混合气体中
和CO组成的混合气体在同温同压下与氮气的密度相同,此时混合气体中 、
、 和CO的体积可能为
和CO的体积可能为
 、
、 和CO组成的混合气体在同温同压下与氮气的密度相同,此时混合气体中
和CO组成的混合气体在同温同压下与氮气的密度相同,此时混合气体中 、
、 和CO的体积可能为
和CO的体积可能为| A.9∶3∶7 | B.6∶5∶15 | C.2∶9∶2 | D.7∶4∶12 |
您最近一年使用:0次
8 . 设NA为阿伏加德罗常数的数值,下列说法正确的是
A.常温下,44gCO2含有NA个 原子 原子 |
| B.1L0.1mol•L-1Na2SO4溶液中含有0.1NA个Na+ |
| C.0.1molNa与足量Cl2反应,转移0.2NA个电子 |
| D.标准状况下,22.4L的H2O含有3NA个原子 |
您最近一年使用:0次
2024-03-01更新
|
71次组卷
|
2卷引用:北京九中2023-2024学年高一下学期开学测试化学试题
名校
9 . 现有一份“将二氧化硫转化为硫酸铵”的资料,摘录如下:
一个典型实例:初步处理后的废气含0.20%的二氧化硫和10%的氧气(体积分数)。在400℃时废气以5 m3·h-1的速率通过五氧化二钒催化剂层与20 L·h-1的速率的氨气混合,再喷水,此时气体温度由400℃降至200℃,在热的结晶装置中得到硫酸铵晶体(气体体积均已折算为标准状况)。利用上述资料,用氨来除去工业废气中的二氧化硫,回答下列问题:
(1)按反应中的理论值,二氧化硫和氧气的物质的量之比为2∶1,该资料中这个比值是___________ ,简述不采用2∶1的理由是___________ 。
(2)通过计算,说明为什么废气以5 m3·h-1的速率与20 L·h-1速率的氨气混合___________ 。
(3)若某厂每天排放1×104 m3这种废气,按上述方法该厂每月(按30天计)可得硫酸铵___________ 吨,消耗氨气___________ 吨。
一个典型实例:初步处理后的废气含0.20%的二氧化硫和10%的氧气(体积分数)。在400℃时废气以5 m3·h-1的速率通过五氧化二钒催化剂层与20 L·h-1的速率的氨气混合,再喷水,此时气体温度由400℃降至200℃,在热的结晶装置中得到硫酸铵晶体(气体体积均已折算为标准状况)。利用上述资料,用氨来除去工业废气中的二氧化硫,回答下列问题:
(1)按反应中的理论值,二氧化硫和氧气的物质的量之比为2∶1,该资料中这个比值是
(2)通过计算,说明为什么废气以5 m3·h-1的速率与20 L·h-1速率的氨气混合
(3)若某厂每天排放1×104 m3这种废气,按上述方法该厂每月(按30天计)可得硫酸铵
您最近一年使用:0次
名校
解题方法
10 . Ⅰ.大气臭氧层可以保护地球生物免受紫外线的伤害,但低空臭氧的浓度过高时对人体有害。在紫外线作用下,氧气可转化臭氧:
(1)该反应所属类型为___________ (填“氧化还原”或“非氧化还原”)反应。
(2)若在上述反应中有60%的氧气转化为臭氧,所得混合气体的平均摩尔质量为___________ 。
(3)某区域收集到 和
和 混合气体0.96g,标准状况下,体积为0.56L,其中
混合气体0.96g,标准状况下,体积为0.56L,其中 与
与 的体积之比为
的体积之比为___________ 。
Ⅱ.某研究小组为了检测某加碘盐中是否含有碘,查阅了有关的资料,发现其检测原理是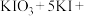
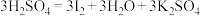 。
。
(4)上述反应中的氧化剂是___________ (填化学式),还原产物与氧化产物的质量之比是___________ 。
(5)上面实验中用到一定物质的量浓度的稀硫酸。
a.若配制0.5mol/L的硫酸溶液450mL,需用量筒量取质量分数为98%、密度为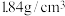 的浓硫酸的体积为
的浓硫酸的体积为___________ mL(保留一位小数),如果实验室有15mL、20mL、50mL量筒,应选用___________ mL量筒最好。
b.下面操作造成所配稀硫酸溶液浓度偏高的是___________ 。
A.用量筒量取浓硫酸时仰视读数
B.转移时没有洗涤烧杯、玻璃棒
C.向容量瓶加水定容时眼睛俯视液面
D.摇匀后发现液面低于刻度线,又加蒸馏水至刻度线

(1)该反应所属类型为
(2)若在上述反应中有60%的氧气转化为臭氧,所得混合气体的平均摩尔质量为
(3)某区域收集到
 和
和 混合气体0.96g,标准状况下,体积为0.56L,其中
混合气体0.96g,标准状况下,体积为0.56L,其中 与
与 的体积之比为
的体积之比为Ⅱ.某研究小组为了检测某加碘盐中是否含有碘,查阅了有关的资料,发现其检测原理是
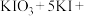
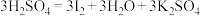 。
。(4)上述反应中的氧化剂是
(5)上面实验中用到一定物质的量浓度的稀硫酸。
a.若配制0.5mol/L的硫酸溶液450mL,需用量筒量取质量分数为98%、密度为
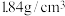 的浓硫酸的体积为
的浓硫酸的体积为b.下面操作造成所配稀硫酸溶液浓度偏高的是
A.用量筒量取浓硫酸时仰视读数
B.转移时没有洗涤烧杯、玻璃棒
C.向容量瓶加水定容时眼睛俯视液面
D.摇匀后发现液面低于刻度线,又加蒸馏水至刻度线
您最近一年使用:0次



