1 . 气态 的一种工业制法流程如图:
的一种工业制法流程如图: 为阿伏加德罗常数的值②
为阿伏加德罗常数的值② 时,次磷酸(
时,次磷酸( )的电离常数
)的电离常数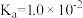 ,下列说法错误的是
,下列说法错误的是
 的一种工业制法流程如图:
的一种工业制法流程如图: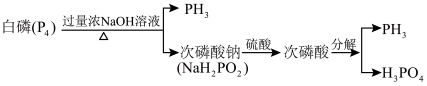
 为阿伏加德罗常数的值②
为阿伏加德罗常数的值② 时,次磷酸(
时,次磷酸( )的电离常数
)的电离常数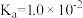 ,下列说法错误的是
,下列说法错误的是| A.液态次磷酸分解反应为熵增过程 |
B. 是非极性分子, 是非极性分子, 所含价层电子对数为 所含价层电子对数为 |
C.白磷与浓 溶液反应生成 溶液反应生成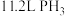 (标准状况下)时,转移电子的数目为 (标准状况下)时,转移电子的数目为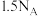 |
D.常温下,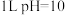 的 的 溶液中由水电离出的 溶液中由水电离出的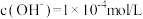 |
您最近一年使用:0次
2024-04-29更新
|
32次组卷
|
2卷引用:湖北省黄冈市2023-2024学年高二上学期期末调研考试化学试题
名校
2 . 设 为阿伏加德罗常数的值,下列叙述中正确的是
为阿伏加德罗常数的值,下列叙述中正确的是
 为阿伏加德罗常数的值,下列叙述中正确的是
为阿伏加德罗常数的值,下列叙述中正确的是A.同温度、同压强下,分别装有 和 和 气体的两个等体积容器中,气体分子数相等 气体的两个等体积容器中,气体分子数相等 |
B.用含 的浓盐酸与足量的 的浓盐酸与足量的 反应,生成的 反应,生成的 在标准状况下的体积为 在标准状况下的体积为 |
C.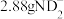 中含有的电子数是 中含有的电子数是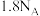 |
D.过氧化钠与水反应时,生成 转移的电子数为 转移的电子数为 |
您最近一年使用:0次
3 .  为阿伏加德罗常数的值。下列叙述正确的是
为阿伏加德罗常数的值。下列叙述正确的是
 为阿伏加德罗常数的值。下列叙述正确的是
为阿伏加德罗常数的值。下列叙述正确的是A.5.6g 与足量稀硫酸完全反应转移电子数为0.3 与足量稀硫酸完全反应转移电子数为0.3 |
B.1  与足量 与足量 完全反应产物中阴离子数一定为2 完全反应产物中阴离子数一定为2 |
C.标准状况下,2.24L氟气含原子数为0.2 |
D.1L0.1  溶液中含氧原子数为1.2 溶液中含氧原子数为1.2 |
您最近一年使用:0次
4 . 设NA为阿伏加德罗常数的值,下列说法正确的是
A.NA个氧分子与NA个氢分子的质量比为 |
B. 的 的 溶液中, 溶液中, 数目为0.2NA 数目为0.2NA |
C.一定量的 与水反应生成 与水反应生成 (标况下),转移的电子数为2NA (标况下),转移的电子数为2NA |
D.常温常压下,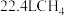 气体含有 气体含有 键的数目为4NA 键的数目为4NA |
您最近一年使用:0次
解题方法
5 . 用 表示阿伏加德罗常数的值。下列说法正确的是
表示阿伏加德罗常数的值。下列说法正确的是
 表示阿伏加德罗常数的值。下列说法正确的是
表示阿伏加德罗常数的值。下列说法正确的是A.用刺有小孔的铝箔包裹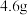 钠,与足量水充分反应,生成 钠,与足量水充分反应,生成 分子数为 分子数为 |
B.不同条件下,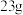 钠在空气中充分反应时转移电子数均为 钠在空气中充分反应时转移电子数均为 |
C.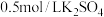 溶液中含有 溶液中含有 的数目为 的数目为 |
D.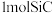 晶体中含有 晶体中含有 的数目为 的数目为 |
您最近一年使用:0次
6 . NA为阿伏加徳罗常数的值,下列说法一定正确的是
| A.4.6g C2H6O中所含“O—H”的数目为0.1NA |
| B.1molNa2O2与足量CO2反应时,转移电子数为2NA |
| C.1L0.3mol/L的FeCl3溶液充分水解可得到Fe(OH)3胶粒的数目为0.3NA |
| D.11 g超重水(T2O)中所含中子数为6NA |
您最近一年使用:0次
2023-07-15更新
|
116次组卷
|
2卷引用:湖北省恩施州教育联盟022-2023学年高二下学期7月期末考试化学试题
7 . 设 为阿伏加德罗常数的值,下列说法错误的是
为阿伏加德罗常数的值,下列说法错误的是
 为阿伏加德罗常数的值,下列说法错误的是
为阿伏加德罗常数的值,下列说法错误的是A.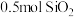 晶体中含 晶体中含 键的数目为 键的数目为 |
B.标准状况下, 与 与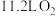 充分反应,得到产物的分子数目为 充分反应,得到产物的分子数目为 |
C.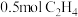 和 和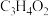 的混合物完全燃烧,消耗 的混合物完全燃烧,消耗 分子数目为 分子数目为 |
D.常温下,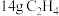 和 和 混合气体所含的共用电子对数目为 混合气体所含的共用电子对数目为 |
您最近一年使用:0次
名校
解题方法
8 . 设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.62g甘醇(乙二醇)中含有羟基数为1 |
B.常温下,0.1mol环氧乙烷( )共有0.3 )共有0.3 个共价键 个共价键 |
C.标准状况下,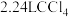 中含有的碳原子数为0.1 中含有的碳原子数为0.1 |
D.标准状况下,11.2L乙烷和丙烯的混合气体中所含碳氢键数为3 |
您最近一年使用:0次
解题方法
9 . 设NA为阿伏伽德罗常数的值。下列说法正确的是
| A.2.0g重水(D2O)中所含中子数为NA |
| B.标准状况下,22.4LCCl4含有的氯原子数为4NA |
| C.1molCl2分别与足量CH4和H2S完全反应,得到的HCl分子数均为2NA |
D.将0.25NA个Cl2与等量H2完全反应后溶于1L水中,所得溶液浓度为 |
您最近一年使用:0次
10 . 用 表示阿伏伽德罗常数的值,下列说法正确的是
表示阿伏伽德罗常数的值,下列说法正确的是
 表示阿伏伽德罗常数的值,下列说法正确的是
表示阿伏伽德罗常数的值,下列说法正确的是A.1 mol Na2O2与足量的SO2反应转移电子数为 |
B.1 L 0.1 mol/L NH4Cl溶液中阳离子的总数大于 |
C.标准状况下,1 L Cl2溶于水形成1 L溶液, 个数为 个数为 |
D.1 mol SiO2含有的共价键数目为 |
您最近一年使用:0次



