名校
解题方法
1 . 锂离子电池的正极材料为LiMn2O4、碳粉及铝箔,某小组设计下列室温下的流程处理废旧锂离子电池的正极材料,下列离子反应方程式书写错误的是


A.加入过量NaOH溶液: |
B.LiMn2O4被氧化: |
C.滤液Ⅱ加入饱和碳酸钠溶液: |
D.滤液I加入过量CO2: ; ; |
您最近一年使用:0次
2022-03-14更新
|
247次组卷
|
14卷引用:广东省广州市第二中学2019-2020学年高二下学期期末考试化学试题
广东省广州市第二中学2019-2020学年高二下学期期末考试化学试题 天津市实验中学2021-2022学年高三上学期第一次阶段考试化学试题 2021年河北省高中名校名师原创预测卷化学(第四模拟)湖北省孝感市孝感高级中学2021届高三2月调研考试化学试题(已下线)热点5 常见元素及其化合物的性质与相互转化-2021年高考化学专练【热点·重点·难点】(新高考)(已下线)难点1 化工流程微设计-2021年高考化学【热点·重点·难点】专练(新高考)(已下线)微专题04 突破离子方程式书写正误判断中的“六大陷阱”-备战2022年高考化学考点微专题山东省济南市历城第二中学2021-2022学年(2022届)高三上学期开学考试(B)化学试题(已下线)第二单元 化学物质及其变化(A卷 新题基础练)-2022年高考化学一轮复习单元滚动双测卷(新高考地区专用)山东省潍坊市第一中学2022届高三10月月考化学试题(已下线)备战2022年高考化学精准检测卷【全国卷】03湖北省安陆市第一高级中学2021-2022学年高一下学期开学考试化学试题吉林省吉林实验中学2021-2022学年上学期高三第一次诊断测试化学试题宁夏回族自治区石嘴山市第三中学2022-2023学年高三上学期第一次月考化学试题
14-15高一上·北京西城·期末
名校
解题方法
2 . 下列反应能用离子方程式H++OH-=H2O表示的是
A.2H2+O2 2H2O 2H2O | B.HCl+NaOH=NaCl+H2O |
| C.2HCl+Cu(OH)2=CuCl2+2H2O | D.Ba(OH)2+H2SO4=BaSO4↓+2H2O |
您最近一年使用:0次
2022-02-18更新
|
1222次组卷
|
17卷引用:2013-2014学年北京市西城区高一上学期期末考试化学试卷
(已下线)2013-2014学年北京市西城区高一上学期期末考试化学试卷2014-2015学年北京市66中高一上学期期中考试化学试卷上海市宝山中学2017-2018学年高三第一学期期中考化学试题北京市丰台区2019-2020学年高一上学期期中考试化学(B卷)试题湖北省鄂东南联盟2019-2020学年高一下学期期中联考化学试题北京市2018年夏季普通高中会考化学试题北京市第四十三中学2020—2021学年高一上学期学期中考试化学试题安徽省六安市城南中学2020-2021学年高一上学期期中考试化学试题天津市第四中学2022-2023学年高一上学期期末考试化学试题天津市和平区2020-2021学年高一上学期期末考试化学试题广西壮族自治区柳州市鹿寨县鹿寨中学2021-2022学年高一上学期12月月考化学试题(已下线)第04讲 离子反应(讲义)-【帮课堂】2022-2023学年高一化学同步精品讲义(人教2019必修第一册 )北京市第四十三中学2022-2023学年高一上学期期中考试化学试题甘肃省平凉市庄浪县阳川中学2022-2023学年高一上学期期中测试化学试题湖南省临湘市第五中学2021-2022学年高一上学期期中考试化学试题陕西省2022-2023学年高二下学期化学学业水平模拟测试(二)四川省阆中东风中学校2023-2024学年高一上学期第一次段考化学试题
名校
3 . FeBr2是一种黄绿色固体,某学习小组制备并探究它的还原性。
Ⅰ.实验室制备FeBr2
实验室用如图所示装置制取溴化亚铁。其中A为CO2发生装置,D和d中均盛有液溴, 为外套电炉丝的不锈钢管,
为外套电炉丝的不锈钢管, 是两个耐高温的瓷皿,其中盛有细铁粉。实验开始时,先将铁粉加热至
是两个耐高温的瓷皿,其中盛有细铁粉。实验开始时,先将铁粉加热至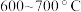 ,然后将干燥、纯净的CO2气流通入D中,
,然后将干燥、纯净的CO2气流通入D中, 管中反应开始。不断将d中液溴滴入温度为
管中反应开始。不断将d中液溴滴入温度为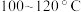 的D中。经过几小时的连续反应,在钢管的一端沉积有黄绿色鳞片状溴化亚铁。
的D中。经过几小时的连续反应,在钢管的一端沉积有黄绿色鳞片状溴化亚铁。


(1)若在A中盛固体CaCO3,a中盛6 mol/L盐酸,为使通入D中的CO2为干燥纯净的气体,则图中B、C处的洗气瓶中的试剂:B为___________ ,C为___________ 。为防止污染空气,实验时应在F处连接盛___________ 的尾气吸收装置。
(2)反应过程中要不断通入CO2,其主要作用是①___________ ,②___________ 。
Ⅱ.探究 的还原性
的还原性
(3)实验需要90 mL0.1 mol/L FeBr2溶液,配制FeBr2溶液除烧杯、量筒、胶头滴管、玻璃棒外,还需要的玻璃仪器是___________ 。
(4)取10mL上述FeBr2溶液,向其中滴加少量新制的氯水,振荡后溶液呈黄色。某同学对产生黄色的原因提出了假设。假设1:Br-被Cl2氧化成Br2溶解在溶液中:假设2:Fe2+被Cl2氧化成Fe3+。设计实验证明假设2正确:___________ 。
(5)请用一个离子方程式来证明还原性Fe2+>Br-:___________ 。
(6)若在40 mL上述FeBr2溶液中通入3×10-3mol Cl2,则反应的离子方程式为___________ 。
Ⅰ.实验室制备FeBr2
实验室用如图所示装置制取溴化亚铁。其中A为CO2发生装置,D和d中均盛有液溴,
 为外套电炉丝的不锈钢管,
为外套电炉丝的不锈钢管, 是两个耐高温的瓷皿,其中盛有细铁粉。实验开始时,先将铁粉加热至
是两个耐高温的瓷皿,其中盛有细铁粉。实验开始时,先将铁粉加热至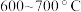 ,然后将干燥、纯净的CO2气流通入D中,
,然后将干燥、纯净的CO2气流通入D中, 管中反应开始。不断将d中液溴滴入温度为
管中反应开始。不断将d中液溴滴入温度为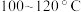 的D中。经过几小时的连续反应,在钢管的一端沉积有黄绿色鳞片状溴化亚铁。
的D中。经过几小时的连续反应,在钢管的一端沉积有黄绿色鳞片状溴化亚铁。

(1)若在A中盛固体CaCO3,a中盛6 mol/L盐酸,为使通入D中的CO2为干燥纯净的气体,则图中B、C处的洗气瓶中的试剂:B为
(2)反应过程中要不断通入CO2,其主要作用是①
Ⅱ.探究
 的还原性
的还原性(3)实验需要90 mL0.1 mol/L FeBr2溶液,配制FeBr2溶液除烧杯、量筒、胶头滴管、玻璃棒外,还需要的玻璃仪器是
(4)取10mL上述FeBr2溶液,向其中滴加少量新制的氯水,振荡后溶液呈黄色。某同学对产生黄色的原因提出了假设。假设1:Br-被Cl2氧化成Br2溶解在溶液中:假设2:Fe2+被Cl2氧化成Fe3+。设计实验证明假设2正确:
(5)请用一个离子方程式来证明还原性Fe2+>Br-:
(6)若在40 mL上述FeBr2溶液中通入3×10-3mol Cl2,则反应的离子方程式为
您最近一年使用:0次
2021-08-05更新
|
260次组卷
|
5卷引用:2017届江西省上高二中高三上学期第三次月考化学试卷
2017届江西省上高二中高三上学期第三次月考化学试卷黑龙江省哈尔滨市第六中学2017届高三下学期第三次模拟考试理科综合化学试题(已下线)【中等生百日捷进提升系列-技能方法】专题27 假设猜想型实验探究评价题天津市新华中学2022-2023学年高三上学期学科练习(一)化学试题重庆市第三十七中学校 2021-2022学年(2022届)高三上学期 7月月考化学试题
9-10高三·江苏·阶段练习
名校
解题方法
4 . 能正确表示下列化学反应的离子方程式的是
| A.氢氧化钡溶液与硫酸的反应:OH-+H+=H2O |
| B.澄清的石灰水与稀盐酸反应:Ca(OH)2+2H+=Ca2++2H2O |
| C.铜片插入硝酸银溶液中:Cu+Ag+=Cu2++Ag |
| D.碳酸钙溶于稀盐酸中:CaCO3+2H+=Ca2++H2O+CO2↑ |
您最近一年使用:0次
2021-03-25更新
|
1158次组卷
|
82卷引用:江苏省2011届高三化学一轮过关测试(10)
(已下线)江苏省2011届高三化学一轮过关测试(10)(已下线)2010年陕西省宝鸡中学高一上学期期中考试化学试卷(已下线)2010年黑龙江“五校联谊”高一上学期期末考试化学卷(已下线)2010—2011学年江苏省如皋市第一中学高二学业水平测试化学试卷(已下线)2011-2012年山西省平遥中学高一上学期期中考试化学(文)试卷(已下线)2011-2012学年广东省新兴县惠能中学高一上学期期中考试化学试卷(已下线)2011-2012学年广东省梅县东山中学高一上学期期中考试化学试卷(已下线)2011-2012学年甘肃省兰州市兰炼一中高一上学期期中考试化学试卷(已下线)2011-2012学年江西省上高二中高一上学期第二次月考化学试卷(已下线)2011-2012学年山东省临清三中高一上学期期末考前考试化学试卷(已下线)2011-2012年度江苏省仪征中学高二第一学期期末模拟考试化学(必修)试卷(已下线)2011-12学年福建莆田十八中高一上学期期未测试(A)化学试卷(已下线)2011-2012学年云南会泽县茚旺高中高一上学期期中考试化学试卷(已下线)2012-2013学年甘肃省天水市一中高一第一学段期中考试化学试卷(已下线)2012-2013学年四川省遂宁二中高一上学期期中考试化学试卷(已下线)2012-2013学年广东惠州实验中学高二上期中考试文科化学试卷(已下线)2012-2013学年山东省聊城市高一上学期七校联考期末检测化学试卷(已下线)2013-2014学年云南省玉溪一中高一上学期期中考试化学试卷2014-2015学年甘肃省武威市六中高一上学期期中化学试卷2014-2015广东省揭阳市三中高一下学期第一次阶段考试文化学试卷2015-2016学年山东省桓台二中高一上学期期中测试化学试卷2015-2016学年安徽省舒城晓天中学高一上学期期中测试化学试卷2015-2016学年广东省清远市梓琛中学高一上学期段考化学试卷2015-2016学年安徽省阜阳市太和八中高一上学期期末文化学试卷2015-2016学年山东省临沂一中高一下学期寒假调研化学试卷2015-2016学年安徽省合肥中科大附中高二下期中文科化学试卷2016-2017学年甘肃省天水一中高一上开学考试化学试卷2016-2017学年福建省厦门一中高一上期中化学卷2016-2017学年河北省定州中学高一12月月考化学试卷黑龙江省哈尔滨市第六中学2017-2018学年高一10月阶段测试化学试题广东省揭阳市第三中学2017-2018学年高一下学期期中考试(文)化学试题吉林省长春汽车经济开发区第六中学2017-2018学年高一上学期期中考试化学试题(已下线)2018年10月24日 《每日一题》人教必修1 离子方程式的书写与正误判断(已下线)【走进新高考】(人教版必修一)高一上学期期中复习模拟(A卷)(基础篇)02广东省广州市中山大学附属中学2018-2019学年高一第一学期期中考试化学试题湖北省利川市第五中学2018-2019学年高一上学期期中模拟考试化学试题广西蒙山县第一中学2018-2019学年高一上学期第二次月考化学试题黑龙江省牡丹江市第三高级中学2018-2019学年高一上学期期中考试化学试题河南省信阳市罗山高级中学2018-2019学年高一上期期中考试化学试题内蒙古自治区正镶白旗察汗淖中学2018-2019学年高一上学期期末考试化学试题江苏省泰州市第二中学2018-2019学年高一上学期期中考试化学试题广东省揭西县河婆中学2018-2019学年高一上学期期末考试化学试题黑龙江省牡丹江市第三高级中学2019-2020学年高一上学期期中考试化学试题广西壮族自治区百色市田阳高中2019-2020学年高一上学期期中考试化学试题福建省厦门集美中学2017-2018学年高一上学期期中考试化学试题四川省自贡市田家炳中学2019-2020学年高一上学期期中考试化学试题黑龙江省哈尔滨市阿城区龙涤中学2019-2020学年高一上学期第一次段考化学试题湖南省张家界市民族中学2019-2020学年高一上学期第三次月考化学试题湖南省张家界市2018-2019学年高一上学期期末考试化学试题湖北省荆州市沙市中学高一化学第二章化学物质及其变化过关训练13广东省广州市天河区华南师范大学附属中学高三化学专题训练(6)河北省邢台市第七中学2018-2019学年高一下学期期中考试化学试题湖南省常德市一中2020-2021学年高一上学期10月月考化学试题新疆乌鲁木齐市第四中学2020-2021学年高一上学期期中考试化学试题新疆生产建设兵团第十师北屯高级中学2020-2021学年高一上学期阶段性检测化学试题广西岑溪市2020-2021学年高一上学期期中考试化学试题天津市滨海新区汉沽第六中学2020-2021学年高一上学期期中化学试题江西省宜春市第九中学2020-2021学年高一上学期第二次月考化学试题黑龙江省漠河市高级中学2020-2021学年高一上学期12月考化学试题海南省海南鑫源高级中学2019-2020学年高一上学期期中考试化学试题云南省文山州砚山县第三高级中学2020-2021学年高一上学期期中考试化学试题吉林省长春市第二十中学2020-2021学年高一上学期第二次考试化学试题(已下线)【浙江新东方】【2021.4.27】【宁波】【高一上】【高中化学】【00146】湖北省长阳县第一高级中学2017-2018学年高一上学期期中考试化学试题山东省青岛市第十七中学2020-2021学年高一上学期期中考试化学试题天津市海河中学2022-2023学年高一上学期期末化学限时训练化学试题新疆维吾尔自治区呼图壁县第一中学2020-2021学年高一下学期期初考试化学试题山西省陵川县平城中学2021-2022学年高一上学期第一次月考化学试题河南省濮阳市第一高级中学2021-2022学年高一上学期期中考试化学试题河南省濮阳市油田第一中学2021年高一上学期第一次月考化学试题贵州省“三新”改革联盟2021-2022学年高一下学期校联考试题化学合格考试题(四)天津市西青区杨柳青一中2022-2023学年高一上学期线上学习效果反馈化学试题四川省泸县第四中学2022-2023学年高一上学期期中考试化学试题新疆柯坪县柯坪湖州国庆中学2021-2022学年高一上学期期中考试化学试题宁夏银川市景博中学2021-2022学年高一上学期期中考试化学试题湖南省株洲市渌口区第三中学2021-2022学年高一上学期期中考试化学试题宁夏回族自治区青铜峡市2022-2023学年高一上学期期中考试化学试题 天津市红桥区2022-2023学年高一学业水平模拟考试化学试题甘肃省部分学校2023-2024学年高一上学期10月期中考试化学试题(已下线)合格考汇编2离子反应 天津市第二南开学校2023-2024学年高一上学期期中考试化学试卷上海市第三女子中学2023-2024学年高二上学期期末化学合格考试题
解题方法
5 . 下列反应的离子方程式正确的是
A.向 溶液中通入 溶液中通入 : :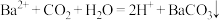 |
B.用醋酸除去水垢中的 : :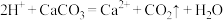 |
C.向硫酸铝溶液中滴加碳酸钠溶液: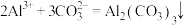 |
D.铜与浓硝酸的反应: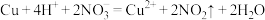 |
您最近一年使用:0次
2020-12-08更新
|
148次组卷
|
4卷引用:天津市河西区2021届高三上学期期中考试化学试题
名校
解题方法
6 . 下列离子方程书写正确的是
A.过量的 ,通入 ,通入 溶液中: 溶液中: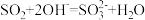 |
B. 溶于过量氢碘酸溶液中: 溶于过量氢碘酸溶液中: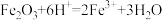 |
C. 溶液中加入过量的 溶液中加入过量的 溶液: 溶液: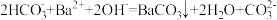 |
D.将 滴入酸性 滴入酸性 溶液中: 溶液中: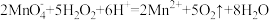 |
您最近一年使用:0次
2020-11-27更新
|
247次组卷
|
2卷引用:山东省泰安市2021届高三上学期期中考试化学试题
名校
解题方法
7 . 下列水溶液中的电离方程式错误的是( )
A.Na2CO3=2Na++CO | B.NaHSO4=Na++H++SO |
C.MgCl2=Mg2++Cl | D.Ba(OH)2=Ba2++2OH- |
您最近一年使用:0次
2020-11-05更新
|
197次组卷
|
5卷引用:辽宁省盘锦市第二高级中学2020-2021学年高一上学期第一次阶段性考试化学试题
名校
解题方法
8 . 下列各组中两稀溶液间的反应可以用同一个离子方程式表示的是
| A.H2SO4溶液(足量)与K2CO3溶液;HNO3溶液(足量)与Na2CO3溶液 |
| B.CH3COOH溶液与KOH溶液;盐酸与NaOH溶液 |
| C.BaCl2溶液与Na2SO4溶液;Ba(OH)2溶液与H2SO4溶液 |
| D.H2SO4溶液与NaOH溶液;H2SO4溶液与Ba(OH)2溶液 |
您最近一年使用:0次
2020-10-23更新
|
224次组卷
|
6卷引用:重庆市万州第三中学2020-2021学年高一上学期第一次月考化学试题
名校
解题方法
9 . 下列方程式正确的是
A.饱和 溶液与 溶液与 固体反应: 固体反应: |
B.酸化 和 和 的混合溶液: 的混合溶液: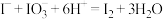 |
C. 碱性溶液与 碱性溶液与 反应: 反应: |
D.电解熔融 的阳极反应: 的阳极反应: |
您最近一年使用:0次
名校
解题方法
10 . 下列化学方程式或离子方程式书写正确的是( )
A.钠在空气中燃烧:4Na+O2 2Na2O 2Na2O |
B.Na2S2O3溶液与稀硫酸的反应:S2O +4H+═SO3+S↓+2H2O +4H+═SO3+S↓+2H2O |
C.浓硝酸与铜片的反应:Cu+4H++2NO =Cu2++2NO2↑+2H2O =Cu2++2NO2↑+2H2O |
| D.用铁氰化钾溶液检验Fe2+:Fe2++[Fe(CN)6]2-═Fe[Fe(CN)6]↓ |
您最近一年使用:0次
2020-06-18更新
|
287次组卷
|
2卷引用:天津市河西区2020届高三总复习质量调查(二)化学试题



