1 . 书写下列反应的离子方程式。
①Na2CO3溶液和H2SO4溶液:___ ;
②KCl溶液和AgNO3溶液:___ ;
③NaOH溶液和NaHSO4溶液:___ 。
①Na2CO3溶液和H2SO4溶液:
②KCl溶液和AgNO3溶液:
③NaOH溶液和NaHSO4溶液:
您最近一年使用:0次
名校
2 . 下列离子方程式中,书写正确的是( )
| A.铁与稀盐酸反应:2Fe+6H+=2Fe3++3H2↑ |
| B.稀硫酸与氢氧化钡溶液反应:Ba2++H++OH-+SO42-=H2O+BaSO4↓ |
| C.碳酸钙与稀盐酸反应:CaCO3+2H+=Ca2++CO2↑+H2O |
| D.铜片跟硝酸银溶液反应:Cu+Ag+=Cu2++Ag |
您最近一年使用:0次
2019-11-11更新
|
315次组卷
|
9卷引用:天津市蓟州区擂鼓台中学2020-2021学年高一上学期第一次月考化学试题
天津市蓟州区擂鼓台中学2020-2021学年高一上学期第一次月考化学试题山东省淄博市淄川区般阳中学2019-2020学年高一10月月考化学试题山东省济南外国语学校三箭分校2019-2020学年高一上学期期中考试化学试题山东省济南外国语学校2019-2020学年高一上学期期中考试化学试题湖北省黄冈市麻城市实验高中2020-2021学年高一上学期10月月考化学试题黑龙江省绥化市第一中学2020-2021学年高一上学期第一次月考化学试题辽宁省锦州市第二高级中学2020-2021学年高一上学期第一次月考化学试题吉林省油田高级中学2019-2020学年高一上学期期中考试化学试题云南省富源一中2021-2022学年高一下学期期末考试化学(文科)试题
解题方法
3 . 元素化合物在日常生活、化工生产和环境科学中有着重要的用途。
(1)生铁中含有一种铁碳化合物X(Fe3C)。X在足量的空气中高温煅烧,生成有磁性的固体Y,将Y溶于过量盐酸后溶液中大量存在的阳离子是______________ 。
(2)自然界中Cr主要以+3价和+6价形式存在。Cr2O 中的Cr能引起细胞的突变,可以用亚硫酸钠在酸性条件下将Cr2O
中的Cr能引起细胞的突变,可以用亚硫酸钠在酸性条件下将Cr2O 还原。写出反应的离子方程式:
还原。写出反应的离子方程式:___________________________________________ 。
(3)当皮肤划破时可用FeCl3溶液应急止血,其主要作用是__________________ 。
(4)高铁酸钾(K2FeO4)是一种既能杀菌、消毒、又能絮凝净水的水处理剂。工业制备高铁酸钾的反应离子方程式Fe(OH)3+ C1O-+ OH-→ FeO + C1-+ H2O(未配平),Fe(OH)3与 C1O-的计量数比为:
+ C1-+ H2O(未配平),Fe(OH)3与 C1O-的计量数比为:__________ ,每生成1mol K2FeO4,转移的电子数是_________ 。
(5)合成氨及其相关工业中,部分物质间的转化关系如下:
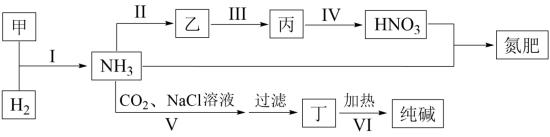
反应IV属于___________ 反应类型,氮肥主要成分的化学式为_______________ ,V的化学反应方程式为_________________ 。
(1)生铁中含有一种铁碳化合物X(Fe3C)。X在足量的空气中高温煅烧,生成有磁性的固体Y,将Y溶于过量盐酸后溶液中大量存在的阳离子是
(2)自然界中Cr主要以+3价和+6价形式存在。Cr2O
 中的Cr能引起细胞的突变,可以用亚硫酸钠在酸性条件下将Cr2O
中的Cr能引起细胞的突变,可以用亚硫酸钠在酸性条件下将Cr2O 还原。写出反应的离子方程式:
还原。写出反应的离子方程式:(3)当皮肤划破时可用FeCl3溶液应急止血,其主要作用是
(4)高铁酸钾(K2FeO4)是一种既能杀菌、消毒、又能絮凝净水的水处理剂。工业制备高铁酸钾的反应离子方程式Fe(OH)3+ C1O-+ OH-→ FeO
 + C1-+ H2O(未配平),Fe(OH)3与 C1O-的计量数比为:
+ C1-+ H2O(未配平),Fe(OH)3与 C1O-的计量数比为:(5)合成氨及其相关工业中,部分物质间的转化关系如下:

反应IV属于
您最近一年使用:0次
4 . 某化学兴趣小组设计如下实验方案。将浓硫酸与铜片反应制备SO2并进行相关实验探究,实验装置如图所示。请回答下列问题:
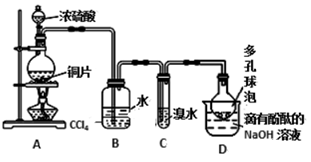
(1)装置B的作用是________________ 。
(2)装置C中发生反应的离子方程式是_____________________________ 。
SO2在装置D中完全转化为酸式酸根离子的过程中,溶液颜色变化是________ 。
(3)已知酸性:HCl>H2SO3>HClO。向Na2SO3溶液中加入盐酸酸化的NaClO溶液时,证明NaClO不足时的试剂是________ 。
(4)请设计简单实验证明:室温下HSO3-的电离平衡常数Ka大于其水解平衡常数Kh。______________ 。

(1)装置B的作用是
(2)装置C中发生反应的离子方程式是
SO2在装置D中完全转化为酸式酸根离子的过程中,溶液颜色变化是
(3)已知酸性:HCl>H2SO3>HClO。向Na2SO3溶液中加入盐酸酸化的NaClO溶液时,证明NaClO不足时的试剂是
(4)请设计简单实验证明:室温下HSO3-的电离平衡常数Ka大于其水解平衡常数Kh。
您最近一年使用:0次
5 . 下列反应的离子方程式书写正确的是
| A.向氯化铁溶液中加入过量的硫化钠:2Fe3++S2- = 2Fe2++S↓ |
| B.氢氧化铁溶于氢碘酸溶液:Fe(OH)3+ 3H+ = Fe3++ 3H2O |
C.硫酸铝溶液中加入过量氨水:Al3++ 4 NH3·H2O=AlO2- +4 NH + 2 H2O + 2 H2O |
| D.向NaHSO4溶液滴加Ba(OH)2溶液至中性:2H++SO42-+ Ba2++ 2OH-=BaSO4↓+2H2O |
您最近一年使用:0次
6 . 下列反应的离子方程式书写正确的是
| A.将鸡蛋壳在醋酸中溶解有气泡产生:CaCO3+2H+==Ca2++H2O+CO2↑ |
| B.NaHCO3与少量的Ca(OH)2溶液反应:2HCO3- + Ca2+ + 2OH- == CaCO3↓+ CO3 2- + 2H2O |
| C.将Cu丝插入AgNO3溶液中:Cu+Ag+==Cu2++Ag |
| D.将铝片放入少量NaOH溶液中:2Al+2NaOH+2H2O==2Al(OH)3↓+3H2↑ |
您最近一年使用:0次



