解题方法
1 . 某化学小组探究硫酸铁铵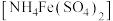 与
与 、
、 的反应。
的反应。
已知: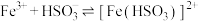 (棕红)
(棕红)
(1)①实验Ⅰ中产生红褐色沉淀与气泡的离子方程式为___________ 。
②由实验Ⅰ可得出与 结合的能力:
结合的能力:
___________  (填“>”、“<”、“=”)。
(填“>”、“<”、“=”)。
(2)资料显示, 可以氧化
可以氧化 。针对实验Ⅱ中的现象,小组同学又设计并实施了如下实验。
。针对实验Ⅱ中的现象,小组同学又设计并实施了如下实验。
①实验Ⅲ中 与
与 反应生成
反应生成 的离子方程式为
的离子方程式为___________ 。
②结合化学反应原理解释实验Ⅱ、Ⅳ中现象存在差异的可能原因___________ 。
(3)针对实验Ⅲ、Ⅳ的现象差异,小组同学提出猜想:pH影响了 的氧化性或
的氧化性或 的还原性,并实施实验。
的还原性,并实施实验。
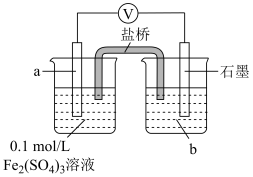
①a、b分别是___________ 。
②结合电极反应解释步骤3中电压表示数减小的原因___________ 。
③补充实验Ⅵ:向实验Ⅱ得到的棕红色液体中加入3滴10%稀硫酸,棕红色迅速变黄,检测到 。结合化学用语解释实验Ⅵ中氧化还原反应明显加快的可能原因
。结合化学用语解释实验Ⅵ中氧化还原反应明显加快的可能原因___________ 。
(4)综合以上实验,盐溶液间反应的多样性与___________ 有关。
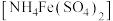 与
与 、
、 的反应。
的反应。| 实验 | 操作 | 现象 |
| Ⅰ | 向2mL 溶液(pH=2.03)中逐滴加入 溶液(pH=2.03)中逐滴加入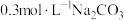 溶液 溶液 | 迅速产生大量红褐色沉淀和大量气泡;继续滴加,当气泡量明显减少时,试管口的湿润红色石蕊试纸开始逐渐变蓝 |
| Ⅱ | 向2mL 溶液(pH=2.03)中逐滴加入 溶液(pH=2.03)中逐滴加入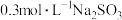 溶液 溶液 | 溶液立即变棕红(无丁达尔现象),继续滴加 溶液至过量,溶液依然为棕红色,放置两天无明显变化 溶液至过量,溶液依然为棕红色,放置两天无明显变化 |
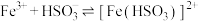 (棕红)
(棕红)(1)①实验Ⅰ中产生红褐色沉淀与气泡的离子方程式为
②由实验Ⅰ可得出与
 结合的能力:
结合的能力:
 (填“>”、“<”、“=”)。
(填“>”、“<”、“=”)。(2)资料显示,
 可以氧化
可以氧化 。针对实验Ⅱ中的现象,小组同学又设计并实施了如下实验。
。针对实验Ⅱ中的现象,小组同学又设计并实施了如下实验。| 实验 | 操作 | 现象 |
| Ⅲ | 向2mL 溶液(pH=1.78)中加入0.5mL 溶液(pH=1.78)中加入0.5mL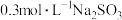 溶液 溶液 | 溶液立即变棕红色,约2小时后,棕红色变为黄色,检测到 |
| Ⅳ | 向2mL 溶液(pH=2.03)中加入0.5mL 溶液(pH=2.03)中加入0.5mL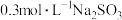 溶液 溶液 | 溶液立即变棕红色,约5小时后,棕红色变为黄色,检测到 |
 与
与 反应生成
反应生成 的离子方程式为
的离子方程式为②结合化学反应原理解释实验Ⅱ、Ⅳ中现象存在差异的可能原因
(3)针对实验Ⅲ、Ⅳ的现象差异,小组同学提出猜想:pH影响了
 的氧化性或
的氧化性或 的还原性,并实施实验。
的还原性,并实施实验。| 实验 | 实验装置 | 实验步骤及现象 |
| Ⅴ |
| 1.按如图搭好装置,接通电路,电压表读数为0.6V; 2.向a电极附近滴加3滴10%稀硫酸,电压表读数不变; 3.向石墨电极附近滴加3滴10%稀硫酸,电压表读数变为0.5V。 |
②结合电极反应解释步骤3中电压表示数减小的原因
③补充实验Ⅵ:向实验Ⅱ得到的棕红色液体中加入3滴10%稀硫酸,棕红色迅速变黄,检测到
 。结合化学用语解释实验Ⅵ中氧化还原反应明显加快的可能原因
。结合化学用语解释实验Ⅵ中氧化还原反应明显加快的可能原因(4)综合以上实验,盐溶液间反应的多样性与
您最近一年使用:0次
2012·辽宁·一模
2 . 某实验小组为探究ClO-、I2、SO42-在酸性条件下的氧化性强弱,设计实验如下:
实验①:
在淀粉碘化钾溶液中加入少量次氯酸钠溶液,并加入少量的稀硫酸,溶液立即变蓝;
实验②:
向实验①的溶液中加入4 mL 0.5 mol/L的亚硫酸钠溶液,蓝色恰好完全褪去。
(1)写出实验①中发生反应的离子方程式____________________________ 。
(2)实验②中化学反应转移电子的物质的量是_______________________ 。
(3)以上实验说明,在酸性条件下ClO-、I2、SO42-的氧化性由弱到强的顺序是_________________ 。
实验①:
在淀粉碘化钾溶液中加入少量次氯酸钠溶液,并加入少量的稀硫酸,溶液立即变蓝;
实验②:
向实验①的溶液中加入4 mL 0.5 mol/L的亚硫酸钠溶液,蓝色恰好完全褪去。
(1)写出实验①中发生反应的离子方程式
(2)实验②中化学反应转移电子的物质的量是
(3)以上实验说明,在酸性条件下ClO-、I2、SO42-的氧化性由弱到强的顺序是
您最近一年使用:0次
名校
解题方法
3 . HNO2是一种不稳定的弱酸,易分解为NO和NO2;有氧化性和还原性,可以把Fe2+氧化为Fe3+;AgNO2难溶于水。下列说法不正确的是
| A.NaNO2溶液加入到新制的氯水中,氯水会褪色 |
B.AgNO2固体加入到新制的氯水中,发生的离子反应为:2Ag++ +Cl2= +Cl2= +2AgCl↓ +2AgCl↓ |
| C.HNO2和浓硝酸都有不稳定性,久置后都会显淡黄色 |
| D.人若误食亚硝酸盐(如NaNO2),会导致血红蛋白中的Fe2+被氧化为Fe3+而中毒 |
您最近一年使用:0次
2020-09-25更新
|
268次组卷
|
6卷引用:北京市清华大学附属中学中学生标准学术能力基础性测试2021届高三9月测试化学试题
名校
解题方法
4 . “84”消毒液(有效成分为NaClO)可用于消毒和漂白,对下列实验现象的分析错误的是
实 |
|
|
|
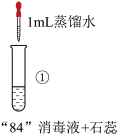
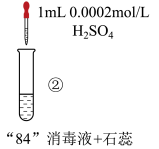
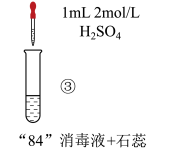
现 | 混合后溶液的pH=9.9,短时间内未褪色,一段时间后蓝色褪去。 | 混合后溶液pH=5.0,蓝色迅速褪去,无气体产生。 | 混合后溶液pH=3.2,蓝色迅速褪去,并产生大量气体,使湿润的淀粉碘化钾试纸变蓝。 |
| A.实验③中产生的气体是Cl2,由HClO分解得到:2HClO=Cl2↑+H2O |
| B.对比实验①和②,②中蓝色迅速褪去的原因是发生了反应ClO-+H+=HClO |
| C.对比实验②和③,溶液的pH可能会影响ClO-的氧化性或Cl-的还原性 |
| D.加酸可以提高“84”消毒液的漂白效果,但需要调控到合适的pH才能安全使用 |
您最近一年使用:0次
2020-03-02更新
|
752次组卷
|
16卷引用:北京市第二十二中学2021-2022学年高三上学期12月阶段性测试理科化学试题
北京市第二十二中学2021-2022学年高三上学期12月阶段性测试理科化学试题【全国百强校】湖南省长沙市雅礼中学2019届高三上学期月考(七)理科综合化学试题湖北名师联盟(人教版)2019-2020学年高三上学期第二次月考精编仿真金卷化学试题福建省福建师范大学附属中学2020届高三上学期期中考试化学试题2019年秋高三化学复习强化练习—— 物质的性质探究实验2020届高三化学二轮冲刺新题专练——氯及其化合物夯基提能2020届高三化学选择题对题专练——选修4化学反应原理——盐类水解平衡的影响因素及探究安徽省六安市第一中学2020届高三下学期自测卷(一)湖南省五市十校2020届高三上学期第二次联考化学试题重庆市第七中学校2020-2021学年高三下学期第一次学情检测化学试题甘肃省兰州市第二十七中学2022届高三上学期8月月考化学试题(已下线)专题07 非金属及其化合物-2022年高考化学二轮复习重点专题常考点突破练黑龙江省哈尔滨市第三中学校2022-2023学年高三上学期第一次验收考试化学试题黑龙江省哈尔滨市第三中学校2022-2023学年高三上学期9月月考化学试题湖南省常德市桃源县第一中学2022-2023学年高三上学期9月月考化学试题湖南省长沙市第一中学2023-2024学年高三上学期月考(一)化学试题
名校
解题方法
5 . 下列对实验现象解释的方程式中,正确的是
A.在煤中添加石灰石,降低尾气中SO2浓度:2CaCO3+2SO2+O2 2CaSO4+2CO2 2CaSO4+2CO2 |
| B.0.1mol/L次氯酸溶液的pH约为4.2:HClO=H++ClO- |
C.H2C2O4有还原性,可使酸性高锰酸钾溶液褪色:2MnO +5C2O +5C2O +16H+=2Mn2++10CO2↑+8H2O +16H+=2Mn2++10CO2↑+8H2O |
D.向NaHSO4溶液中加入足量Ba(OH)2溶液,得到白色沉淀:2H++SO +Ba2++2OH-=BaSO4↓+2H2O +Ba2++2OH-=BaSO4↓+2H2O |
您最近一年使用:0次
名校
解题方法
6 . 下列解释事实的方程式不正确的是
| A.醋酸溶液显酸性:CH3COOH⇌H++CH3COO- |
| B.用氨水除去烟气中的SO2:SO2+2NH3•H2O=(NH4)2SO3+H2O |
| C.向盐碱地中施放硫酸钙,降低其碱性:Na2CO3+CaSO4=CaCO3+Na2SO4 |
| D.用三氯化铁溶液腐蚀线路板:Fe3++Cu=Fe2++Cu2+ |
您最近一年使用:0次
7 . 探究草酸(H2C2O4)性质,进行如下实验。(已知:室温下,0.1 mol·L−1 H2C2O4的pH=1.3)
由上述实验所得草酸性质所对应的方程式不正确的是
| 实验 | 装置 | 试剂a | 现象 |
| ① |  | Ca(OH)2溶液(含酚酞) | 溶液褪色,产生白色沉淀 |
| ② | 少量NaHCO3溶液 | 产生气泡 | |
| ③ | 酸性KMnO4溶液 | 紫色溶液褪色 | |
| ④ | C2H5OH和浓硫酸 | 加热后产生有香味物质 |
由上述实验所得草酸性质所对应的方程式不正确的是
| A.H2C2O4有酸性,Ca(OH)2+ H2C2O4=CaC2O4↓+2H2O |
| B.酸性:H2C2O4> H2CO3,NaHCO3+ H2C2O4=NaHC2O4+CO2↑+H2O |
C.H2C2O4具有还原性,2 +5 +5 +16H+=2Mn2++10CO2↑+ 8H2O +16H+=2Mn2++10CO2↑+ 8H2O |
D.H2C2O4可发生酯化反应,HOOCCOOH+2C2H5OH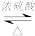 C2H5OOCCOOC2H5+2H2O C2H5OOCCOOC2H5+2H2O |
您最近一年使用:0次
2019-06-09更新
|
9629次组卷
|
68卷引用:2019年北京高考化学试题
2019年北京高考化学试题北京市延庆区2021届高三上学期统测(9月)考试化学试题北京市第一〇一中学2021届高三上学期9月月考化学试题(已下线)北京市第四中学2021-2022学年高三上学期期中考试化学试题北京市昌平区第二中学2022-2023 学年高三上学期期中考试化学试题(已下线)T11-物质性质的探究北京市海淀区中关村中学2021-2022学年高三上学期10月月考化学试题北京师范大学附属实验中学2023-2024学年高三上学期开学摸底测试化学试题北京市第六十五中学2023-2024学年高三上学期期中达标测试化学试题北京工业大学附属中学2022-2023学年高三上学期开学测试化学试题北京市第十四中学2023-2024学年高三上学期10月月考化学试题北京市第三中学2021-2022学年高三上学期期中考试化学试题福建省漳州市华安一中、龙海二中2020届高三上学期第一次联考化学试题2020届高考化学小题狂练(全国通用版)专练19 化学实验基础(已下线)考点24 元素与理论综合——《备战2020年高考精选考点专项突破题集》(已下线)考点26 高三化学一轮成果检测卷B——《备战2020年高考精选考点专项突破题集》2019年秋高三化学复习强化练习—— 氧化还原反应2020届高三化学大二轮增分强化练——与量有关的离子方程式2019年秋高三化学复习强化练习—— 物质的性质探究实验2020届高考化学知识点必练——氧化还原反应的规律专题1.2 离子反应(疑难突破)——巅峰冲刺2020年高考化学二轮专项提升(已下线)【南昌新东方】 莲塘一中2020届高三10月质量检测(已下线)专题五 离子反应(真题汇编)-2020年高考二轮模块化复习之《化学基本概念》名师讲案与提分特训(已下线)第3讲 离子反应-2021年高考化学一轮复习名师精讲练(已下线)第二章 能力提升检测卷(测)——2021年高考化学一轮复习讲练测(已下线)小题必刷03 电解质与离子方程式——2021年高考化学一轮复习小题必刷(通用版)(已下线)易错04 离子方程式正误判断-备战2021年高考化学一轮复习易错题(已下线)小题必刷06 与量有关的离子方程式书写——2021年高考化学一轮复习小题必刷(通用版)河南省郑州市第一中学2020届高三12月联考化学试题甘肃省白银市会宁县第四中学2021届高三上学期第一次月考化学试题内蒙古通辽市开鲁县第一中学2021届高三上学期第一次月考化学试题(已下线)易错20 表格类化学实验选择题-备战2021年高考化学一轮复习易错题福建省福州市格致中学2020-2021学年高三上学期第一学段质量检测化学试题上海市七宝中学2021届高三上学期期中考试化学试题山东省济南大学城实验高级中学2021届高三4月阶段性测试化学试题(已下线)课时05 电解质与离子方程式-2022年高考化学一轮复习小题多维练(全国通用)(已下线)考点04 离子反应-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点04 离子反应-备战2022年高考化学一轮复习考点帮(浙江专用)福建省宁化第一中学2021-2022学年高三上学期第一次阶段考试化学试题(已下线)第十单元 化学实验基础(B卷 真题滚动练)-2022年高考化学一轮复习单元滚动双测卷(新高考地区专用)黑龙江省哈尔滨市第三中学2021-2022学年上学期高三第三次验收考试化学试题(已下线)卷03 离子方程式正误判断-【小题小卷】冲刺2022年高考化学小题限时集训(新高考专用)上海市普陀区2022届高三适应性练习(二模)化学试题(已下线)考点04 离子反应-备战2023年高考化学一轮复习考点帮(全国通用)广东省广州市省实、执信、广雅、六中四校2022-2023学年高三8月联考化学试题陕西省安康中学2023届高三第一次检测性考试化学试题湖南省祁东县育贤中学2022-2023学年高三上学期第一次月考化学试题河南省濮阳市南乐县第一高级中学2022-2023学年高三上学期7月月考化学试题广东省深圳市红岭中学2022-2023学年高三上学期期中考试化学试题(已下线)第2讲 离子反应 离子方程式北京市大兴区2022-2023学年高二下学期期末考试化学试题福建省厦门第一中学海沧校区2023-2024学年高三上学期9月月考化学试题福建省漳州市华安县第一中学2023-2024学年高三上学期10月月考化学试题黑龙江省哈尔滨市第六中学2018-2019学年高二下学期期末考试化学试题甘肃省甘谷第一中学2018-2019学年高二下学期期末考试化学试题广东省梅州市梅州中学2019-2020学年高二下学期4月月考化学试题山西省运城市芮城县2019-2020学年高二下学期期末调研测试化学试题黑龙江省大庆实验中学2019-2020学年高二下学期期末考试化学试题浙江省金华十校2019-2020学年高二下学期期末调研考试化学试题吉林省白城市第一中学2019-2020学年高二下学期期末考试化学试题江西省永丰县永丰中学2020-2021学年高二上学期期中考试化学试题江苏省苏州陆慕高级中学2020-2021学年高二上学期期中考试化学试题安徽省安庆市第十中学2020-2021学年高二5月月考化学试题江苏省淮安市2021-2022学年高二上学期期末调研测试化学试题宁夏银川市第二中学2021-2022学年高二上学期期末考试化学试题浙江金华第一中学2021-2022学年高二下学期期中考试化学试题浙江省强基联盟2021-2022学年高一下学期5月份联考化学试题 江西省南昌市知行中学2022-2023学年高二上学期11月份作业练习(月考)化学试题
名校
8 . 下列污水处理的方法中,表示其原理的离子方程式不正确 的是
A.混凝法,用明矾做混凝剂:Al3++3H2O Al(OH)3+3H+ Al(OH)3+3H+ |
B.中和法,用过量CO2中和碱性废水:CO2+2OH-=CO +H2O +H2O |
| C.沉淀法,用Na2S处理含Hg2+废水:Hg2++S2-=HgS↓ |
D.氧化还原法,用FeSO4将酸性废水中Cr2O72-还原为Cr3+:Cr2O +6Fe2++14H+=2Cr3++6Fe3++7H2O +6Fe2++14H+=2Cr3++6Fe3++7H2O |
您最近一年使用:0次
2017-01-18更新
|
856次组卷
|
10卷引用:2017届北京市海淀区高三上学期期末化学试卷
2017届北京市海淀区高三上学期期末化学试卷北京市昌平临川育人学校2018届高三上学期期末考试化学试题北京市第五中学2021届高三上学期第二次阶段性考试化学试题北京市中央民族大学附属中学2022届高三9月月考化学试题北京师范大学附属实验中学2023届高三下学期三模化学试题(已下线)20231218+12月月考1737051759696343040北京师范大学实验中学2023-2024学年高三上学期12月月考化学试卷【校级联考】辽宁省重点六校协作体2019届高三上学期期中考试化学试题广东省华南师范大学附属中学2023-2024学年高三上学期第一次月考化学试题陕西省西安工业大学附属中学2023-2024学年高三下学期第七次适应性考试理综试题-高中化学
名校
9 . 下列离子方程式书写正确的是( )
| A.用漂白液将污水中的NH3氧化成N2:ClO-+2NH3=N2+Cl-+3H2O |
| B.向NH4HCO3稀溶液中滴加过量Ca(OH)2溶液:NH4++HCO3-+2OH-=NH3·H2O+CO32-+H2O |
| C.酸性条件下,用H2O2将I-转化为I2:H2O2+2I-=I2+2OH- |
| D.用少量的氨水吸收硫酸工业尾气中的SO2:SO2+NH3·H2O=NH4++HSO3- |
您最近一年使用:0次