1 . 向200mL1.5mol∙L-lFeBr2溶液中逐渐通入Cl2,其中n(Fe2+)、n(Br-)随通入Cl2的物质的量n(Cl2)变化如图所示,下列说法错误的是
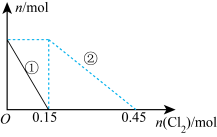

| A.①代表Fe2+,②代表Br- |
| B.还原性强弱:Br->Fe2+ |
| C.n(Cl2)=0.35mol时,溶液中c(Fe3+)=c(Br-) |
| D.n(Cl2)=0.45mol时,总的离子方程式为:2Fe2++4Br-+3Cl2=2Fe3++2Br2+6Cl- |
您最近一年使用:0次
2022-12-13更新
|
122次组卷
|
3卷引用:山东省烟台市莱州市第一中学2023-2024学年高一下学期开学化学试题
名校
2 . 学习小组进行如下实验:
下列说法错误的是
| 序号 | 实验操作 | 实验现象 |
| Ⅰ | 将1mLpH=1的0.1mol·L-1 FeSO4溶液和2滴0.1mol·L-1KSCN溶液混合,接着向混合溶液中逐滴滴加0.5mL0.3mol·L-1的H2O2溶液 | 滴入H2O2溶液,溶液立即变红,继续滴加,溶液红色变浅并逐渐褪去 |
| Ⅱ | 向i的混合溶液中滴入KSCN溶液 | 溶液变红 |
| Ⅲ | 向1mL0.3mol·L-1的H2O2溶液中滴加2滴0.1mol·L-1KSCN溶液,继续加入0.5mLpH=1的H2SO4溶液,静置2min | 无明显现象 |
| Ⅳ | 向ⅲ的混合溶液中滴入2滴Fe2(SO4)3溶液 | 滴入Fe2(SO4)3溶液,溶液立即变红,静置2min,溶液红色变浅并逐渐褪去 |
| A.实验中溶液变红的原因是生成Fe(SCN)3 |
| B.实验i~ⅱ说明实验i中SCN-被H2O2全部氧化 |
| C.实验ⅲ~ⅳ说明酸性溶液中H2O2氧化KSCN的速度慢 |
| D.实验i~ⅳ说明Fe2+能加速H2O2氧化KSCN的反应 |
您最近一年使用:0次
2022-02-25更新
|
773次组卷
|
8卷引用:山东省烟台第二中学2021-2022学年高三下学期开年摸底联考化学试题
山东省烟台第二中学2021-2022学年高三下学期开年摸底联考化学试题湖南省百师联盟2021-2022学年高三下学期开年摸底联考化学试题山西省吕梁市2021-2022学年高三下学期开学考试理综化学试题(已下线)第15讲 铁盐和亚铁盐(讲义)-【帮课堂】2022-2023学年高一化学同步精品讲义(人教2019必修第一册 )湖南省张家界市2023届高三下学期模拟考试化学试题辽宁省名校联盟2023年高三下学期3月高考适应性测试化学试题黑龙江省双鸭山市第一中学2023-2024学年高三上学期10月月考化学试题湖北省部分县市区省级示范高中温德克英协作体2023-2024学年高二上学期期末综合性调研考试化学试题
名校
解题方法
3 . 为了防止钢铁零件生锈,常采用化学处理使钢铁零件表面生成 的致密保护层——“发蓝”。化学处理过程中其中一步的反应为:
的致密保护层——“发蓝”。化学处理过程中其中一步的反应为: ,下列叙述不正确的是
,下列叙述不正确的是
 的致密保护层——“发蓝”。化学处理过程中其中一步的反应为:
的致密保护层——“发蓝”。化学处理过程中其中一步的反应为: ,下列叙述不正确的是
,下列叙述不正确的是| A.钢铁零件“发蓝”实质上是使铁表面钝化 |
| B.上述反应中,铁被氧化 |
C. 的氧化性大于 的氧化性大于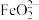 的氧化性 的氧化性 |
D.反应中转移 电子,生成还原产物 电子,生成还原产物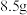 |
您最近一年使用:0次
2021-01-27更新
|
928次组卷
|
18卷引用:山东省烟台市莱州市第一中学2023-2024学年高一下学期开学化学试题
山东省烟台市莱州市第一中学2023-2024学年高一下学期开学化学试题甘肃省民勤县第四中学2020-2021学年高一下学期开学考试化学试题山东省济南市历城区第二中学2021-2022学年高一下学期开学考试化学试题湖南省岳阳市 岳阳县第一中学2023-2024学年高一下学期开学化学试题鲁科版必修一2019—2020学年第三章检测试题天津市静海区第一中学2019-2020学年高一上学期12月学业能力调研化学试题2019-2020学年高一上学期期末复习《新题速递·化学》12月(考点01-05)辽宁省大连市普兰店区第一中学2019-2020学年高一上学期期末考试化学试题(已下线)第三单元 物质的性质与转化(基础过关)-2020-2021学年高一化学必修第一册单元测试定心卷 (鲁科版2019)山东省菏泽地区2020-2021学年高一上学期期末联考化学试题山东省临朐县实验中学2020-2021学年高一1月阶段性测试化学试题天津市第三中学2020-2021学年高一上学期12月月考化学试题 江西省抚州市金溪县第一中学2020-2021学年高一上学期第二次月考化学试题山西省太原市第五十六中学2020-2021学年高二下学期5月月考化学试题重庆市秀山高级中学校2021-2022学年高三上学期10月月考化学试题山东部分名校2021-2022学年上学期高一12月份质量检测化学试题河南省洛阳市新安县第一高级中学2022-2023学年高一上学期11月考试化学试题江苏省响水中学2022-2023学年高一3月学情分析化学试题
名校
4 . 已知氧化性强弱顺序:Cl2>Br2>Fe3+>I2,则下列说法正确的是
| A.向含碘化钾、淀粉的溶液中滴加FeCl3溶液,溶液变蓝 |
| B.向FeBr2溶液中通入少量Cl2,发生反应的离子方程式为:2Br- + Cl2 = Br2 + 2Cl- |
| C.某溶液中含有Fe2+、Cl-、I-,为了除去I-而不减少其他离子,可通入过量氯气 |
| D.向含有NaBr、NaI的溶液中通入适量氯气,充分作用后,将溶液蒸干、灼烧,可能得到NaCl和NaI的固体混合物 |
您最近一年使用:0次
2017-03-19更新
|
357次组卷
|
3卷引用:2016-2017学年山东省烟台第二中学高一下学期开学考试化学试卷



