名校
1 . 实验室从含碘废液(除H2O外,含有CCl4、I2、I-等)中回收碘,其实验过程如图:
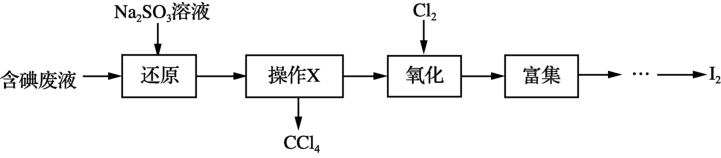
已知KI等离子化合物易溶于水,不溶于有机溶剂(如CCl4)。
(1)操作X的名称为__ ,该操作需要使用的玻璃仪器有___ 。
(2)配平方程式:Na2SO3+I2+H2O=Na2SO4+HI___ 。
(3)氧化的目的是___ 。

已知KI等离子化合物易溶于水,不溶于有机溶剂(如CCl4)。
(1)操作X的名称为
(2)配平方程式:Na2SO3+I2+H2O=Na2SO4+HI
(3)氧化的目的是
您最近一年使用:0次
解题方法
2 . A、B、C、D、E五种短周期元素的原子序数逐渐增大。A是原子半径最小的元素,B可形成多种同素异形体,其中一种的硬度是自然界中最大的。D元素原子的最外层电子数是次外层电子数的3倍。E元素的M层电子数等于A和B的质子数之和。
(1)写出元素D在元素周期表中的位置:________________________ 。
(2)B、C、D三种元素的最简单氢化物的稳定性由强到弱的顺序是________________ (填化学式)。
(3)A、B、C、D几种元素之间可以形成多种10电子微粒,写出上述10电子微粒中离子之间发生反应的一个离子方程式:________________________________ 。
(4)ED2是一种具有强氧化性的新型消毒剂,一定条件下4mol ED2与5 mol C2A4恰好完全反应,请写出反应的化学方程式:_________________________________ ;若反应消耗1 mol C2A4,则转移电子的物质的量为______________ 。
(1)写出元素D在元素周期表中的位置:
(2)B、C、D三种元素的最简单氢化物的稳定性由强到弱的顺序是
(3)A、B、C、D几种元素之间可以形成多种10电子微粒,写出上述10电子微粒中离子之间发生反应的一个离子方程式:
(4)ED2是一种具有强氧化性的新型消毒剂,一定条件下4mol ED2与5 mol C2A4恰好完全反应,请写出反应的化学方程式:
您最近一年使用:0次



