名校
解题方法
1 . (1)水热法制备Fe3O4纳米颗粒的反应是3Fe2++2S2O +O2+4OH-=Fe3O4↓+S4O
+O2+4OH-=Fe3O4↓+S4O +2H2O
+2H2O
①参加反应的氧化剂与还原剂的物质的量之比为______ 。
②若有2molFe2+被氧化,则被Fe2+还原的O2的物质的量为______ mol。
③每生成1molFe3O4,反应转移的电子为______ mol。
(2)往含Fe3+、H+、NO 的混合液中加入少量SO
的混合液中加入少量SO ,反应的离子方程式为
,反应的离子方程式为______ 。
 +O2+4OH-=Fe3O4↓+S4O
+O2+4OH-=Fe3O4↓+S4O +2H2O
+2H2O①参加反应的氧化剂与还原剂的物质的量之比为
②若有2molFe2+被氧化,则被Fe2+还原的O2的物质的量为
③每生成1molFe3O4,反应转移的电子为
(2)往含Fe3+、H+、NO
 的混合液中加入少量SO
的混合液中加入少量SO ,反应的离子方程式为
,反应的离子方程式为
您最近一年使用:0次
名校
解题方法
2 . 双线桥法标出电子转移并填空。
3Cu+8HNO3=3Cu(NO3)2+2NO+4H2O,______ 。被还原的物质为______ ,还原剂为______ 。
3Cu+8HNO3=3Cu(NO3)2+2NO+4H2O,
您最近一年使用:0次
名校
解题方法
3 . 2Al+Fe2O3 2Fe+Al2O3。氧化剂
2Fe+Al2O3。氧化剂___ ;还原剂___ ;氧化产物___ ;还原产物___ 。
 2Fe+Al2O3。氧化剂
2Fe+Al2O3。氧化剂
您最近一年使用:0次
名校
解题方法
4 . 2FeCl3+Fe=3FeCl2的氧化剂为___ ;还原剂为___ ;氧化产物为___ ;还原产物为___ 。
您最近一年使用:0次
名校
解题方法
5 . 已知铜在常温下能被稀硝酸溶解,其反应的化学方程式如下:3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O
(1)上述反应的氧化剂是_____ ,还原剂是____ ,氧化产物是____ ,还原产物是____ 。
(2)用双线桥法分析上述反应的电子转移方向和数目______ 。
(1)上述反应的氧化剂是
(2)用双线桥法分析上述反应的电子转移方向和数目
您最近一年使用:0次
2020-12-10更新
|
124次组卷
|
2卷引用:吉林油田第十一中学2020-2021学年高一上学期期中考试化学试题
6 . 高铁酸钠(Na2FeO4)是一种高效的饮用水处理剂,可由下列方法制得:2Fe(OH)3+3NaClO+4NaOH=2Na2FeO4+3NaCl+5H2O。关于该反应说法正确的是
| A.Fe(OH)3中铁元素化合价为+3,只有氧化性 |
| B.Na2FeO4具有强氧化性,能消毒杀菌 |
| C.反应中NaClO是氧化剂,NaCl是氧化产物 |
| D.生成5 mol H2O,转移了3 mol电子 |
您最近一年使用:0次
7 . 下列叙述正确的是
①阳离子只有氧化性,阴离子只有还原性;
②含最高价元素的化合物,一定具有强氧化性;
③失电子多的还原剂还原性就强;
④有单质生成的化学反应一定是氧化还原反应;
⑤含金属元素的离子不一定都是阳离子;
⑥金属阳离子被还原不一定得到金属单质;
⑦在氧化还原反应中,非金属单质一定是氧化剂。
①阳离子只有氧化性,阴离子只有还原性;
②含最高价元素的化合物,一定具有强氧化性;
③失电子多的还原剂还原性就强;
④有单质生成的化学反应一定是氧化还原反应;
⑤含金属元素的离子不一定都是阳离子;
⑥金属阳离子被还原不一定得到金属单质;
⑦在氧化还原反应中,非金属单质一定是氧化剂。
| A.②③⑤ | B.①②③⑥ | C.④⑤⑦ | D.⑤⑥ |
您最近一年使用:0次
名校
8 . 已知氧化性Br2>Fe3+>I2>S,下列反应不能发生的是( )
| A.2Fe2++I2=2Fe3++2I- | B.Br2+H2S=S+2HBr |
| C.2Fe3++2I-=2Fe2++I2 | D.Br2+2Fe2+=Fe3++2Br- |
您最近一年使用:0次
2020-12-08更新
|
143次组卷
|
9卷引用:吉林省油田高级中学2019-2020学年高一上学期期中考试化学试题
解题方法
9 . 下列变化过程中需要加氧化剂才能实现的是
A.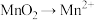 | B. |
C.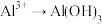 | D.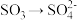 |
您最近一年使用:0次
2020-12-07更新
|
294次组卷
|
2卷引用:吉林省长春市农安县2020-2021学年高一上学期期中考试化学试题
解题方法
10 . 下列化学反应中,水作为还原剂的是
A. | B. |
C. | D.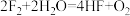 |
您最近一年使用:0次
2020-12-07更新
|
150次组卷
|
3卷引用:吉林省长春市农安县2020-2021学年高一上学期期中考试化学试题



