1 . 砷(33As)在元素周期表中与氮、磷同主族,其在自然界存在的主要化合物有砒霜(As2O3)、雄黄( As4S4)、雌黄(As2S3)等。
(1)砷在元素周期表中的位置为________ 。
(2)在一定条件下,雄黄(As4S4(雄黄中As元素化合价为+2)和雌黄As2S3之间的转化关系如图所示。
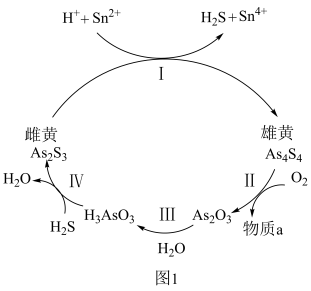
①H3AsO3中砷元素呈_______ 价;则在转化关系I中,被还原的元素名称是____________ 。
②反应Ⅱ中,若1mol As4S4参加反应时,转移12mole-,则物质a为______ (填化学式);将As2O3(俗称砒霜)在高温下用焦炭还原可制备砷,同时产生一种无毒气体,写出用焦炭还原As2O3时的化学方程式:_________ 。
③在转化关系Ⅲ中,将As2O3溶于热水生成亚砷酸(H3AsO3),已知H3AsO3是两性偏酸性的化合物,Na3AsO3溶液呈碱性,原因是_________ (用水解离子方程式表示)。
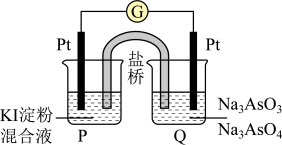
(3)某原电池装置如图,电池总反应为AsO +2I-+H2O
+2I-+H2O AsO
AsO +I2+2OH-。当P池中溶液由无色变成蓝色时,正极上的电极反应式为
+I2+2OH-。当P池中溶液由无色变成蓝色时,正极上的电极反应式为___________ 。
(1)砷在元素周期表中的位置为
(2)在一定条件下,雄黄(As4S4(雄黄中As元素化合价为+2)和雌黄As2S3之间的转化关系如图所示。

①H3AsO3中砷元素呈
②反应Ⅱ中,若1mol As4S4参加反应时,转移12mole-,则物质a为
③在转化关系Ⅲ中,将As2O3溶于热水生成亚砷酸(H3AsO3),已知H3AsO3是两性偏酸性的化合物,Na3AsO3溶液呈碱性,原因是
(3)某原电池装置如图,电池总反应为AsO
 +2I-+H2O
+2I-+H2O AsO
AsO +I2+2OH-。当P池中溶液由无色变成蓝色时,正极上的电极反应式为
+I2+2OH-。当P池中溶液由无色变成蓝色时,正极上的电极反应式为
您最近一年使用:0次
11-12高三上·黑龙江哈尔滨·期中
解题方法
2 . A-H及X均为中学化学常见物质, X是一种金属单质,A、B是非金属单质且A在常温下为气体。它们在一定条件下有如下转化关系(图中条件均已略去)。
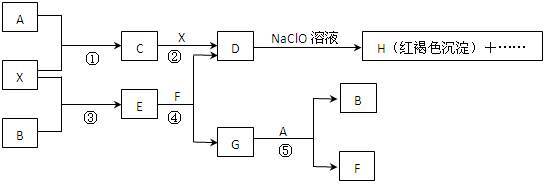
试回答下列问题:
(1)写出C物质的化学式___________ ;
(2)在上述①-⑤反应中肯定不属于氧化还原反应的是___________ (填编号);
(3)指出元素X在元素周期表中的位置:___________ ;
(4)请写出反应④和⑤的离子方程式:④___________ ,⑤___________ ;
(5)用离子方程式表示在D溶液中加入NaClO溶液产生红褐色沉淀的原因:___________ 。

试回答下列问题:
(1)写出C物质的化学式
(2)在上述①-⑤反应中肯定不属于氧化还原反应的是
(3)指出元素X在元素周期表中的位置:
(4)请写出反应④和⑤的离子方程式:④
(5)用离子方程式表示在D溶液中加入NaClO溶液产生红褐色沉淀的原因:
您最近一年使用:0次



