解题方法
1 . (1)加入双氧水能提高软锰矿(主要成分是MnO2)的浸出率,锰转化成Mn2+。写出酸性条件下双氧水提高软锰矿浸出率的离子方程式:_________ 。
(2)碘与氢氧化钠反应的生成物中含有IO3-,写出反应过程的离子方程式:___ 。
(3) 电镀污泥中的Cr2O3与加入的Na2CO3在空气中焙烧,Cr2O3被氧化为Na2CrO4,还有CO2逸出,写出该反应的化学方程式:_____________ 。
(4)某科研小组在实验室用较浓的KOH溶液直接吸收氯气,研究发现反应进行一段时间后开始出现KClO3并逐渐增多,产生KClO3的离子方程式是_______ 。
(5) 用氧缺位铁酸铜(CuFe2O4-x)作催化剂,利用太阳能热化学循环分解H2O也可制H2,其物质转化如图1所示。
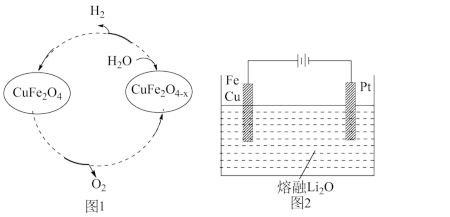
①氧缺位铁酸铜(CuFe2O4-x)与水反应的化学方程式为_________ 。
②CuFe2O4可用电化学方法得到,其原理如图2所示,则阳极的电极反应式为_________ 。
(2)碘与氢氧化钠反应的生成物中含有IO3-,写出反应过程的离子方程式:
(3) 电镀污泥中的Cr2O3与加入的Na2CO3在空气中焙烧,Cr2O3被氧化为Na2CrO4,还有CO2逸出,写出该反应的化学方程式:
(4)某科研小组在实验室用较浓的KOH溶液直接吸收氯气,研究发现反应进行一段时间后开始出现KClO3并逐渐增多,产生KClO3的离子方程式是
(5) 用氧缺位铁酸铜(CuFe2O4-x)作催化剂,利用太阳能热化学循环分解H2O也可制H2,其物质转化如图1所示。

①氧缺位铁酸铜(CuFe2O4-x)与水反应的化学方程式为
②CuFe2O4可用电化学方法得到,其原理如图2所示,则阳极的电极反应式为
您最近一年使用:0次
名校
解题方法
2 . 按要求回答下列问题:
(1)加入双氧水能提高软锰矿(主要成分是MnO2)的浸出率,锰转化成Mn2+。写出酸性条件下双氧水提高软锰矿浸出率的离子方程式:_______ 。
(2)电镀污泥中的Cr2O3与加入的Na2CO3在空气中焙烧,Cr2O3被氧化为Na2CrO4,还有CO2逸出,写出该反应的化学方程式:_______ 。
(3)某科研小组在实验室用较浓的KOH溶液直接吸收氯气,研究发现反应进行一段时间后开始出现KClO3并逐渐增多,产生KClO3的离子方程式是:_______ 。
(4)用氧缺位铁酸铜(CuFe2O4-x)作催化剂,利用太阳能热化学循环分解H2O也可制H2,其物质转化如图1所示。

①氧缺位铁酸铜(CuFe2O4-x)与水反应的化学方程式为:_______ 。
②CuFe2O4可用电化学方法得到,其原理如图2所示,则阳极的电极反应式为:_______ 。
(1)加入双氧水能提高软锰矿(主要成分是MnO2)的浸出率,锰转化成Mn2+。写出酸性条件下双氧水提高软锰矿浸出率的离子方程式:
(2)电镀污泥中的Cr2O3与加入的Na2CO3在空气中焙烧,Cr2O3被氧化为Na2CrO4,还有CO2逸出,写出该反应的化学方程式:
(3)某科研小组在实验室用较浓的KOH溶液直接吸收氯气,研究发现反应进行一段时间后开始出现KClO3并逐渐增多,产生KClO3的离子方程式是:
(4)用氧缺位铁酸铜(CuFe2O4-x)作催化剂,利用太阳能热化学循环分解H2O也可制H2,其物质转化如图1所示。

①氧缺位铁酸铜(CuFe2O4-x)与水反应的化学方程式为:
②CuFe2O4可用电化学方法得到,其原理如图2所示,则阳极的电极反应式为:
您最近一年使用:0次
名校
3 . 氯及其化合物对人类生产及生活有重要作用。
(1)氯的原子结构示意图为_______ ;实验室氯气的尾气处理常用NaOH溶液,请用离子方程式表示该反应:________ ;工业上将氯气通入冷的消石灰制取漂白粉,漂白粉的有效成分是___ (填化学式)。
(2)NaClO2的漂白能力是漂白粉的4到5倍。NaClO2广泛用于造纸工业、污水处理等。工业上生产NaClO2的工艺流程如下:

①发生器中用NaClO3与Na2SO3在酸性环境下反应制备ClO2,则氧化剂与还原剂的物质的量之比为:_____________ 。
②吸收器中生成NaClO2反应的离子方程式为_______ ,吸收器中的反应温度不能过高,可能的原因为__________ 。
③Cl2和ClO2均能将工业废水中得CN-氧化成无毒的物质,而自身被还原为Cl-,则处理相同量的CN-所需Cl2的质量是ClO2的多少倍。______ (计算结果保留一位小数)。
(1)氯的原子结构示意图为
(2)NaClO2的漂白能力是漂白粉的4到5倍。NaClO2广泛用于造纸工业、污水处理等。工业上生产NaClO2的工艺流程如下:

①发生器中用NaClO3与Na2SO3在酸性环境下反应制备ClO2,则氧化剂与还原剂的物质的量之比为:
②吸收器中生成NaClO2反应的离子方程式为
③Cl2和ClO2均能将工业废水中得CN-氧化成无毒的物质,而自身被还原为Cl-,则处理相同量的CN-所需Cl2的质量是ClO2的多少倍。
您最近一年使用:0次
名校
解题方法
4 . A、B、C是中学化学中常见的三种短周期元素。已知:
①A元素的价电子排布式为nsnnpn;②B元素最高正价与最低负价的代数和为2;③C元素有多种化合价,且常温下C元素的单质与石灰水反应,可得到两种含C元素的化合物;④B、C两种元素质子数之和是A元素质子数的4倍。
(1)写出常温下C的单质和澄清石灰水反应的离子方程式________________________ ;
(2)比较B、C元素的最高价氧化物对应的水化物酸性的强弱______________ >_____________ ;
(3)已知砷(As)元素原子的最外层电子排布是 4s24p3。砷元素的最高价氧化物的化学式是________ ,砷酸钠的化学式是________ 。砷酸钠在酸性条件下能把碘化钾氧化为单质碘,同时生成亚砷酸钠(Na3AsO3)和水,该反应的离子方程式为____________________________
①A元素的价电子排布式为nsnnpn;②B元素最高正价与最低负价的代数和为2;③C元素有多种化合价,且常温下C元素的单质与石灰水反应,可得到两种含C元素的化合物;④B、C两种元素质子数之和是A元素质子数的4倍。
(1)写出常温下C的单质和澄清石灰水反应的离子方程式
(2)比较B、C元素的最高价氧化物对应的水化物酸性的强弱
(3)已知砷(As)元素原子的最外层电子排布是 4s24p3。砷元素的最高价氧化物的化学式是
您最近一年使用:0次
名校
解题方法
5 . 实验操作能达到目的的是
| 选项 | 目的 | 实验操作 |
| A | 证明氯水具有酸性和氧化性 | 向石蕊试液中滴加氯水,试液先变红后褪色 |
| B | 证明氯气可以支持燃烧 | 氢气点燃后在氯气中安静燃烧,发出苍白色火焰,有白烟生成 |
| C | 测定84消毒液的 | 用洁净的玻璃棒蘸取少许84消毒液滴在 试纸上 试纸上 |
| D | 验证某补铁口服液中是否含有 | 向该口服液中滴加几滴新制氯水,振荡,再加入少量 溶液,观察溶液颜色变化 溶液,观察溶液颜色变化 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次



