名校
1 . a、b、c、d、e为五种短周期主族元素,原子序数依次递增。下图是a~e五种元素的单质及其化合物(或其溶液)的转化关系。已知A为金属单质,B、C、D是非金属单质,且在常温常压下都是气体,D常用于自来水的杀菌、消毒;化合物G的焰色试验呈黄色,化合物F通常状况下呈气态。请回答下列问题
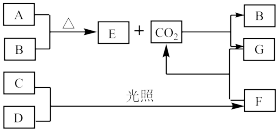
(1)d在元素周期表中的位置位于___________ ,CO2的电子式为___________ 。
(2)e的单质与d的最高价氧化物对应的水化物反应的化学方程式是___________ 。
(3)Na2O2可在呼吸面具中作为氧气来源,假设每人每分钟消耗0.448LO2(标准状况),且所需的O2全部由Na2O2来提供,则某消防员工作1小时所需Na2O2的质量为___________ g
(4)b、c、d元素中,原子半径由小到大的顺序是___________ (填元素符号);c、d、e元素分别形成的简单离子中离子半径最小的是___________ (填离子符号)。
(5)b和e两元素相比较,非金属性较强是___________ (填元素符号),可以证明该结论的是___________ 。
A.e的气态氢化物比b的气态氢化物稳定
B.b氧化物对应的水化物的酸性弱于e氧化物对应的水化物的酸性
C.b的简单氢化物的沸点比e的氢化物沸点低
D.b和e形成的化合物中的化合价b为正价,e为负价

(1)d在元素周期表中的位置位于
(2)e的单质与d的最高价氧化物对应的水化物反应的化学方程式是
(3)Na2O2可在呼吸面具中作为氧气来源,假设每人每分钟消耗0.448LO2(标准状况),且所需的O2全部由Na2O2来提供,则某消防员工作1小时所需Na2O2的质量为
(4)b、c、d元素中,原子半径由小到大的顺序是
(5)b和e两元素相比较,非金属性较强是
A.e的气态氢化物比b的气态氢化物稳定
B.b氧化物对应的水化物的酸性弱于e氧化物对应的水化物的酸性
C.b的简单氢化物的沸点比e的氢化物沸点低
D.b和e形成的化合物中的化合价b为正价,e为负价
您最近一年使用:0次
2022-03-08更新
|
227次组卷
|
2卷引用:湖北省新高考联考协作体2021-2022学年高一下学期3月考试化学试题
2 . 下图表示由元素周期表中1到20号且不同主族的元素组成的单质及化合物之间的转化关系(产物中的水已略去)。其中A为黄绿色气体单质,D有漂白性;在实验室中常用固体B和固体C加热制取刺激性气味F;F和G的组成元素相同,G与H分子所含电子数相同。

请回答
(1)单质A的组成元素在周期表中的位置是________ ;
(2)B的化学式为________ ,F的电子式为________ ,C中所含化学键类型有_______ ;
(3)写出反应②的化学方程式_____________ ;
(4)反应④中F和气体H在空气中相遇时的实验现象为__________ 写出的F一种具体用途_______________ ;
(5)向具有漂白作用的D溶液中加入H的浓溶液有A生成,其反应的离子方程式为______________ 。
(6)砷元素(As)与上述某元素处于同一主族。砷酸铅可用作杀虫剂。已知:
①在砷酸铅中,砷处于最高价态,铅处于稳定价态。
②砷酸铅是正砷酸对应的盐,1mol正砷酸分子中含有8mol原子.
砷的最高价氧化物的化学式为___________ 砷酸铅的化学式为________

请回答
(1)单质A的组成元素在周期表中的位置是
(2)B的化学式为
(3)写出反应②的化学方程式
(4)反应④中F和气体H在空气中相遇时的实验现象为
(5)向具有漂白作用的D溶液中加入H的浓溶液有A生成,其反应的离子方程式为
(6)砷元素(As)与上述某元素处于同一主族。砷酸铅可用作杀虫剂。已知:
①在砷酸铅中,砷处于最高价态,铅处于稳定价态。
②砷酸铅是正砷酸对应的盐,1mol正砷酸分子中含有8mol原子.
砷的最高价氧化物的化学式为
您最近一年使用:0次
3 . Ⅰ.A、B、C、D、E、X是中学常见的无机物,存在下图所示转化关系(部分生成物和反应条件略去),已知A由短周期非金属元素组成,B具有漂白性且光照易分解。

(1)若A为单质,且常温下0.1mol•L-1C溶液的pH为1,请回答以下问题:
①组成单质A的元素在元素周期表中的位置为______________________ ;
②A与H2O反应的离子反应方程式为______________________ ;
③X可能为________ (填代号)。a.NaOH b.AlCl3 c.Na2CO3 d.NaAlO2
(2)若A为两种元素形成的化合物,且E与水反应生成G的浓溶液遇C有白烟产生则:
①A的电子式为______________________ ;
②A与H2O反应的化学反应方程式为______________________ ;
Ⅱ.某化合物A是一种易溶于水的不含结晶水盐,溶于水后完全电离出三种中学化学常见离子,其中有两种是10电子的阳离子。用A进行如下实验:取2.370gA溶于蒸馏水配成溶液;向该溶液中逐滴加入一定量的氢氧化钠溶液,过程中先观察到产生白色沉淀B,后产生能使湿润红色石蕊试纸变蓝的气体 C,气体不再产生时沉淀开始溶解,当沉淀恰好完全溶解时共用去氢氧化钠的物质的量为0.050mol.回答下列问题:
(3)请画出沉淀B中金属元素的原子结构示意图______________________ ;
(4)请写出沉淀B溶解在氢氧化钠溶液中的离子方程式______________________ ;
(5)请写出气体C与氯气发生氧化还原反应的化学方程式______________________ 。

(1)若A为单质,且常温下0.1mol•L-1C溶液的pH为1,请回答以下问题:
①组成单质A的元素在元素周期表中的位置为
②A与H2O反应的离子反应方程式为
③X可能为
(2)若A为两种元素形成的化合物,且E与水反应生成G的浓溶液遇C有白烟产生则:
①A的电子式为
②A与H2O反应的化学反应方程式为
Ⅱ.某化合物A是一种易溶于水的不含结晶水盐,溶于水后完全电离出三种中学化学常见离子,其中有两种是10电子的阳离子。用A进行如下实验:取2.370gA溶于蒸馏水配成溶液;向该溶液中逐滴加入一定量的氢氧化钠溶液,过程中先观察到产生白色沉淀B,后产生能使湿润红色石蕊试纸变蓝的气体 C,气体不再产生时沉淀开始溶解,当沉淀恰好完全溶解时共用去氢氧化钠的物质的量为0.050mol.回答下列问题:
(3)请画出沉淀B中金属元素的原子结构示意图
(4)请写出沉淀B溶解在氢氧化钠溶液中的离子方程式
(5)请写出气体C与氯气发生氧化还原反应的化学方程式
您最近一年使用:0次
名校
解题方法
4 . 下列框图所示的物质转化关系中,甲是日常生活中常见的金属,乙、丙、丁是常见的气体单质。气体B与气体C相遇产生大量的白烟,D是日常生活中常见的盐(部分反应物和生成物及溶剂水已略去)。

请回答下列问题:
(1)甲元素在周期表中的位置_______ 。
(2)A的电子式为_______ ;B的电子式为_______ 。
(3)写出A溶液和甲反应生成丙的化学方程式_______ 。
(4)如何检验E溶液中阳离子?_______ 。
(5)B的实验室制法化学方程式_______ 。

请回答下列问题:
(1)甲元素在周期表中的位置
(2)A的电子式为
(3)写出A溶液和甲反应生成丙的化学方程式
(4)如何检验E溶液中阳离子?
(5)B的实验室制法化学方程式
您最近一年使用:0次
名校
5 . 常温下,A是可用来对自来水进行消毒的黄绿色单质气体,A、B、C、D、E都含X元素,其转化关系如下图所示,部分产物已略去。
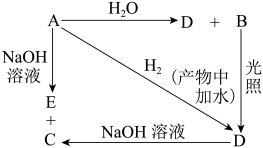
(1)请分别写出A、B、C、E的化学式(如为溶液请写出溶质的化学式):
A___________ 、B___________ 、C___________ 、E___________ 。
(2)A常用于合成漂白粉,漂白粉的有效成分的化学式为:_______________ ;写出工业生产合成漂白粉的化学方程式:____________ 。
(3)漂白粉长期露置在空气中会变质,写出漂白粉变质过程中涉及的化学方程式:____________ 、____________ 。

(1)请分别写出A、B、C、E的化学式(如为溶液请写出溶质的化学式):
A
(2)A常用于合成漂白粉,漂白粉的有效成分的化学式为:
(3)漂白粉长期露置在空气中会变质,写出漂白粉变质过程中涉及的化学方程式:
您最近一年使用:0次
名校
解题方法
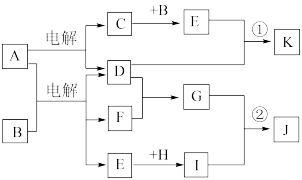
6 . 已知物质A~K之间有如下图所示转化关系。其中A是一种易溶于水的离子化合物,在空气中易潮解和变质,在水中可以电离出电子总数相等的两种离子;E为生活中常用消毒剂的有效成分,F是生活中不可缺少的调味剂,G为无色液体,B、C、D、K都是单质;反应②~⑤都是重要的工业反应。(部分反应需要在溶液中进行)
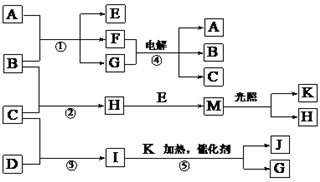
(1)物质D中所含元素在周期表中的位置为____________________________ ,
E中所含化学键类型有___________________________________________ ,
M的结构式为___________________________________________________ 。
(2)反应④的离子方程式为___________________________________________ 。
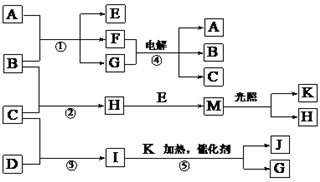
(1)物质D中所含元素在周期表中的位置为
E中所含化学键类型有
M的结构式为
(2)反应④的离子方程式为
您最近一年使用:0次
2017-10-16更新
|
198次组卷
|
2卷引用:河北省“名校联盟”(五校联考)2018届高三上学期教学质量监测(一)化学试题
名校
解题方法
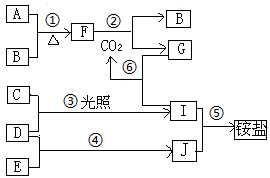
7 . 下图是部分短周期元素的单质及化合物(或溶液)的转化关系:
已知B、C、D、E是非金属单质,且在常温下都是气体;化合物G的焰色反应为黄色,化合物I、J通常状况下呈气态;反应④是化工生产中的一种重要固氮反应。请回答下列问题:
(1)写出A、B元素在周期表中的位置:A__________________ B__________________
(2)①~⑥反应中属于氧化还原反应的是___________________________________ (填序号)
(3)写出②的化学方程式:_____________________________
⑥的离子方程式:______________________________________
(4)反应⑤的现象是________ ,J的另一种检验方法及现象是_______________ 。
已知B、C、D、E是非金属单质,且在常温下都是气体;化合物G的焰色反应为黄色,化合物I、J通常状况下呈气态;反应④是化工生产中的一种重要固氮反应。请回答下列问题:
(1)写出A、B元素在周期表中的位置:A
(2)①~⑥反应中属于氧化还原反应的是
(3)写出②的化学方程式:
⑥的离子方程式:
(4)反应⑤的现象是
您最近一年使用:0次
2017-04-12更新
|
317次组卷
|
2卷引用:2016-2017学年黑龙江省大庆第一中学高一下学期第二次月考化学试卷
解题方法
8 . 在下图所示的物质转化关系中,A是海水中含量最丰富的盐,B是常见的无色液体,F在D中燃烧发出苍白色火焰。H可用于制造光导纤维,J是一种乳白色凝胶状沉淀。(部分生成物和部分反应条件未列出) 请回答下列问题:
(1)形成单质D的元素在周期表中的位置
(2)形成C、D、F单质的元素半径由大到小的顺序(填写元素符号)
(3)C长期暴露在空气中,最终产物是
(4)H在高温下与碳反应方程式为 ,若转移4mol电子参加反应的碳为 mol。
(5)写出反应①的离子方程式
(6)写出反应②的化学方程式

(1)形成单质D的元素在周期表中的位置
(2)形成C、D、F单质的元素半径由大到小的顺序(填写元素符号)
(3)C长期暴露在空气中,最终产物是
(4)H在高温下与碳反应方程式为 ,若转移4mol电子参加反应的碳为 mol。
(5)写出反应①的离子方程式
(6)写出反应②的化学方程式
您最近一年使用:0次



