1 . 碱式碳酸镁[MgCO3 Mg(OH)2]是一种重要的无机化工产品,在现代社会中具有广泛的应用。白云石[主要成分为CaMg(CO3)2]碳化法制备碱式碳酸镁的流程如图所示:
Mg(OH)2]是一种重要的无机化工产品,在现代社会中具有广泛的应用。白云石[主要成分为CaMg(CO3)2]碳化法制备碱式碳酸镁的流程如图所示:
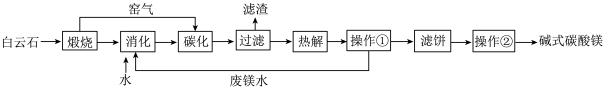
已知:①“碳化”时发生的反应为Mg(OH)2+Ca(OH)2+3CO2=Mg(HCO3)2+CaCO3↓+H2O;
②滤饼的主要成分为MgCO3 Mg(OH)2,还含有少量Mg(HCO3)2。
Mg(OH)2,还含有少量Mg(HCO3)2。
回答下列问题:
(1)“煅烧”时发生反应的化学方程式为___________ ,为了加快“煅烧”速率,可以采取的措施有___________ (写出一种)。
(2)“消化”过程需要加水、搅拌并保持60℃消化1 h,得到精灰乳,若往精灰乳中通入氯气,其中Ca(OH)2悬浊液与氯气发生反应的化学方程式为___________ 。
(3)操作①为___________ ,操作②包含___________ 、___________ ;碱式碳酸镁属于___________ (填标号)。
a.混合物 b.碱 c.盐 d.氧化物
(4)采用上述流程制得的碱式碳酸镁常含一定量结晶水,化学式为MgCO3·Mg(OH)2·xH2O。称取10.0 g样品,进行热重分析,并绘制出如图所示热重曲线示意图。则T℃时所得固体的化学式为___________ ,计算x=___________ 。

 Mg(OH)2]是一种重要的无机化工产品,在现代社会中具有广泛的应用。白云石[主要成分为CaMg(CO3)2]碳化法制备碱式碳酸镁的流程如图所示:
Mg(OH)2]是一种重要的无机化工产品,在现代社会中具有广泛的应用。白云石[主要成分为CaMg(CO3)2]碳化法制备碱式碳酸镁的流程如图所示:
已知:①“碳化”时发生的反应为Mg(OH)2+Ca(OH)2+3CO2=Mg(HCO3)2+CaCO3↓+H2O;
②滤饼的主要成分为MgCO3
 Mg(OH)2,还含有少量Mg(HCO3)2。
Mg(OH)2,还含有少量Mg(HCO3)2。回答下列问题:
(1)“煅烧”时发生反应的化学方程式为
(2)“消化”过程需要加水、搅拌并保持60℃消化1 h,得到精灰乳,若往精灰乳中通入氯气,其中Ca(OH)2悬浊液与氯气发生反应的化学方程式为
(3)操作①为
a.混合物 b.碱 c.盐 d.氧化物
(4)采用上述流程制得的碱式碳酸镁常含一定量结晶水,化学式为MgCO3·Mg(OH)2·xH2O。称取10.0 g样品,进行热重分析,并绘制出如图所示热重曲线示意图。则T℃时所得固体的化学式为

您最近一年使用:0次
2 . 工业上用电解饱和食盐水的方法生产氯气和烧碱.
(1)食盐溶于水发生电离,其电离方程式为__________ 。
(2)2004年4月15日,某化工厂发生氯气泄漏事件,工作人员喷射NaOH溶液形成液幕,包围并吸收泄漏的氯气,其反应原理为____________ (用离子方程式表示)。
(3)事件过后,附近居民向记者反映当时晾在外面的衣服褪色了,其原因是_________ (结合化学方程式解释)。
(1)食盐溶于水发生电离,其电离方程式为
(2)2004年4月15日,某化工厂发生氯气泄漏事件,工作人员喷射NaOH溶液形成液幕,包围并吸收泄漏的氯气,其反应原理为
(3)事件过后,附近居民向记者反映当时晾在外面的衣服褪色了,其原因是
您最近一年使用:0次
2016-12-09更新
|
99次组卷
|
3卷引用:2015-2016学年河北省保定市望都中学高一上学期期末化学试卷



