23-24高三上·河北衡水·期末
名校
解题方法
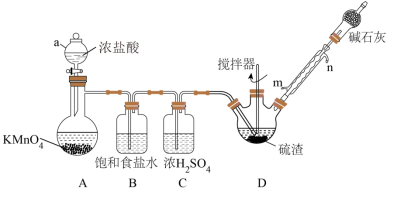
1 . 某实验小组利用硫渣(主要成分为Sn,含少量Cu2S、Pb、As等)与氯气反应制备四氯化锡,其过程如图所示(夹持、加热及控温装置略)。已知:SnCl4遇水极易水解。
相关产物的熔沸点:
(1)仪器a的名称___________ 。
(2)冷凝管的进水口为___________ (填“m”或“n”),碱石灰的作用为___________ 。
(3)如果缺少B装置,可能造成的影响为___________ 。
(4)实验结束后,将三颈烧瓶中得到的物质冷却至室温,___________ (填操作名称),得到粗产品,粗产品再精馏可得到纯净的SnCl4。
(5)用碘量法测量粗产品的纯度:取10.00g粗产品溶于水,加入0.100mol·L-1标准I2溶液20.00mL,并加入少量的淀粉溶液:用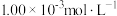 的硫代硫酸钠标准溶液滴定过量的碘。滴定终点时消耗20.00mL硫代硫酸钠标准溶液。测定过程中发生的相关反应:
的硫代硫酸钠标准溶液滴定过量的碘。滴定终点时消耗20.00mL硫代硫酸钠标准溶液。测定过程中发生的相关反应:
①
②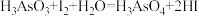
③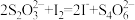
则产品中SnCl4的质量分数___________ (保留三位有效数字)。

相关产物的熔沸点:
| 物质性质 | SnCl4 | SnCl2 | CuCl | PbCl2 | AsCl3 | S |
| 熔点/℃ | -33 | 246 | 426 | 501 | -18 | 112 |
| 沸点/℃ | 114 | 652 | 1490 | 951 | 130 | 444 |
(2)冷凝管的进水口为
(3)如果缺少B装置,可能造成的影响为
(4)实验结束后,将三颈烧瓶中得到的物质冷却至室温,
(5)用碘量法测量粗产品的纯度:取10.00g粗产品溶于水,加入0.100mol·L-1标准I2溶液20.00mL,并加入少量的淀粉溶液:用
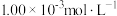 的硫代硫酸钠标准溶液滴定过量的碘。滴定终点时消耗20.00mL硫代硫酸钠标准溶液。测定过程中发生的相关反应:
的硫代硫酸钠标准溶液滴定过量的碘。滴定终点时消耗20.00mL硫代硫酸钠标准溶液。测定过程中发生的相关反应:①

②
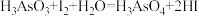
③
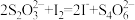
则产品中SnCl4的质量分数
您最近一年使用:0次
23-24高三上·天津和平·期中
名校
2 . 某化学兴趣小组利用如图所示实验装置(夹持及加热装置省略)在实验室制备 并测定其纯度。回答下列问题:
并测定其纯度。回答下列问题:_______ ,与分液漏斗相比,使用滴液漏斗a的优点是_______ 。
(2)装置B中发生反应的离子方程式为_______ 。
(3)若装置B温度控制不当会有 生成,且反应生成的
生成,且反应生成的 、
、 的物质的量均为1mol,则消耗的
的物质的量均为1mol,则消耗的 的物质的量为
的物质的量为_______ mol。
(4)某同学认为该装置设计有缺陷,改进措施为_______ ,否则会使产率偏低。
(5)测定所得 样品的纯度:该小组同学认为可以利用一定质量
样品的纯度:该小组同学认为可以利用一定质量 样品与过量
样品与过量 在酸性条件下发生反应,再以淀粉溶液为指示剂,用
在酸性条件下发生反应,再以淀粉溶液为指示剂,用 标准溶液滴定产生的
标准溶液滴定产生的 测定
测定 样品的纯度。
样品的纯度。
①预设滴定终点时溶液的颜色为_______ 。
②在方案可行性分析时,实验发现在KI溶液和稀硫酸的混合溶液中加入 溶液,最终得到了无色溶液而没有得到预设中的碘溶液,可能的原因是
溶液,最终得到了无色溶液而没有得到预设中的碘溶液,可能的原因是_______ 。
③有同学提出可以使用质量分析法测定 样品的纯度:称量
样品的纯度:称量 样品mg、
样品mg、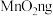 ,混合加热至质量不再改变,剩余固体质量为pg,则样品中
,混合加热至质量不再改变,剩余固体质量为pg,则样品中 的纯度为
的纯度为_______ (用含m、n、p的代数式表达)。
 并测定其纯度。回答下列问题:
并测定其纯度。回答下列问题:
(2)装置B中发生反应的离子方程式为
(3)若装置B温度控制不当会有
 生成,且反应生成的
生成,且反应生成的 、
、 的物质的量均为1mol,则消耗的
的物质的量均为1mol,则消耗的 的物质的量为
的物质的量为(4)某同学认为该装置设计有缺陷,改进措施为
(5)测定所得
 样品的纯度:该小组同学认为可以利用一定质量
样品的纯度:该小组同学认为可以利用一定质量 样品与过量
样品与过量 在酸性条件下发生反应,再以淀粉溶液为指示剂,用
在酸性条件下发生反应,再以淀粉溶液为指示剂,用 标准溶液滴定产生的
标准溶液滴定产生的 测定
测定 样品的纯度。
样品的纯度。①预设滴定终点时溶液的颜色为
②在方案可行性分析时,实验发现在KI溶液和稀硫酸的混合溶液中加入
 溶液,最终得到了无色溶液而没有得到预设中的碘溶液,可能的原因是
溶液,最终得到了无色溶液而没有得到预设中的碘溶液,可能的原因是③有同学提出可以使用质量分析法测定
 样品的纯度:称量
样品的纯度:称量 样品mg、
样品mg、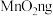 ,混合加热至质量不再改变,剩余固体质量为pg,则样品中
,混合加热至质量不再改变,剩余固体质量为pg,则样品中 的纯度为
的纯度为
您最近一年使用:0次
22-23高三上·辽宁沈阳·期末
名校
解题方法
3 . 下列指定反应的离子方程式正确的是
A.工业制漂白粉: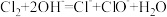 |
B.向 溶液中滴加硝酸: 溶液中滴加硝酸: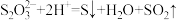 |
C.向苯酚钠溶液中通入少量 : : |
D.向 悬浊液中滴入 悬浊液中滴入 氨水: 氨水: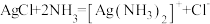 |
您最近一年使用:0次
2023-02-11更新
|
616次组卷
|
3卷引用:河北省石家庄市2023届高中毕业年级教学质量检测(一模)变式题(选择题1-5)
(已下线)河北省石家庄市2023届高中毕业年级教学质量检测(一模)变式题(选择题1-5)辽宁省东北育才学校等五校2022-2023学年高三上学期期末考试化学试题黑龙江省哈尔滨市第六中学2023-2024学年高三上学期期中考试化学试题
22-23高三上·山东潍坊·阶段练习
解题方法
4 . 某小组同学探究不同条件下氯气与二价锰化合物的反应
资料:i. 在一定条件下被
在一定条件下被 或
或 氧化成
氧化成 (棕黑色)、
(棕黑色)、 (绿色)、
(绿色)、 (紫色)。
(紫色)。
ii.浓碱条件下, 可被
可被 还原为
还原为 。
。
iii. 的氧化性与溶液的酸碱性无关,NaClO的氧化性随碱性增强而减弱。
的氧化性与溶液的酸碱性无关,NaClO的氧化性随碱性增强而减弱。
实验装置如图(夹持装置略)
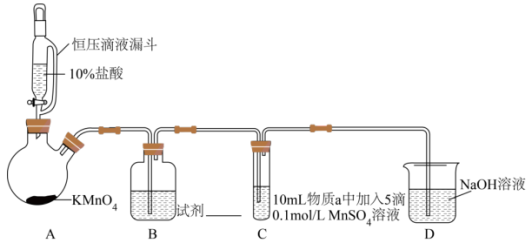
(1)通入 前,II、III中沉淀由白色变为黑色的化学方程式为
前,II、III中沉淀由白色变为黑色的化学方程式为_______ 。
(2)对比实验I、II通入 后的实验现象,对于二价锰化合物还原性的认识是
后的实验现象,对于二价锰化合物还原性的认识是_______ 。
(3)根据资料ⅱ,III中应得到绿色溶液,实验中得到紫色溶液,分析现象与资料不符的原因:
原因一:可能是通入 发生反应
发生反应 ,导致溶液的碱性减弱。但通过实验测定溶液的碱性变化很小。
,导致溶液的碱性减弱。但通过实验测定溶液的碱性变化很小。
原因二:可能是氧化剂过量,氧化剂将 氧化为
氧化为 。
。
①取III中放置后的1mL悬浊液,加入4mL40%NaOH溶液,溶液紫色迅速变为绿色,且绿色缓慢加深。溶液紫色变为绿色的离子方程式为_______ ,溶液绿色缓慢加深,原因是 被
被_______ (填“化学式”)氧化,可证明III的悬浊液中氧化剂过量;
②取II中放置后的1mL悬浊液,加入4mL水,溶液紫色缓慢加深,发生的反应是_______ 。
③从反应速率的角度,分析实验III未得到绿色溶液的可能原因_______ 。
资料:i.
 在一定条件下被
在一定条件下被 或
或 氧化成
氧化成 (棕黑色)、
(棕黑色)、 (绿色)、
(绿色)、 (紫色)。
(紫色)。ii.浓碱条件下,
 可被
可被 还原为
还原为 。
。iii.
 的氧化性与溶液的酸碱性无关,NaClO的氧化性随碱性增强而减弱。
的氧化性与溶液的酸碱性无关,NaClO的氧化性随碱性增强而减弱。实验装置如图(夹持装置略)

| 序号 | 物质a | C中实验现象 | |
通入 前 前 | 通入 后 后 | ||
| I | 水 | 得到无色溶液 | 产生棕黑色沉淀,且放置后不发生变化 |
| II | 5%NaOH溶液 | 产生白色沉淀,在空气中缓慢变成棕黑色沉淀 | 棕黑色沉淀增多,放置后溶液变为紫色,仍有沉淀 |
| III | 40%NaOH溶液 | 产生白色沉淀,在空气中缓慢变成棕黑色沉淀 | 棕黑色沉淀增多,放置后溶液变为紫色,仍有沉淀 |
 前,II、III中沉淀由白色变为黑色的化学方程式为
前,II、III中沉淀由白色变为黑色的化学方程式为(2)对比实验I、II通入
 后的实验现象,对于二价锰化合物还原性的认识是
后的实验现象,对于二价锰化合物还原性的认识是(3)根据资料ⅱ,III中应得到绿色溶液,实验中得到紫色溶液,分析现象与资料不符的原因:
原因一:可能是通入
 发生反应
发生反应 ,导致溶液的碱性减弱。但通过实验测定溶液的碱性变化很小。
,导致溶液的碱性减弱。但通过实验测定溶液的碱性变化很小。原因二:可能是氧化剂过量,氧化剂将
 氧化为
氧化为 。
。①取III中放置后的1mL悬浊液,加入4mL40%NaOH溶液,溶液紫色迅速变为绿色,且绿色缓慢加深。溶液紫色变为绿色的离子方程式为
 被
被②取II中放置后的1mL悬浊液,加入4mL水,溶液紫色缓慢加深,发生的反应是
③从反应速率的角度,分析实验III未得到绿色溶液的可能原因
您最近一年使用:0次
20-21高三·河北石家庄·阶段练习
名校
解题方法
5 . 已知HClO的电离常数K介于H2CO3的Ka1与Ka2之间,能正确表示下列反应的离子方程式的是
A.向等物质的量的NaOH和Na2CO3的混合溶液中滴加3倍体积的等浓度的稀盐酸:3H++CO +2OH-=HCO +2OH-=HCO +2H2O +2H2O |
B.将少量的双氧水滴入酸性高锰酸钾溶液中:7H2O2+2MnO +6H+=10H2O+2Mn2++6O2↑ +6H+=10H2O+2Mn2++6O2↑ |
C.将少量SO2通入“84”消毒液中:SO2+3ClO-+H2O=SO +Cl-+2HClO +Cl-+2HClO |
D.将少量氯气通入纯碱溶液中:Cl2+CO +H2O=Cl-+HCO +H2O=Cl-+HCO +HClO +HClO |
您最近一年使用:0次
2021-03-05更新
|
404次组卷
|
5卷引用:选择题16-20
(已下线)选择题16-20河北省石家庄精英中学2021届高三二轮专题一阶段考试化学试卷(已下线)重点2 离子反应-2021年高考化学【热点·重点·难点】专练(山东专用)(已下线)题型5 信息给予型离子方程式的书写-高考必备50个题型陕西省西安市长安区第一中学2021-2022学年高二下学期期中考试化学试题



