名校
1 . 二氧化锰( )与浓盐酸混合加热可得到氯气,如下是制取
)与浓盐酸混合加热可得到氯气,如下是制取 并探究
并探究 化学性质的装置图。
化学性质的装置图。
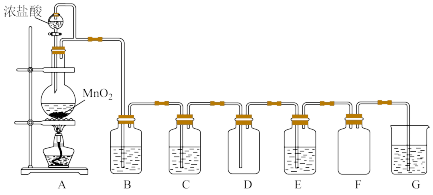
(1)盛装浓盐酸的仪器名称为_______ ,圆底烧瓶中发生反应的化学方程式为_______ 。
(2)若要得到干燥纯净的气体,则B中应盛放的试剂是_______ ,作用是_______ ;C中应盛放的试剂是_______ ,作用是_______ 。
(3)E中若装有淀粉—KI溶液,能观察到的实验现象是_______ 。
(4)F装置的作用是_______ ,G中盛有_______ 溶液,其作用是_______ (用离子方程式回答)
 )与浓盐酸混合加热可得到氯气,如下是制取
)与浓盐酸混合加热可得到氯气,如下是制取 并探究
并探究 化学性质的装置图。
化学性质的装置图。 
(1)盛装浓盐酸的仪器名称为
(2)若要得到干燥纯净的气体,则B中应盛放的试剂是
(3)E中若装有淀粉—KI溶液,能观察到的实验现象是
(4)F装置的作用是
您最近一年使用:0次
名校
2 . “84”消毒液的成分是NaClO,某化学研究性学习小组在实验室制备NaClO并探究其性质。该学习小组用如图装置进行实验(部分夹持装置略去),反应一段时间后,取C瓶中的溶液进行实验,测得溶液的pH=12。(查阅资料:饱和NaClO溶液pH为11)。回答下列问题:
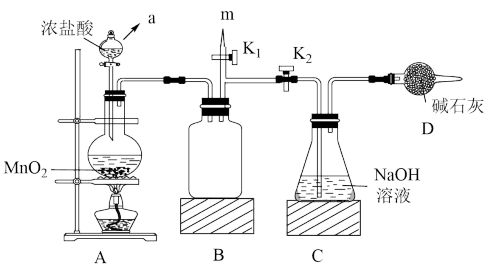
(1)仪器a的名称为_______ 。
(2)实验结束后,在m处最好连接盛______ (填“NaOH溶液”或“水”)的注射器,然后打开K1关闭K2,最后再拆除装置。
(3)测定C瓶溶液中NaClO含量的实验步骤如下:
步骤1:将C瓶溶液加入硫酸酸化,加入过量KI溶液,塞紧瓶塞并在暗处充分反应后滴入5~6滴淀粉溶液。
步骤2:分两次各取步骤1的溶液20mL于锥形瓶中,用0.1000mol·L-1Na2S2O3标准溶液滴定,滴定终点时两次耗Na2S2O3溶液体积的平均值为16.00mL。(已知:I2+2S2O =2I-+S4O
=2I-+S4O )
)
①步骤1的C瓶中发生反应的离子方程式为:_____ 。
②滴定终点的现象为______ 。
③C瓶溶液中NaClO含量为_____ g·L-1。
④若盛Na2S2O3标准溶液的滴定管未用Na2S2O3标准溶液润洗,则测得C瓶溶液中NaClO含量______ (填“偏大”、“偏小”或“不变”)。

(1)仪器a的名称为
(2)实验结束后,在m处最好连接盛
(3)测定C瓶溶液中NaClO含量的实验步骤如下:
步骤1:将C瓶溶液加入硫酸酸化,加入过量KI溶液,塞紧瓶塞并在暗处充分反应后滴入5~6滴淀粉溶液。
步骤2:分两次各取步骤1的溶液20mL于锥形瓶中,用0.1000mol·L-1Na2S2O3标准溶液滴定,滴定终点时两次耗Na2S2O3溶液体积的平均值为16.00mL。(已知:I2+2S2O
 =2I-+S4O
=2I-+S4O )
)①步骤1的C瓶中发生反应的离子方程式为:
②滴定终点的现象为
③C瓶溶液中NaClO含量为
④若盛Na2S2O3标准溶液的滴定管未用Na2S2O3标准溶液润洗,则测得C瓶溶液中NaClO含量
您最近一年使用:0次
2022-01-11更新
|
68次组卷
|
3卷引用:四川省广安市第二中学2021-2022学年高二下学期第一次月考化学试题



