1 . 下列物质结构与性质或物质性质与用途具有对应关系的是
A. 受热易分解,可用作化肥 受热易分解,可用作化肥 |
B. 性质稳定,可作为气体燃料 性质稳定,可作为气体燃料 |
C.纳米 能与酸反应,可用作铁磁性材料 能与酸反应,可用作铁磁性材料 |
D. 可与人体血液中血红蛋白结合, 可与人体血液中血红蛋白结合, 会引起人体中毒 会引起人体中毒 |
您最近一年使用:0次
解题方法
2 . 下列物质性质与用途具有对应关系的是
| A.N2性质不活泼,可作为粮食保护气 | B.NH3具有还原性,可用作致冷剂 |
| C.NO能被还原,可用于制备HNO3 | D.NH4Cl受热易分解,可用作铁的除锈剂 |
您最近一年使用:0次
3 . 合成17 t NH3,放出Q kJ热量。利用浓氨水吸收氯气工业的尾气,同时得到副产品NH4Cl;也可以用FeCl2溶液吸收氯气制得FeCl3溶液,然后制备Fe(OH)3胶体;经实验发现,溶液几乎都有丁达尔效应(粒子对光的散射现象),且丁达尔现象随其浓度升高逐渐增强,胶体的丁达尔现象比溶液的强。下列物质的性质与用途具有对应关系的是
| A.NH3具有还原性,可用作制冷剂 |
| B.NO有氧化性,可用于CO去除 |
| C.FeCl3溶液呈酸性,可用于腐蚀印刷电路板上的Cu |
| D.NH4Cl易溶于水,可用作化肥 |
您最近一年使用:0次
4 . 氧化物在生产、生活中有广泛应用。下列氧化物的性质与用途具有对应关系的是
| A.SO2具有氧化性,可用于纸浆漂白 |
| B.CaO能快速吸水,可用作食品干燥剂 |
| C.NO能被还原,可用于制备硝酸 |
| D.Al2O3具有两性,可用于电解冶炼铝 |
您最近一年使用:0次
5 . 一氧化氮、二氧化氮等氮氧化物是常见的大气污染物,然而它们在工业上有着广泛的用途。
已知:①室温下,2NO+Na2O2=2NaNO2;
②酸性条件下,NO或NO 都能与MnO
都能与MnO 反应生成NO
反应生成NO 和Mn2+,如5NO
和Mn2+,如5NO +2MnO
+2MnO +6H+=5NO
+6H+=5NO +2Mn2++3H2O。
+2Mn2++3H2O。
I.以木炭、浓硝酸、水和铜为原料生成的一氧化氮与过氧化钠反应制备亚硝酸钠的装置如图所示:
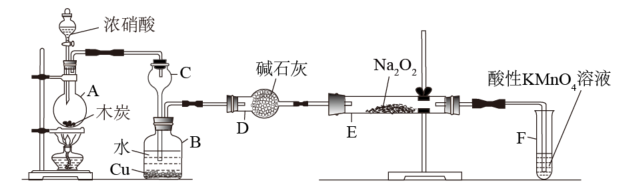
(1)A中观察到的现象是_______ 。
(2)B中反应的两个离子方程式分别是_______ 、_______ 。
(3)装置F的作用是_______ 。
II.某研究性学习小组对NO2和Na2O2能否发生反应进行探究。
[提出假设]假设一:NO2与Na2O2不反应:假设二:NO2能被Na2O2氧化;假设三 :_______ 。
[设计实验]
(1)实验时,将NO2气体通入盛有Na2O2的玻璃管中,淡黄色粉末完全变成白色,说明假设_______ 不成立。
(2)若假设二成立,则反应的化学方程式是_______ 。
(3)为验证假设二是否成立,该小组同学进行如下定性实验研究,请完成表中内容。(可供选择的试剂有:稀硫酸、稀盐酸、氯化铁溶液、高锰酸钾溶液。)
已知:①室温下,2NO+Na2O2=2NaNO2;
②酸性条件下,NO或NO
 都能与MnO
都能与MnO 反应生成NO
反应生成NO 和Mn2+,如5NO
和Mn2+,如5NO +2MnO
+2MnO +6H+=5NO
+6H+=5NO +2Mn2++3H2O。
+2Mn2++3H2O。I.以木炭、浓硝酸、水和铜为原料生成的一氧化氮与过氧化钠反应制备亚硝酸钠的装置如图所示:

(1)A中观察到的现象是
(2)B中反应的两个离子方程式分别是
(3)装置F的作用是
II.某研究性学习小组对NO2和Na2O2能否发生反应进行探究。
[提出假设]假设一:NO2与Na2O2不反应:假设二:NO2能被Na2O2氧化;假设三 :
[设计实验]
(1)实验时,将NO2气体通入盛有Na2O2的玻璃管中,淡黄色粉末完全变成白色,说明假设
(2)若假设二成立,则反应的化学方程式是
(3)为验证假设二是否成立,该小组同学进行如下定性实验研究,请完成表中内容。(可供选择的试剂有:稀硫酸、稀盐酸、氯化铁溶液、高锰酸钾溶液。)
| 实验步骤(不要求写具体操作过程,试剂、仪器任选) | 预期的实验现象及结论 |
| 取适量的白色固体置于试管中,加蒸馏水溶解, |
您最近一年使用:0次



