1 . 下列实验操作对应现象描述正确的是
| A.向紫色石蕊溶液中滴加氨水,溶液变红色 | B.蘸有浓硫酸的玻璃棒接近氨水瓶口,产生白烟 |
C.加热含足量 的品红溶液,溶液变红色 的品红溶液,溶液变红色 | D.在稀硫酸中加入铁粉,溶液变黄色 |
您最近半年使用:0次
2 . 化学与生产,生活息息相关.下列叙述错误的是
A.葡萄酒中添加 作杀菌剂 作杀菌剂 | B.熟石膏常用于制作医疗的石膏绷带 |
| C.二氧化硅常作太阳能电池板 | D.工业上常用液氨作制冷剂 |
您最近半年使用:0次
2024高三·全国·专题练习
解题方法
3 . 根据实验方案和现象,判断下列结论正确的是
| 选项 | 实验方案 | 现象 | 结论 |
| A | 将过量Cl2通入淀粉—碘化钾溶液中 | 溶液颜色最终未变蓝 | 说明Cl2不能氧化I- |
| B | 向0.1 mol·L-1 Na2S溶液中加入H2O2 | 产生淡黄色沉淀 | H2O2将S2-氧化为S |
| C | 在Ca(ClO)2溶液中通入SO2 | 产生白色沉淀 | 酸性:H2SO3>HClO |
| D | 用pH试纸分别测定1 mol·L-1的Na2S和1 mol·L-1的NaCl溶液的pH | 前者的试纸颜色比后者深 | 非金属性:S<Cl |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2024高三·全国·专题练习
4 . 根据下列实验现象所得出的结论正确的是
A.向某溶液中加入足量氯化钡溶液,生成白色沉淀,证明该溶液中含SO |
| B.向Na2S溶液中通入足量SO2,生成淡黄色沉淀,证明SO2具有酸性和氧化性 |
| C.向FeI2溶液中滴加少量氯水,溶液变为黄色,证明氧化性:Cl2>Fe3+ |
D.向某溶液中加入NaOH稀溶液,用湿润的蓝色石蕊试纸检验生成的气体时无颜色变化,证明该溶液中无NH |
您最近半年使用:0次
2024高三·全国·专题练习
解题方法
5 . 下列物质的应用中与该物质的氧化性或还原性无关的是
| A.过氧化钠用作供氧剂 | B.液氨用作制冷剂 |
| C.葡萄酒中添加二氧化硫 | D.铁粉用于食品保存 |
您最近半年使用:0次
名校
6 . 高砷煤中含有砷硫铁(FeAsS)等物质。燃煤产生的烟气中含NO、 、粉尘等,经过SCR脱硝除去NO,粉尘经沉降得到粉煤灰。
、粉尘等,经过SCR脱硝除去NO,粉尘经沉降得到粉煤灰。
(1)燃煤固硫
①燃烧高砷煤时加入生石灰将大部分硫元素转化为___________ (填化学式)留在煤渣中。
②高砷煤燃烧过程中,砷硫铁在高温下被氧化成 释放到烟气中,该反应的化学方程式为
释放到烟气中,该反应的化学方程式为___________ 。
(2)SCR脱硝(脱除烟气中的NO)
在烟气中加入适量氨气,用钒氧化物作催化剂将 、NO、
、NO、 转化为
转化为 。
。
①在SCR脱硝的反应中还原剂为___________ (填化学式)。
②若 与NO的物质的量之比为1∶1,写出SCR脱硝法的反应原理
与NO的物质的量之比为1∶1,写出SCR脱硝法的反应原理___________ (用化学方程式表示)。
(3)粉煤灰成分研究
粉煤灰可用于水泥工业,粉煤灰中的氨含量( 或铵盐)会影响水泥的性能。取50.00g粉煤灰加入NaOH蒸出
或铵盐)会影响水泥的性能。取50.00g粉煤灰加入NaOH蒸出 ,用20mL 0.1000
,用20mL 0.1000 的
的 溶液吸收
溶液吸收 ,用0.200
,用0.200 NaOH溶液滴定过量的
NaOH溶液滴定过量的 至终点,平行滴定3次,平均消耗NaOH溶液10.00mL,计算粉煤灰中的以
至终点,平行滴定3次,平均消耗NaOH溶液10.00mL,计算粉煤灰中的以 计的氨含量
计的氨含量___________ (用 表示,写出计算过程)。
表示,写出计算过程)。
 、粉尘等,经过SCR脱硝除去NO,粉尘经沉降得到粉煤灰。
、粉尘等,经过SCR脱硝除去NO,粉尘经沉降得到粉煤灰。(1)燃煤固硫
①燃烧高砷煤时加入生石灰将大部分硫元素转化为
②高砷煤燃烧过程中,砷硫铁在高温下被氧化成
 释放到烟气中,该反应的化学方程式为
释放到烟气中,该反应的化学方程式为(2)SCR脱硝(脱除烟气中的NO)
在烟气中加入适量氨气,用钒氧化物作催化剂将
 、NO、
、NO、 转化为
转化为 。
。①在SCR脱硝的反应中还原剂为
②若
 与NO的物质的量之比为1∶1,写出SCR脱硝法的反应原理
与NO的物质的量之比为1∶1,写出SCR脱硝法的反应原理(3)粉煤灰成分研究
粉煤灰可用于水泥工业,粉煤灰中的氨含量(
 或铵盐)会影响水泥的性能。取50.00g粉煤灰加入NaOH蒸出
或铵盐)会影响水泥的性能。取50.00g粉煤灰加入NaOH蒸出 ,用20mL 0.1000
,用20mL 0.1000 的
的 溶液吸收
溶液吸收 ,用0.200
,用0.200 NaOH溶液滴定过量的
NaOH溶液滴定过量的 至终点,平行滴定3次,平均消耗NaOH溶液10.00mL,计算粉煤灰中的以
至终点,平行滴定3次,平均消耗NaOH溶液10.00mL,计算粉煤灰中的以 计的氨含量
计的氨含量 表示,写出计算过程)。
表示,写出计算过程)。
您最近半年使用:0次
名校
7 . 某班同学用如下实验探究 、
、 的性质。(已知
的性质。(已知 遇
遇 溶液生成蓝色沉淀)回答下列问题:
溶液生成蓝色沉淀)回答下列问题:
(1)分别取一定量氯化铁、氯化亚铁固体,均配制成0.1 的溶液。在
的溶液。在 溶液中需加入少量铁屑,其目的是
溶液中需加入少量铁屑,其目的是___________ 。
(2)甲组同学取2mL 溶液,加入几滴氯水,再加入1滴KSCN溶液,溶液变红,说明
溶液,加入几滴氯水,再加入1滴KSCN溶液,溶液变红,说明 可将
可将 氧化。
氧化。 溶液与氯水反应的离子方程式为
溶液与氯水反应的离子方程式为___________ 。
(3)乙组同学认为甲组的实验不够严谨,该组同学在2mL 溶液中先加入0.5mL煤油,再于液面下依次加入几滴氯水和1滴KSCN溶液,溶液变红,煤油的作用是
溶液中先加入0.5mL煤油,再于液面下依次加入几滴氯水和1滴KSCN溶液,溶液变红,煤油的作用是___________ 。
(4)丙组同学取10mL 0.1 KI溶液,加入6mL 0.1
KI溶液,加入6mL 0.1
 溶液混合。分别取2mL此溶液于3支试管中进行如下实验:
溶液混合。分别取2mL此溶液于3支试管中进行如下实验:
①第一支试管中加入1mL 充分振荡、静置,
充分振荡、静置, 层显紫色;
层显紫色;
②第二支试管中加入1滴 溶液,生成蓝色沉淀;
溶液,生成蓝色沉淀;
③第三支试管中加入1滴KSCN溶液,溶液变红。
实验②检验的离子是___________ (填离子符号);实验①和③说明:在 过量的情况下,溶液中仍含有
过量的情况下,溶液中仍含有___________ (填离子符号),由此可以证明该氧化还原反应为___________ 。
(5)丁组同学向盛有 溶液的试管中加入几滴酸化的
溶液的试管中加入几滴酸化的 溶液,溶液变成棕黄色,发生反应的离子方程式为
溶液,溶液变成棕黄色,发生反应的离子方程式为___________ 。
(6)利用如图装置探究 的稳定性。
的稳定性。___________ (填字母)。
A. 、
、 、
、
B. 、
、 、
、 、
、
C.FeO、 、
、 、
、 、
、
②III中溴水是用来检验是否有 气体生成,若有
气体生成,若有 生成,溴水将褪色。实验中,观察到溴水褪色,据此推测
生成,溴水将褪色。实验中,观察到溴水褪色,据此推测 分解最有可能被氧化的元素是
分解最有可能被氧化的元素是___________ 。
③NaOH的作用是吸收 气体,请写出用过量NaOH溶液吸收
气体,请写出用过量NaOH溶液吸收 气体的化学方程式:
气体的化学方程式:___________ 。
 、
、 的性质。(已知
的性质。(已知 遇
遇 溶液生成蓝色沉淀)回答下列问题:
溶液生成蓝色沉淀)回答下列问题:(1)分别取一定量氯化铁、氯化亚铁固体,均配制成0.1
 的溶液。在
的溶液。在 溶液中需加入少量铁屑,其目的是
溶液中需加入少量铁屑,其目的是(2)甲组同学取2mL
 溶液,加入几滴氯水,再加入1滴KSCN溶液,溶液变红,说明
溶液,加入几滴氯水,再加入1滴KSCN溶液,溶液变红,说明 可将
可将 氧化。
氧化。 溶液与氯水反应的离子方程式为
溶液与氯水反应的离子方程式为(3)乙组同学认为甲组的实验不够严谨,该组同学在2mL
 溶液中先加入0.5mL煤油,再于液面下依次加入几滴氯水和1滴KSCN溶液,溶液变红,煤油的作用是
溶液中先加入0.5mL煤油,再于液面下依次加入几滴氯水和1滴KSCN溶液,溶液变红,煤油的作用是(4)丙组同学取10mL 0.1
 KI溶液,加入6mL 0.1
KI溶液,加入6mL 0.1
 溶液混合。分别取2mL此溶液于3支试管中进行如下实验:
溶液混合。分别取2mL此溶液于3支试管中进行如下实验:①第一支试管中加入1mL
 充分振荡、静置,
充分振荡、静置, 层显紫色;
层显紫色;②第二支试管中加入1滴
 溶液,生成蓝色沉淀;
溶液,生成蓝色沉淀;③第三支试管中加入1滴KSCN溶液,溶液变红。
实验②检验的离子是
 过量的情况下,溶液中仍含有
过量的情况下,溶液中仍含有(5)丁组同学向盛有
 溶液的试管中加入几滴酸化的
溶液的试管中加入几滴酸化的 溶液,溶液变成棕黄色,发生反应的离子方程式为
溶液,溶液变成棕黄色,发生反应的离子方程式为(6)利用如图装置探究
 的稳定性。
的稳定性。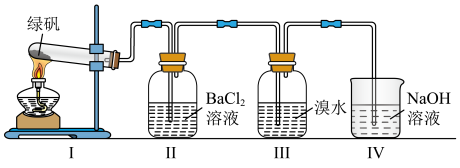
A.
 、
、 、
、
B.
 、
、 、
、 、
、
C.FeO、
 、
、 、
、 、
、
②III中溴水是用来检验是否有
 气体生成,若有
气体生成,若有 生成,溴水将褪色。实验中,观察到溴水褪色,据此推测
生成,溴水将褪色。实验中,观察到溴水褪色,据此推测 分解最有可能被氧化的元素是
分解最有可能被氧化的元素是③NaOH的作用是吸收
 气体,请写出用过量NaOH溶液吸收
气体,请写出用过量NaOH溶液吸收 气体的化学方程式:
气体的化学方程式:
您最近半年使用:0次
名校
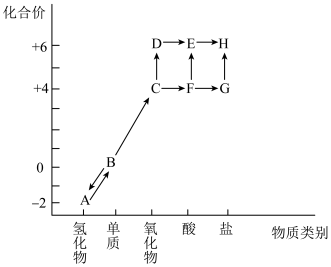
8 . “价—类”二维图是预测物质性质的重要思维工具。下图是硫元素的常见化合价与部分物质类别的对应关系。___________ 氧化物。
(2)A 中硫元素处于最低化合价,具有___________ 性,预测 A 溶液久置于空气会出现的现象为___________ ,写出发生反应的化学方程式___________ 。
(3)试管内壁附着的单质B可用热的NaOH溶液洗涤,反应过程中仅生成G、水以及另一种钠盐,上述反应过程中生成的“另一种钠盐”的化学式为___________ 。
(4)检验某溶液中是否含有 的方法为
的方法为___________ 。
(5)E的浓溶液与碳单质在加热条件下发生反应,若要验证气体产物有CO2和SO2可选择以下试剂进行实验:①酸性高锰酸钾溶液 ②品红溶液 ③澄清石灰水
合理的顺序为___________ :
___________→___________→ ___________→___________(填序号)。
(2)A 中硫元素处于最低化合价,具有
(3)试管内壁附着的单质B可用热的NaOH溶液洗涤,反应过程中仅生成G、水以及另一种钠盐,上述反应过程中生成的“另一种钠盐”的化学式为
(4)检验某溶液中是否含有
 的方法为
的方法为(5)E的浓溶液与碳单质在加热条件下发生反应,若要验证气体产物有CO2和SO2可选择以下试剂进行实验:①酸性高锰酸钾溶液 ②品红溶液 ③澄清石灰水
合理的顺序为
___________→___________→ ___________→___________(填序号)。
您最近半年使用:0次
9 . 化学与生产、生活密切相关。下列说法错误 的是
| A.葡萄酒中添加适量的SO2可以起到杀菌和抗氧化的作用 |
| B.硫酸钡俗称“钡餐”,在医疗上可被用作消化系统X射线检查的内服药剂 |
| C.SiO2具有导电性,可用来制造硅太阳能电池、光导纤维 |
| D.“祝融号”火星车使用的新型铝基碳化硅复合材料中的碳化硅是一种新型无机非金属材料 |
您最近半年使用:0次
名校
10 . 按要求填空
(1)浓硫酸具有如下的性质: A.酸性B.强氧化性C.吸水性D.脱水性,E难挥发性。下列事实主要表现浓硫酸的什么性质(填字母序号)。
①浓硫酸使蔗糖变黑___________ ;
②碳投入热的浓硫酸中溶解___________ ;
③浓硫酸与氧化铜反应___________ ;
④浓硫酸干燥氢气___________ 。
(2)浓硝酸具有如下的性质:A.酸性B.强氧化性C.不稳定性,下列事实主要表现浓硝酸的什么性质(填字母序号)。
①浓硝酸需避光保存___________ ;
②常温下可用铝或者铁遇浓硝酸钝化___________ 。
(3)二氧化硫气体在下列反应中表现的性质填写在横线上(填字母序号)。
A氧化性 B.漂白性 C.还原性 D.酸性氧化物的性质
①SO2+2OH= +H2O
+H2O___________ ;
②SO2+2H2S=3S↓+2H2O___________ ;
③SO2+Ca(OH)2=CaSO3↓+H2O___________ ;
④SO2+Cl2+2H2O=2HCl+H2SO4___________ 。
(4)氮元素是地球大气中含量最多的元素,请完成下列有关问题:
①写出氮元素的原子结构示意图:___________ 。
②通常情况下,氮气性质不活泼,其原因是___________ 。
A氮分子是双原子分子 B.氮元素的非金属性很强
C.氮原子的半径较小 D.破坏氮分子中的化学键很难
③N2的电子式:___________ 。
④氨是一种重要的化工原料,请写出工业合成氨的化学方程式:___________ 。
⑤检验NH3的方法是___________ 。
(1)浓硫酸具有如下的性质: A.酸性B.强氧化性C.吸水性D.脱水性,E难挥发性。下列事实主要表现浓硫酸的什么性质(填字母序号)。
①浓硫酸使蔗糖变黑
②碳投入热的浓硫酸中溶解
③浓硫酸与氧化铜反应
④浓硫酸干燥氢气
(2)浓硝酸具有如下的性质:A.酸性B.强氧化性C.不稳定性,下列事实主要表现浓硝酸的什么性质(填字母序号)。
①浓硝酸需避光保存
②常温下可用铝或者铁遇浓硝酸钝化
(3)二氧化硫气体在下列反应中表现的性质填写在横线上(填字母序号)。
A氧化性 B.漂白性 C.还原性 D.酸性氧化物的性质
①SO2+2OH=
 +H2O
+H2O②SO2+2H2S=3S↓+2H2O
③SO2+Ca(OH)2=CaSO3↓+H2O
④SO2+Cl2+2H2O=2HCl+H2SO4
(4)氮元素是地球大气中含量最多的元素,请完成下列有关问题:
①写出氮元素的原子结构示意图:
②通常情况下,氮气性质不活泼,其原因是
A氮分子是双原子分子 B.氮元素的非金属性很强
C.氮原子的半径较小 D.破坏氮分子中的化学键很难
③N2的电子式:
④氨是一种重要的化工原料,请写出工业合成氨的化学方程式:
⑤检验NH3的方法是
您最近半年使用:0次



