2022高一·上海·专题练习
解题方法
1 . 298K时,向V升真空容器中通入n摩SO2和m摩H2S。
(1)若n=2,则当m=_______ 时,反应后容器内气体的密度最小。
(2)若2n>m,则反应后氧化产物与还原产物的质量差为_______ 克。
(3)若5n=m,且反应后氧化产物与还原产物的质量和为48克,则n+m=_______ 。
(1)若n=2,则当m=
(2)若2n>m,则反应后氧化产物与还原产物的质量差为
(3)若5n=m,且反应后氧化产物与还原产物的质量和为48克,则n+m=
您最近一年使用:0次
2 . 将一定量 通入
通入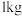 质量分数为
质量分数为 的
的 溶液中,制成含有
溶液中,制成含有 和
和 的混合溶液。用此溶液吸收标准状况下
的混合溶液。用此溶液吸收标准状况下 ,恰好形成中性溶液(假设气体均完全反应),请计算:
,恰好形成中性溶液(假设气体均完全反应),请计算:
(1) 溶液中
溶液中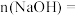
___________  。
。
(2)已知混合溶液中 ,则混合溶液中
,则混合溶液中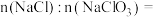
___________ 。
(3)所通 在标准状况下的体积为
在标准状况下的体积为___________ L。
 通入
通入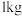 质量分数为
质量分数为 的
的 溶液中,制成含有
溶液中,制成含有 和
和 的混合溶液。用此溶液吸收标准状况下
的混合溶液。用此溶液吸收标准状况下 ,恰好形成中性溶液(假设气体均完全反应),请计算:
,恰好形成中性溶液(假设气体均完全反应),请计算:(1)
 溶液中
溶液中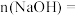
 。
。(2)已知混合溶液中
 ,则混合溶液中
,则混合溶液中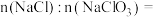
(3)所通
 在标准状况下的体积为
在标准状况下的体积为
您最近一年使用:0次
2022-05-04更新
|
903次组卷
|
4卷引用:浙江省杭州地区(含周边)重点中学2021-2022学年高一下学期期中考试化学试题
3 . 某工厂使用的煤中硫的质量分数为1.28%,该工厂每天燃烧这种煤100t,请计算:
(1)100t该煤含S的物质的量为_______ mol。
(2)假设煤中的硫全部转化为SO2,每天产生的SO2气体在标准状况下体积为_______ L。
(3)若把产生的SO2全部用来生产硫酸,每天可得到98%的浓硫酸质量_______ 吨(请写出计算过程)
(1)100t该煤含S的物质的量为
(2)假设煤中的硫全部转化为SO2,每天产生的SO2气体在标准状况下体积为
(3)若把产生的SO2全部用来生产硫酸,每天可得到98%的浓硫酸质量
您最近一年使用:0次
2022-01-23更新
|
634次组卷
|
2卷引用: 浙江省丽水市2021-2022学年高一上学期普通高中教学质量监控(期末)化学试题
名校
解题方法
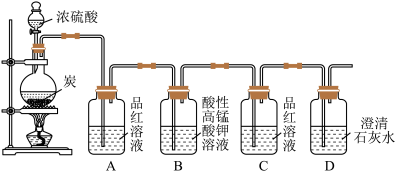
4 . 某同学欲验证碳与浓硫酸反应产物的性质。现已将装置如图连接,请回答下列问题。
(1)烧瓶中发生反应的化学反应方程式是___________ 。
(2)实验中两次使用到品红溶液,其目的不同。A的使用目的是_____ ,通过洗气瓶C中无现象和___ 的现象,证明反应有_______ (填化学式)生成。
(3)洗气瓶B中溶液颜色变浅,说明碳与浓硫酸反应的产物之一______ (填名称)具有______ 的性质。
(4)实验完成后,取出洗气瓶A中的无色溶液于试管中,加热,可观察到__________ 。
(1)烧瓶中发生反应的化学反应方程式是
(2)实验中两次使用到品红溶液,其目的不同。A的使用目的是
(3)洗气瓶B中溶液颜色变浅,说明碳与浓硫酸反应的产物之一
(4)实验完成后,取出洗气瓶A中的无色溶液于试管中,加热,可观察到
您最近一年使用:0次
2020-01-05更新
|
360次组卷
|
3卷引用:贵州省从江县第一民族中学2021-2022学年高一下学期第一次月考化学试题
5 . 一定量的SO2通入到含0.16mol NaOH的溶液中,充分反应后生成的Na2SO3和 NaHSO3物质的量之比为3:2。再向反应后溶液中通入Cl2使硫元素全部转化为SO42-。
请计算:
(1)SO2的质量为___________________ g。
(2)通入Cl2的物质的量至少为___________________ mol。
请计算:
(1)SO2的质量为
(2)通入Cl2的物质的量至少为
您最近一年使用:0次
2018-03-10更新
|
619次组卷
|
6卷引用:安徽省芜湖市2021-2022学年高一下学期期末质量监测化学试题



