名校
1 . 下列方案设计、现象和结论均正确的是
| 目的 | 方案设计 | 现象和结论 | |
| A | 证明 与 与 在光照条件下发生的是取代反应 在光照条件下发生的是取代反应 | 通过排饱和NaCl溶液的方法收集半试管 和半试管 和半试管 ,固定好后,放在光亮处,静置,反应结束后用手堵住试管口取出试管,向其中加硝酸银溶液 ,固定好后,放在光亮处,静置,反应结束后用手堵住试管口取出试管,向其中加硝酸银溶液 | 若出现白色沉淀,说明有 生成,发生的是取代反应 生成,发生的是取代反应 |
| B | 探究 固体样品是否变质 固体样品是否变质 | 取少量待测样品溶于蒸馏水,加入足量稀硝酸,再加入足量 溶液 溶液 | 若有白色沉淀产生,则样品已经变质 |
| C | 检验某无色气体是否为 | 将气体通入品红溶液中,再加热 | 若通入气体后品红溶液褪色,加热该褪色溶液能恢复红色,则一定为 |
| D | 探究铁与水蒸气发生反应后的产物中铁元素的价态 | 取少量固体产物溶于足量稀硫酸后,再取上层清液,依次入KSCN溶液和双氧水 | 若上层清液开始无明显现象,加双氧水后出现红色溶液,则说明产物中含+2价的铁 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-04-20更新
|
257次组卷
|
2卷引用:浙江省杭州市及周边重点中学2022-2023学年高一下学期期中考试化学试题
名校
2 . 下列各实验的现象或结论有错误的是
| 选项 | 实验 | 现象 | 结论 |
| A | 取少量 固体样品溶于蒸馏水,加入足量稀盐酸,再加入足量 固体样品溶于蒸馏水,加入足量稀盐酸,再加入足量 溶液 溶液 | 有白色沉淀产生 |  固体样品已变质 固体样品已变质 |
| B | 将氧气通入 的水溶液中 的水溶液中 | 溶液变浑浊 | 氧的非金属性大于硫 |
| C | 浓硫酸滴入蔗糖中,产生的气体通入澄清石灰水 | 蔗糖变黑、体积膨胀,澄清石灰水变浑浊 | 使澄清石灰水变浑浊的气体一定是 |
| D | 向滴有酚酞的 溶液中加入 溶液中加入 固体 固体 | 溶液中有白色沉淀生成,溶液中的红色褪去 |  溶液中存在 溶液中存在 的水解平衡 的水解平衡 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-11-08更新
|
112次组卷
|
2卷引用:河南省周口市项城市2023-2024学年高三上学期11月期中联考化学试题
解题方法
3 . 在“价-类”二维图中融入“杠杆模型”,可直观辨析部分物质转化及其定量关系。图中的字母分别代表硫及其常见化合物,f、g均为含钠元素的正盐,请回答:
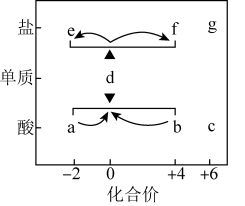
(1)当a与b混合时,可观察到的现象是___________ ;
(2)固体f露置在空气中易变质转化为g,该转化的化学方程式为___________ ;
(3)某同学利用下列装置测定空气中 的含量。
的含量。
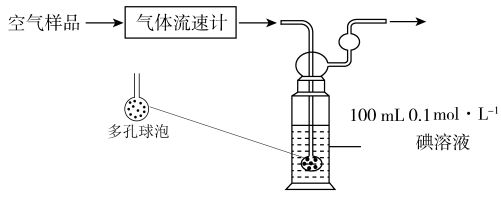
通空气样品的导管末端是带许多小孔的玻璃球泡,其主要作用是___________ ,该装置中 与碘
与碘 溶液发生反应的化学方程式为:
溶液发生反应的化学方程式为:___________ 。若空气流速为 ,当
,当 与碘
与碘 溶液恰好完全反应时,耗时10min,则该空气样品中
溶液恰好完全反应时,耗时10min,则该空气样品中 的含量是
的含量是___________  。(用含V的最简表达式表示)
。(用含V的最简表达式表示)

(1)当a与b混合时,可观察到的现象是
(2)固体f露置在空气中易变质转化为g,该转化的化学方程式为
(3)某同学利用下列装置测定空气中
 的含量。
的含量。
通空气样品的导管末端是带许多小孔的玻璃球泡,其主要作用是
 与碘
与碘 溶液发生反应的化学方程式为:
溶液发生反应的化学方程式为: ,当
,当 与碘
与碘 溶液恰好完全反应时,耗时10min,则该空气样品中
溶液恰好完全反应时,耗时10min,则该空气样品中 的含量是
的含量是 。(用含V的最简表达式表示)
。(用含V的最简表达式表示)
您最近一年使用:0次
2023-04-21更新
|
177次组卷
|
2卷引用:浙江省杭州市六县九校联考2022-2023学年高一下学期4月期中考试化学试题
名校
解题方法
4 . 下列每组的叙述Ⅰ、Ⅱ都正确,且有因果关系的是
| 叙述Ⅰ | 叙述Ⅱ | |
| A | 实验室中可通加热固体氯化铵的方法制备氨气 | 氯化铵受热易分解生成氨气 |
| B | 将纯净的 通入紫色石蕊试液中,溶液褪色 通入紫色石蕊试液中,溶液褪色 |  有漂白性 有漂白性 |
| C | 断裂 分子中H-N键要吸收热量 分子中H-N键要吸收热量 | 工业上用液氨作制冷剂 |
| D | 取少量 固体样品溶于蒸馏水,加入足量稀盐酸,再加入足量 固体样品溶于蒸馏水,加入足量稀盐酸,再加入足量 溶液,若有白色沉淀产生,说明产品已变质 溶液,若有白色沉淀产生,说明产品已变质 |  暴露于空气中容易被氧化为 暴露于空气中容易被氧化为 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
5 . 硫酸亚铁在农业上可以做杀虫剂,防治大麦的黑穗病,工业上可用于染色和木材防腐。现用以下装置研究硫酸亚铁受热分解的产物。相关固定和加热装置已经省略。左侧试管中的粉末是FeSO4,在实验中用酒精灯对试管进行加热。加热过程中白色粉末逐渐变成红色,在中间U型管中收集到无色透明固体X,右侧集气瓶中收集到少量无色气体Y。实验结束后对相关产物进行了研究。
已知:SO3是无色易挥发的固体,熔点16.8 oC,沸点44.8 oC。
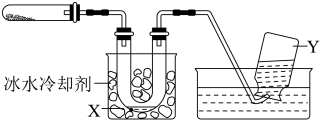
(1)当右侧导管口不再有气泡冒出时,说明反应已经停止,此时合理的操作是___________ 。
(2)为了证明反应后的红色粉末是Fe2O3,而不含Fe3O4和FeO,进行实验:取少量反应后的粉末于试管中,___________ ,证明该粉末中不含Fe3O4和FeO。
(3)实验后将气体Y通入含有品红溶液的试管中,品红褪色,证明集气瓶中收集到的气体Y是___________ 。
(4)根据以上结果,写出FeSO4分解的化学方程式:___________ 。
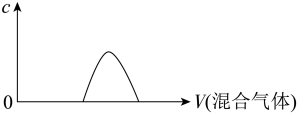
(5)若将反应中产生的SO2和SO3混合气体持续通入到200 mL 0.2 mol/L的NaOH溶液中,溶液中某离子浓度随混合气体体积变化关系如下图所示,写出这种离子的化学式:___________ 。
(6)FeSO4在空气中容易变质为黄褐色碱式硫酸铁,该化合物中含1种阳离子和2种阴离子,且2种阴离子的数目相等,写出由FeSO4生成碱式硫酸铁的化学方程式:___________ 。
已知:SO3是无色易挥发的固体,熔点16.8 oC,沸点44.8 oC。

(1)当右侧导管口不再有气泡冒出时,说明反应已经停止,此时合理的操作是
(2)为了证明反应后的红色粉末是Fe2O3,而不含Fe3O4和FeO,进行实验:取少量反应后的粉末于试管中,
(3)实验后将气体Y通入含有品红溶液的试管中,品红褪色,证明集气瓶中收集到的气体Y是
(4)根据以上结果,写出FeSO4分解的化学方程式:
(5)若将反应中产生的SO2和SO3混合气体持续通入到200 mL 0.2 mol/L的NaOH溶液中,溶液中某离子浓度随混合气体体积变化关系如下图所示,写出这种离子的化学式:

(6)FeSO4在空气中容易变质为黄褐色碱式硫酸铁,该化合物中含1种阳离子和2种阴离子,且2种阴离子的数目相等,写出由FeSO4生成碱式硫酸铁的化学方程式:
您最近一年使用:0次



