1 . 下列有关实验、现象及结论等叙述正确的个数有
①向溶有SO2的BaCl2溶液中通入气体X,出现白色沉淀,X具有强氧化性
②将稀盐酸滴入硅酸钠溶液中,充分振荡,有白色沉淀产生,非金属性:Cl>Si
③向X溶液加新制氯水,再加入少量KSCN溶液,溶液变为红色,X溶液中一定含有Fe2+
④向饱和NaHCO3溶液中滴加硼酸,无气泡产生,酸性:硼酸<碳酸
⑤取少量Fe(NO3)2样品溶于稀硫酸,滴入KSCN溶液,溶液变红色,证明样品已变质
⑥除去干燥CO2中混有的少量SO2,可将混合气体依次通过盛有酸性KMnO4溶液、浓硫酸的洗气瓶
①向溶有SO2的BaCl2溶液中通入气体X,出现白色沉淀,X具有强氧化性
②将稀盐酸滴入硅酸钠溶液中,充分振荡,有白色沉淀产生,非金属性:Cl>Si
③向X溶液加新制氯水,再加入少量KSCN溶液,溶液变为红色,X溶液中一定含有Fe2+
④向饱和NaHCO3溶液中滴加硼酸,无气泡产生,酸性:硼酸<碳酸
⑤取少量Fe(NO3)2样品溶于稀硫酸,滴入KSCN溶液,溶液变红色,证明样品已变质
⑥除去干燥CO2中混有的少量SO2,可将混合气体依次通过盛有酸性KMnO4溶液、浓硫酸的洗气瓶
| A.1个 | B.2个 | C.3个 | D.4个 |
您最近一年使用:0次
2024-04-19更新
|
297次组卷
|
2卷引用:黑龙江省大庆铁人中学2023-2024学年高一下学期开学考试化学试题
解题方法
2 . 常温下,根据下列实验操作和现象得出的结论正确的是
| 选项 | 实验操作和现象 | 实验结论 |
| A | 分别测量浓度均为0.1mol·L-1Na2CO3溶液和Na[Al(OH)4]溶液的pH,后者pH更大 | Al(OH) 比CO 比CO 更容易结合H+ 更容易结合H+ |
| B | 将亚硫酸钠样品溶于水,加入盐酸酸化的Ba(NO3)2溶液,出现白色沉淀 | 亚硫酸钠样品已变质 |
| C | 将盐酸滴入Na2CO3溶液产生无色气体,将产生的气体直接通入Na2SiO3溶液, | 非金属性:Cl>C>Si |
| D | 向BaCl2溶液中通入SO2和气体X,出现白色沉淀 | 气体X一定具有氧化性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
3 . 硫和氮及其化合物在生产生活中应用广泛。请回答:
(1)蔗糖炭化的过程中,会发生反应:C+2H2SO4(浓) CO2↑+2SO2↑+2H2O,若生成0.5 mol CO2,则转移电子的物质的量是
CO2↑+2SO2↑+2H2O,若生成0.5 mol CO2,则转移电子的物质的量是______ mol,蔗糖炭化过程体现了浓H2SO4的____ (选填:脱水性、吸水性、氧化性、酸性)。
(2)实验室有一瓶放置很久的Na2SO3固体药品,小明同学想设计一个实验验证这瓶药品有没有变质?请你帮助他设计一个实验______________________________________ 。
(3)Cl2和SO2均可以使品红溶液褪色,将二者等体积混合通入品红,发现红色不褪去,用化学方程式解释其原因__________________________________________________ 。
(4)工业上可以通过氮气和氢气在一定条件下合成氨气。下列关于氨气的性质和用途描述正确的是____________ 。
A.氨气易液化,液氨可作制冷剂 B.可用排水法收集氨气
C.氨气是一种无色无味的气体 D.向氨水中滴加酚酞,溶液变红
(5)氨气在一定条件下还可以被氧气所氧化,请写出化学方程式_____________________
(6)实验室检验试管里氨气是否收集满的方法是___________________ (写出一种即可)。
(7)25.6 g Cu与含2 mol/L的HNO3和1mol/LH2SO4的200mL混合酸充分反应,反应后收集到的气体在标准状况下的体积为___________________ (假设HNO3还原产物为NO)。
(1)蔗糖炭化的过程中,会发生反应:C+2H2SO4(浓)
 CO2↑+2SO2↑+2H2O,若生成0.5 mol CO2,则转移电子的物质的量是
CO2↑+2SO2↑+2H2O,若生成0.5 mol CO2,则转移电子的物质的量是(2)实验室有一瓶放置很久的Na2SO3固体药品,小明同学想设计一个实验验证这瓶药品有没有变质?请你帮助他设计一个实验
(3)Cl2和SO2均可以使品红溶液褪色,将二者等体积混合通入品红,发现红色不褪去,用化学方程式解释其原因
(4)工业上可以通过氮气和氢气在一定条件下合成氨气。下列关于氨气的性质和用途描述正确的是
A.氨气易液化,液氨可作制冷剂 B.可用排水法收集氨气
C.氨气是一种无色无味的气体 D.向氨水中滴加酚酞,溶液变红
(5)氨气在一定条件下还可以被氧气所氧化,请写出化学方程式
(6)实验室检验试管里氨气是否收集满的方法是
(7)25.6 g Cu与含2 mol/L的HNO3和1mol/LH2SO4的200mL混合酸充分反应,反应后收集到的气体在标准状况下的体积为
您最近一年使用:0次
2020-07-06更新
|
114次组卷
|
2卷引用:黑龙江省哈尔滨师范大学附属中学2020-2021学年高三上学期开学考试化学试题
名校
解题方法
4 . 研究小组为探究 在空气中变质后的产物,进行如下实验并记录现象。
在空气中变质后的产物,进行如下实验并记录现象。
实验①:取 样品加水溶解,得到澄清溶液a。
样品加水溶解,得到澄清溶液a。
实验②:取少量溶液a,向其中加入过量盐酸,有臭鸡蛋气味的气体生成,且出现淡黄色浑浊。
实验③:将实验②中的浊液过滤,向滤液中加入 溶液,产生白色沉淀。
溶液,产生白色沉淀。
已知信息:i. 溶液能溶解S,并生成
溶液能溶解S,并生成 ,
, 与酸反应生成S和
与酸反应生成S和 (臭鸡蛋气味);ii.
(臭鸡蛋气味);ii. 易溶于水。
易溶于水。
下列说法不正确的是
 在空气中变质后的产物,进行如下实验并记录现象。
在空气中变质后的产物,进行如下实验并记录现象。实验①:取
 样品加水溶解,得到澄清溶液a。
样品加水溶解,得到澄清溶液a。实验②:取少量溶液a,向其中加入过量盐酸,有臭鸡蛋气味的气体生成,且出现淡黄色浑浊。
实验③:将实验②中的浊液过滤,向滤液中加入
 溶液,产生白色沉淀。
溶液,产生白色沉淀。已知信息:i.
 溶液能溶解S,并生成
溶液能溶解S,并生成 ,
, 与酸反应生成S和
与酸反应生成S和 (臭鸡蛋气味);ii.
(臭鸡蛋气味);ii. 易溶于水。
易溶于水。下列说法不正确的是
A.实验②中淡黄色浑浊可能是 与 与 反应产生的 反应产生的 |
B.实验①和实验②说明 样品中一定含有S 样品中一定含有S |
C.实验③中产生的白色沉淀是 |
D. 样品中可能含有 样品中可能含有 |
您最近一年使用:0次
2023-02-09更新
|
685次组卷
|
12卷引用:北京交通大学附属中学2023-2024学年高三上学期开学考试化学试题
北京交通大学附属中学2023-2024学年高三上学期开学考试化学试题北京市第一○一中学2023-2024学年高三下学期开学考试化学试题北京市西城区2021~2022学年高三上学期期末考试化学试题河北省五校联盟(保定市第一中学等)2021-2022学年高三下学期3月模拟考试化学试题(已下线)二轮拔高卷2-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(北京专用)(已下线)化学-2022年高考押题预测卷01(北京卷)安徽省示范高中培优联盟 2022-2023学年高二上学期联赛化学试题黑龙江省佳木斯市第十二中学2022-2023学年高三上学期期中考试化学试题巩固训练7北京市第二中学2022-2023学年高二下学期3月月考化学试题北京市第二中学2023-2024学年高三上学期12月月考化学试题(已下线)北京市第四中学2023-2024学年高三下学期一模模拟化学试题
5 . 如图是铜与浓硫酸反应并验证其产物性质的装置图。请回答下列问题。
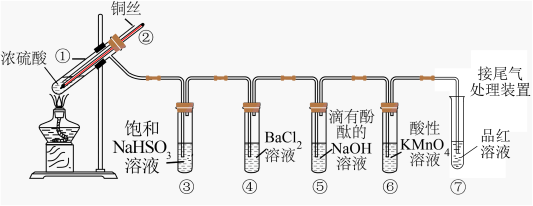
(1)试管①中发生反应的化学方程式为____ ;其中硫酸发生了____ (填“氧化”或“还原”)反应。
(2)一段时间后,④中溶液无明显现象,⑤⑥⑦溶液均褪色,试管⑤⑥⑦中的现象分别说明SO2的水溶液具有____ 、SO2具有____ 、漂白性。
(3)下列说法正确的是____ (填字母)。
a.上下移动铜丝可控制反应的发生与停止
b.反应结束后,从导管向装置中鼓入空气,使气体完全被吸收,防止污染
c.实验结束后,试管①中有白色固体出现,为确认白色固体为产物CuSO4,可立刻向试管①中加水,观察颜色
(4)充分反应后发现,铜丝与硫酸都有剩余,在此情况下,加入下列物质能使溶液中n(Cu2+)变大的是____ (填字母)。
a.HClb.Fe2O3c.KNO3
(5)反应停止后,待装置冷却,向试管④中加入氯水,产生白色沉淀,反应的离子方程式为____ 。
(6)为了测定尾气中SO2的含量,将尾气样品经过管道通入盛有400mL0.1mol·L-1酸性KMnO4溶液的密闭容器中。若管道中气体流量为aL·min-1,经过8min溶液恰好褪色,假定样品中SO2被充分吸收,该尾气样品中SO2的含量为____ g·L-1。(假设尾气中其他气体不与酸性KMnO4溶液反应)

(1)试管①中发生反应的化学方程式为
(2)一段时间后,④中溶液无明显现象,⑤⑥⑦溶液均褪色,试管⑤⑥⑦中的现象分别说明SO2的水溶液具有
(3)下列说法正确的是
a.上下移动铜丝可控制反应的发生与停止
b.反应结束后,从导管向装置中鼓入空气,使气体完全被吸收,防止污染
c.实验结束后,试管①中有白色固体出现,为确认白色固体为产物CuSO4,可立刻向试管①中加水,观察颜色
(4)充分反应后发现,铜丝与硫酸都有剩余,在此情况下,加入下列物质能使溶液中n(Cu2+)变大的是
a.HClb.Fe2O3c.KNO3
(5)反应停止后,待装置冷却,向试管④中加入氯水,产生白色沉淀,反应的离子方程式为
(6)为了测定尾气中SO2的含量,将尾气样品经过管道通入盛有400mL0.1mol·L-1酸性KMnO4溶液的密闭容器中。若管道中气体流量为aL·min-1,经过8min溶液恰好褪色,假定样品中SO2被充分吸收,该尾气样品中SO2的含量为
您最近一年使用:0次
2022-08-24更新
|
77次组卷
|
2卷引用:安徽省宣城市三校2022-2023学年高二上学期期初联考化学试题
名校
6 . 研究性学习小组对某硫酸亚铁晶体(FeSO4·xH2O)热分解研究,该小组同学称取ag硫酸亚铁晶体样品按下图高温加热,使其完全分解,对所得产物进行探究,并通过称量装置B质量测出x的值。
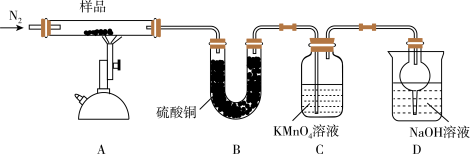
(1)装置B中硫酸铜粉末变蓝,质量增加12.6g,说明产物中有_____ (填分子式)。
(2)硫酸亚铁晶体完全分解后装置A中还残留红棕色固体氧化铁。
(3)装置C中高锰酸钾溶液褪色,说明产物中存在_____ (填氧化性或还原性)气体_____ (填分子式)。
(4)实验中要持续通入氮气,否则测出的x会_____ (填“偏大”、“偏小”或“不变”)。
(5)从理论上分析得出硫酸亚铁分解还生成另-物质三氧化硫,写出硫酸亚铁分解的化学方程式____ 。
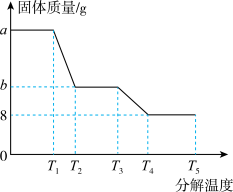
(6)某研究所利用SDTQ600热分析仪对硫酸亚铁晶体(FeSO4·xH2O)进行热分解,获得相关数据,绘制成固体质量一分解温度的关系如图,根据图中有关数据,可计算出FeSO4·xH2O中的x=_____ 。(写出计算过程)

(1)装置B中硫酸铜粉末变蓝,质量增加12.6g,说明产物中有
(2)硫酸亚铁晶体完全分解后装置A中还残留红棕色固体氧化铁。
(3)装置C中高锰酸钾溶液褪色,说明产物中存在
(4)实验中要持续通入氮气,否则测出的x会
(5)从理论上分析得出硫酸亚铁分解还生成另-物质三氧化硫,写出硫酸亚铁分解的化学方程式
(6)某研究所利用SDTQ600热分析仪对硫酸亚铁晶体(FeSO4·xH2O)进行热分解,获得相关数据,绘制成固体质量一分解温度的关系如图,根据图中有关数据,可计算出FeSO4·xH2O中的x=

您最近一年使用:0次
2020-08-31更新
|
370次组卷
|
3卷引用:江苏省启东中学2020-2021学年高一上学期期初考试化学试题
江苏省启东中学2020-2021学年高一上学期期初考试化学试题河北省张家口市宣化第一中学2021-2022学年高一上学期期初考试化学试题(已下线)第1章 章末检测-2020-2021学年高一化学同步课堂帮帮帮(人教版2019必修第一册)



