1 . 高纯二氧化硅可用来制造光纤。某蛇纹石的成分见下表:
通过下图流程可由蛇纹石制备较纯净的二氧化硅。
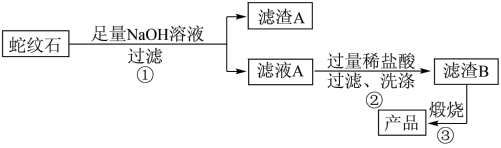
(1)蛇纹石中涉及的可溶性金属氧化物有_______ (写化学式)。
(2)步骤①中涉及SiO2反应的离子方程式为_______ 。
(3)滤渣 的成分有
的成分有_______ (填化学式)。
(4)步骤②中洗涤沉淀的方法是_______
(5)步骤③反应的化学方程式为____ ;实验室进行步骤③需要用到的主要仪器有____ 、泥三角、酒精灯和____
| 组分 | SiO2 | MgO | Na2O | K2O | Fe2O3 |
| 质量分数/% | 59.20 | 38.80 | 0.25 | 0.50 | 0.8 |

(1)蛇纹石中涉及的可溶性金属氧化物有
(2)步骤①中涉及SiO2反应的离子方程式为
(3)滤渣
 的成分有
的成分有(4)步骤②中洗涤沉淀的方法是
(5)步骤③反应的化学方程式为
您最近一年使用:0次
2 . 某兴趣小组对化合物X开展探究实验:
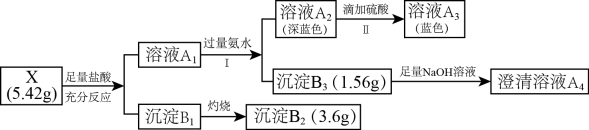
其中:化合物X有由4种元素组成;沉淀B2是工业生产玻璃的重要原料。
请回答:
(1)组成X的四种元素中除含O外,还有___________ (填元素符号)。
(2)在澄清溶液A4中通入过量CO2,产生沉淀的离子方程式为___________ 。
(3)步骤I中生成沉淀B3的离子方程式为___________ 。
(4)步骤II中溶液由深蓝色转变为蓝色的原因是___________ 。
(5)为进一步确定X的化学式,往溶液A1中通入足量的SO2,生成0.995g的白色沉淀(其中氯元素的质量分数为35.7%),在反应后的溶液中滴加BaCl2溶液,有白色沉淀生成。
①写出A1中通入SO2的离子反应方程式___________ 。
②确定X的化学式为___________ 。

其中:化合物X有由4种元素组成;沉淀B2是工业生产玻璃的重要原料。
请回答:
(1)组成X的四种元素中除含O外,还有
(2)在澄清溶液A4中通入过量CO2,产生沉淀的离子方程式为
(3)步骤I中生成沉淀B3的离子方程式为
(4)步骤II中溶液由深蓝色转变为蓝色的原因是
(5)为进一步确定X的化学式,往溶液A1中通入足量的SO2,生成0.995g的白色沉淀(其中氯元素的质量分数为35.7%),在反应后的溶液中滴加BaCl2溶液,有白色沉淀生成。
①写出A1中通入SO2的离子反应方程式
②确定X的化学式为
您最近一年使用:0次
3 . 硅是无机非金属材料的主角,硅的氧化物和硅酸盐占地壳质量的90%以上。
(1)写出地壳中含量最高的元素的符号:_______ 。
(2)写出通信中硅的氧化物的一种用途:_______ 。
(3)科学家用金属钠、四氯化碳和四氯化硅制得了碳化硅纳米棒,反应的化学方程式为 。
。
①该反应中Si元素的化合价为_______ 价。
②其中还原产物的化学式为_______ 。
③高温真空环境中,C与SiO2反应也可以生成SiC,写出该反应的化学方程式:_______ 。
(4)用Na2SiO3水溶液浸泡过的棉花不易燃烧,说明Na2SiO3溶液可以用作_______ ;设计简单实验比较醋酸与H2SiO3酸性的强弱:_______ 。
(1)写出地壳中含量最高的元素的符号:
(2)写出通信中硅的氧化物的一种用途:
(3)科学家用金属钠、四氯化碳和四氯化硅制得了碳化硅纳米棒,反应的化学方程式为
 。
。①该反应中Si元素的化合价为
②其中还原产物的化学式为
③高温真空环境中,C与SiO2反应也可以生成SiC,写出该反应的化学方程式:
(4)用Na2SiO3水溶液浸泡过的棉花不易燃烧,说明Na2SiO3溶液可以用作
您最近一年使用:0次



