2013·上海闵行·三模
1 . 钠及其化合物在生产和生活中有广泛的应用。例如:Na2O2在医院、潜水、高空飞行中用作供氧剂。
(1)制备Na2O2的反应为:4Na+O2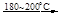 2Na2O 2Na2O +O2
2Na2O 2Na2O +O2 2Na2O2 。
2Na2O2 。
①实验测得某过氧化钠样品含有少量氧化钠杂质,其中钠、氧原子个数比为10︰9.5,该样品中Na2O2的纯度为_________ 。
②取上述过氧化钠样品7.64g放入烧杯中,加入足量水,搅拌,使固体完全溶解,冷却后,在容量瓶中配制成100mL溶液,则该溶液中OH-离子的物质的量浓度为______________ 。
(2)某同学为了检验引起光化学烟雾的气体成分(NO、CO、NO2、HCHO、CH3OH、CH4等),查阅资料得知:Na2O2+2NO→2NaNO2、Na2O2+2NO2→2NaNO3,于是取用a gM气体与b g 氧气混合后,用电火花不断引燃,充分反应后,气体通过足量Na2O2,Na2O2固体质量增加c g。
①若a=c,则M气体的成分可能含有__________________________________ 。
②若2a=c,则M气体可能是什么气体?通过计算回答______ 。
(1)制备Na2O2的反应为:4Na+O2
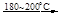 2Na2O 2Na2O +O2
2Na2O 2Na2O +O2 2Na2O2 。
2Na2O2 。①实验测得某过氧化钠样品含有少量氧化钠杂质,其中钠、氧原子个数比为10︰9.5,该样品中Na2O2的纯度为
②取上述过氧化钠样品7.64g放入烧杯中,加入足量水,搅拌,使固体完全溶解,冷却后,在容量瓶中配制成100mL溶液,则该溶液中OH-离子的物质的量浓度为
(2)某同学为了检验引起光化学烟雾的气体成分(NO、CO、NO2、HCHO、CH3OH、CH4等),查阅资料得知:Na2O2+2NO→2NaNO2、Na2O2+2NO2→2NaNO3,于是取用a gM气体与b g 氧气混合后,用电火花不断引燃,充分反应后,气体通过足量Na2O2,Na2O2固体质量增加c g。
①若a=c,则M气体的成分可能含有
②若2a=c,则M气体可能是什么气体?通过计算回答
您最近一年使用:0次
10-11高三·浙江杭州·阶段练习
2 . 科学家用NaNO3和Na2O在一定条件下化合制得晶体A,A由钠离子和某阴离子B构成,则:
(1)A的化学式为___________ ,
(2)A对CO2特别敏感,与CO2反应相当剧烈,生成两种常见的物质,该反应的化学方程式为:_________________ ;
(3)此外,科学家还制备了另一种钠盐D,其与A的组成元素完全相同,D中的阴离子与A中的阴离子表观形式相同(元素种类和原子个数均相同),但D中阴离子的结构中含有一个过氧键:-O-O- ,电导实验表明,同条件下其电导能力与NaCl相同,该阴离子的化学式为_________ ,其与水反应生成过氧化氢的离子方程式为______________________ ,该反应______ (填是或不是)氧化-还原反应。
(1)A的化学式为
(2)A对CO2特别敏感,与CO2反应相当剧烈,生成两种常见的物质,该反应的化学方程式为:
(3)此外,科学家还制备了另一种钠盐D,其与A的组成元素完全相同,D中的阴离子与A中的阴离子表观形式相同(元素种类和原子个数均相同),但D中阴离子的结构中含有一个过氧键:-O-O- ,电导实验表明,同条件下其电导能力与NaCl相同,该阴离子的化学式为
您最近一年使用:0次
3 . 将a mol Na溶于b g水中,a1 mol Na2O溶于b1g水中,a2 mol Na2O2溶于b2g水中,均能得到质量分数为8%的NaOH溶液。(已知:2Na2O2+ 2H2O ==4NaOH + O2↑)
(1)若a1∶a2=1,则b1=b2=____________ (2)若a=0.2,则b=______________
(3)若b=b1=b2,则a、a1和a2之间的关系式为_______________________________
(1)若a1∶a2=1,则b1=b2=
(3)若b=b1=b2,则a、a1和a2之间的关系式为
您最近一年使用:0次
4 . 钠是很活泼的金属,在空气中燃烧的产物是Na2O2。Na2O的制取一般可以通过下列两个反应完成:
反应①: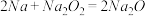
反应②: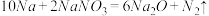
(1)分析以上两个反应,完成下表:
(2)按照绿色化学的原则,最理想的“原子经济”就是反应物的原子全部转化为所期望的最终产物,上述两个反应中满足“原子经济”要求的是____ (填序号)。
(3)欲将23g钠全部转化成Na2O,现按照反应:①进行反应,需先将一部分钠氧化成Na2O2,则被氧化成Na2O2的金属钠的物质的量为________ 。
(4)Na2O在空气中很容易进一步氧化成Na2O2。100g某Na2O样品(含Na2O2)中加入足量的水,生成5.6L气体(标准状况),则样品中Na2O的质量分数为_____ 。
反应①:
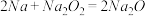
反应②:
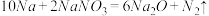
(1)分析以上两个反应,完成下表:
| 作氧化剂的元素(填元素符号) | 基本反应类型 | |
| 反应① | ||
| 反应② | 置换反应 |
(2)按照绿色化学的原则,最理想的“原子经济”就是反应物的原子全部转化为所期望的最终产物,上述两个反应中满足“原子经济”要求的是
(3)欲将23g钠全部转化成Na2O,现按照反应:①进行反应,需先将一部分钠氧化成Na2O2,则被氧化成Na2O2的金属钠的物质的量为
(4)Na2O在空气中很容易进一步氧化成Na2O2。100g某Na2O样品(含Na2O2)中加入足量的水,生成5.6L气体(标准状况),则样品中Na2O的质量分数为
您最近一年使用:0次
10-11高一上·山西太原·期中
5 . 将表面已部分被氧化为氧化钠的金属钠样品5.4g放入40g水中,在标准状况下放出1.12LH2。求:____
(1)产生H2的物质的量为多少?
(2)原混合物中金属钠的质量为多少克?
(3)若反应后溶液的体积为40mL,所得溶液的物质的量浓度为多少?
(1)产生H2的物质的量为多少?
(2)原混合物中金属钠的质量为多少克?
(3)若反应后溶液的体积为40mL,所得溶液的物质的量浓度为多少?
您最近一年使用:0次
6 . 在隔绝空气的条件下,某同学将一块部分被氧化的钠块用一张已除去氧化膜、并用针刺一些小孔的铝箔包好,然后放入盛满水且倒置于水槽中的容器内。待钠块反应完全后,在容器中仅收集到1.12 L氢气(标准状况),此时测得铝箔质量比反应前减少了0.27 g,水槽和容器内溶液的总体积为2.0 L,溶液中NaOH的浓度为0.050 mol·L-1(忽略溶液中离子的水解和溶解的氢气的量)。
(1)写出该实验中发生反应的化学方程式:_____________ _____________ _____________
(2)试通过计算确定该钠块中钠元素的质量分数为_________
(1)写出该实验中发生反应的化学方程式:
(2)试通过计算确定该钠块中钠元素的质量分数为
您最近一年使用:0次
2009-11-17更新
|
1624次组卷
|
3卷引用:2007年普通高等学校招生全国统一考试(江苏卷)化学试题



