解题方法
1 .  不稳定,受热易分解,现有2.96g未完全分解的碳酸氢钠样品,欲测定其分解率,将其完全溶于水制成溶液,然后向此溶液中缓慢滴加稀盐酸,并不断搅拌。溶液中有关离子的物质的量随盐酸加入的变化如图所示,则
不稳定,受热易分解,现有2.96g未完全分解的碳酸氢钠样品,欲测定其分解率,将其完全溶于水制成溶液,然后向此溶液中缓慢滴加稀盐酸,并不断搅拌。溶液中有关离子的物质的量随盐酸加入的变化如图所示,则
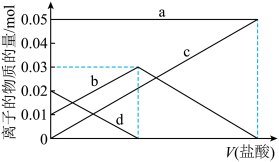
(1)a、d对应的离子分别是_______ (填离子符号);
(2)该样品中 的质量分数为
的质量分数为_______ ;(保留两位小数)
(3)原 的分解率为
的分解率为_______ 。
 不稳定,受热易分解,现有2.96g未完全分解的碳酸氢钠样品,欲测定其分解率,将其完全溶于水制成溶液,然后向此溶液中缓慢滴加稀盐酸,并不断搅拌。溶液中有关离子的物质的量随盐酸加入的变化如图所示,则
不稳定,受热易分解,现有2.96g未完全分解的碳酸氢钠样品,欲测定其分解率,将其完全溶于水制成溶液,然后向此溶液中缓慢滴加稀盐酸,并不断搅拌。溶液中有关离子的物质的量随盐酸加入的变化如图所示,则
(1)a、d对应的离子分别是
(2)该样品中
 的质量分数为
的质量分数为(3)原
 的分解率为
的分解率为
您最近一年使用:0次
解题方法
2 . 依据图像特点判断溶液溶质成分


若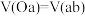 (即 (即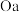 段与 段与 段消耗盐酸的体积相同) 段消耗盐酸的体积相同) | 溶液中的溶质为 | 涉及离子方程式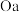 : : : : |
若 (即 (即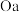 段消耗盐酸的体积大于 段消耗盐酸的体积大于 段消耗盐酸的体积) 段消耗盐酸的体积) | 溶液中的溶质为 | 涉及离子方程式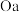 : : : : |
若 (即 (即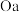 段消耗盐酸的体积小于 段消耗盐酸的体积小于 段消耗盐酸的体积) 段消耗盐酸的体积) | 溶液中的溶质为 | 涉及离子方程式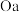 : : : : |
若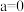 (即图像从原点开始) (即图像从原点开始) | 溶液中的溶质为 | 涉及离子方程式: |
您最近一年使用:0次
解题方法
3 . 碳捕集技术是减少二氧化碳排放的一种途径,其基本思路是将工业排放的二氧化碳分离出来,以某种方式封存或者进一步利用。二氧化碳可以作为气体肥料促进植物的光合作用,也可以作为原料生产可降解塑料。某工厂废气中含有大量二氧化碳,但是二氧化碳的收集和转运是个难题。请你设计操作简单、经济合理的方案,实现二氧化碳的收集和转运,并概括出你的设计思路________ 。
您最近一年使用:0次
解题方法
4 . 碳酸钠(Na2CO3)
(1)碳酸钠是白色固体,俗称_______ ,_______ 于水;电离方程式_______ 。
(2)实验探究-Na2CO3的性质
(3)Na2CO3溶液与酸的反应
①与足量盐酸反应:_______
②通入足量CO2:_______
(1)碳酸钠是白色固体,俗称
(2)实验探究-Na2CO3的性质
| 实验 | 现象 | 结论(或化学方程式) |
| 将澄清石灰水加入碳酸钠溶液中 | ||
| 将氯化钙溶液加入碳酸钠溶液中 | ||
| 测碳酸钠溶液pH | pH | 碳酸钠溶液呈 |
| 将沾有油污的铜片放入热的碳酸钠溶液中 | 碳酸钠溶液具有 |
①与足量盐酸反应:
②通入足量CO2:
您最近一年使用:0次
2022-08-17更新
|
292次组卷
|
2卷引用:课前-3.2.2 碳酸钠、碳酸氢钠-苏教版2020必修第一册
2022高一·全国·专题练习
5 . 仅用试管和胶头滴管,你能鉴别Na2CO3溶液和稀盐酸吗?若能,简述原理。
您最近一年使用:0次
2022高三·全国·专题练习
解题方法
6 . 如图进行实验,将a溶液逐渐加入盛b溶液的试管中,写出试管中观察到的现象及对应的离子方程式。


| a | b | 试管中现象 | 离子方程式 |
| Na2CO3 | 稀盐酸 | ||
| 稀盐酸 | Na2CO3 |
您最近一年使用:0次
7 . 在饱和碳酸钠溶液中加入稀盐酸,边加入边搅拌,最初无气体产生,溶液变浑浊,其原因是_______ ,化学反应方程式为_______ 。继续滴入稀盐酸有气体放出,溶液变澄清,其原因是_______ ,化学反应方程式为_______ 。
您最近一年使用:0次
解题方法
8 . 我国著名化学家侯德榜发明的“联合制碱法”的反应原理用化学方程式可简要表示为:
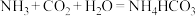 ,
,
 ;
;
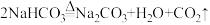 。
。
(1)纯碱属于___________ (填“酸”“碱”或“盐”)。
(2)检验碳酸氢钠中含有碳酸钠的方法是___________ 。
(3) ,请写出该反应能发生的原因
,请写出该反应能发生的原因_________ 。
(4)向含有碳酸钠和碳酸氢钠的溶液中逐滴滴加1 mol/L盐酸,产生标准状况下气体的体积与盐酸体积关系如图所示:
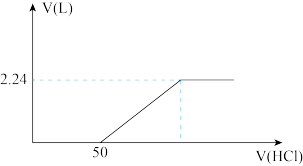
①逐滴滴加盐酸的过程中 物质的量变化趋势是
物质的量变化趋势是___________ ;
②上述混合溶液碳酸氢钠的物质的量是___________ 。
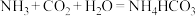 ,
, ;
;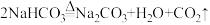 。
。(1)纯碱属于
(2)检验碳酸氢钠中含有碳酸钠的方法是
(3)
 ,请写出该反应能发生的原因
,请写出该反应能发生的原因(4)向含有碳酸钠和碳酸氢钠的溶液中逐滴滴加1 mol/L盐酸,产生标准状况下气体的体积与盐酸体积关系如图所示:

①逐滴滴加盐酸的过程中
 物质的量变化趋势是
物质的量变化趋势是②上述混合溶液碳酸氢钠的物质的量是
您最近一年使用:0次
2021-12-23更新
|
1279次组卷
|
4卷引用:广西河池市八校2021-2022学年高一上学期第二次联考化学试题
广西河池市八校2021-2022学年高一上学期第二次联考化学试题(已下线)专题36 碳酸钠质量分数测定的实验探究-2022年高考化学毕业班二轮热点题型归纳与变式演练(全国通用)(已下线)第二章《 海水中的重要元素----钠和氯》基础过关单元检测-【帮课堂】2022-2023学年高一化学同步精品讲义(人教版2019必修第一册)天津市外国语大学附属外国语学校2022~2023学年高一上学期阶段性检测化学试题
2021高三·全国·专题练习
解题方法
9 . 写出下列反应的离子方程式
(1)可溶性多元弱酸(或其酸酐)与碱溶液反应。
如CO2通入NaOH溶液中
①CO2少量____________
②CO2过量____________
(2)多元弱酸(或其酸酐)与更弱酸的盐溶液。
如CO2通入到NaAlO2溶液中
①NaAlO2过量:____________
②NaAlO2不足____________
(3)多元弱酸盐与强酸反应,
如Na2CO3溶液与稀盐酸
①盐酸不足:____________
②盐酸过量:____________
(4)铝盐溶液与强碱溶液
如AlCl3溶液和NaOH溶液反应
①AlCl3过量:____________
②NaOH过量:____________
(5)NaAlO2溶液与强酸的反应
如NaAlO2溶液与盐酸的反应
①NaAlO2过量:____________
②盐酸过量:____________
(1)可溶性多元弱酸(或其酸酐)与碱溶液反应。
如CO2通入NaOH溶液中
①CO2少量
②CO2过量
(2)多元弱酸(或其酸酐)与更弱酸的盐溶液。
如CO2通入到NaAlO2溶液中
①NaAlO2过量:
②NaAlO2不足
(3)多元弱酸盐与强酸反应,
如Na2CO3溶液与稀盐酸
①盐酸不足:
②盐酸过量:
(4)铝盐溶液与强碱溶液
如AlCl3溶液和NaOH溶液反应
①AlCl3过量:
②NaOH过量:
(5)NaAlO2溶液与强酸的反应
如NaAlO2溶液与盐酸的反应
①NaAlO2过量:
②盐酸过量:
您最近一年使用:0次



