名校
解题方法
1 . 食品工业经常使用 和
和 作膨松剂
作膨松剂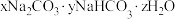 。室温下,向含3.07g某膨松剂试样的溶液中逐滴加入稀盐酸,反应过程中含碳元素微粒的物质的量随
。室温下,向含3.07g某膨松剂试样的溶液中逐滴加入稀盐酸,反应过程中含碳元素微粒的物质的量随 变化的图象如图所示。
变化的图象如图所示。 点溶液溶质的主要成分的化学式为
点溶液溶质的主要成分的化学式为___________ ;图中A点n(Na2CO3)=___________ mol。
(2)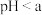 时发生反应的离子反应方程式为
时发生反应的离子反应方程式为___________ 。x:y:z=___________ 。
 和
和 作膨松剂
作膨松剂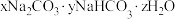 。室温下,向含3.07g某膨松剂试样的溶液中逐滴加入稀盐酸,反应过程中含碳元素微粒的物质的量随
。室温下,向含3.07g某膨松剂试样的溶液中逐滴加入稀盐酸,反应过程中含碳元素微粒的物质的量随 变化的图象如图所示。
变化的图象如图所示。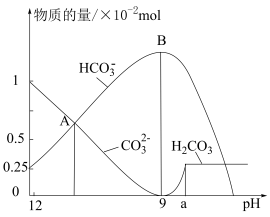
 点溶液溶质的主要成分的化学式为
点溶液溶质的主要成分的化学式为(2)
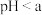 时发生反应的离子反应方程式为
时发生反应的离子反应方程式为
您最近一年使用:0次
名校
解题方法
2 . 现有一份 溶液,向其中通入一定量
溶液,向其中通入一定量 ,得到一份混合溶液,为测定溶液的成分,某小组同学做了以下实验:
,得到一份混合溶液,为测定溶液的成分,某小组同学做了以下实验:
Ⅰ.配制 的标准盐酸
的标准盐酸
实验室现有密度为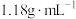 ,质量分数为36.5%的浓盐酸,若要配制
,质量分数为36.5%的浓盐酸,若要配制 标准盐酸,据此回答下列问题:
标准盐酸,据此回答下列问题:
(1)该浓盐酸的物质的量浓度为_____  ;应选用的容量瓶的规格为
;应选用的容量瓶的规格为_____ 。
(2)在配制稀盐酸溶液时,有如下操作,正确的操作顺序是_____ 。
A.用量筒量取浓盐酸注入烧杯中,再向烧杯中加入少量蒸馏水,慢慢搅动,使其混合均匀
B.用蒸馏水洗涤烧杯内壁及玻璃棒仪器各2~3次,将洗涤液全部注入容量瓶中,轻轻摇动容量瓶
C.盖好瓶塞,反复上下颠倒摇匀
D.将已恢复至室温的盐酸转移注入所选用的容量瓶中
E.用胶头滴管滴加蒸馏水,使溶液的凹液面恰好与容量瓶上的刻度线相切
F.继续往容量瓶中加蒸馏水,直到液面接近瓶颈上的刻度线1~2cm处
(3)若是定容时俯视容量瓶瓶颈上的刻度线会使所配制的溶液浓度_____ (填“偏低”“偏高”“无影响”,下同);容量瓶用蒸馏水洗净后,没烘干直接使用对实验的结果_____ 。
Ⅱ、测定混合溶液成分
向混合溶液中滴入上述配制的稀盐酸,滴入盐酸体积与产生气体体积(标准状况)如图所示:
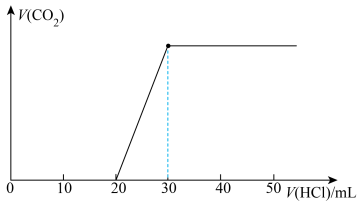
(4)混合溶液的溶质为_____ (填化学式)。
(5)原 溶液的物质的量浓度为
溶液的物质的量浓度为_____ 。
 溶液,向其中通入一定量
溶液,向其中通入一定量 ,得到一份混合溶液,为测定溶液的成分,某小组同学做了以下实验:
,得到一份混合溶液,为测定溶液的成分,某小组同学做了以下实验:Ⅰ.配制
 的标准盐酸
的标准盐酸实验室现有密度为
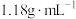 ,质量分数为36.5%的浓盐酸,若要配制
,质量分数为36.5%的浓盐酸,若要配制 标准盐酸,据此回答下列问题:
标准盐酸,据此回答下列问题:(1)该浓盐酸的物质的量浓度为
 ;应选用的容量瓶的规格为
;应选用的容量瓶的规格为(2)在配制稀盐酸溶液时,有如下操作,正确的操作顺序是
A.用量筒量取浓盐酸注入烧杯中,再向烧杯中加入少量蒸馏水,慢慢搅动,使其混合均匀
B.用蒸馏水洗涤烧杯内壁及玻璃棒仪器各2~3次,将洗涤液全部注入容量瓶中,轻轻摇动容量瓶
C.盖好瓶塞,反复上下颠倒摇匀
D.将已恢复至室温的盐酸转移注入所选用的容量瓶中
E.用胶头滴管滴加蒸馏水,使溶液的凹液面恰好与容量瓶上的刻度线相切
F.继续往容量瓶中加蒸馏水,直到液面接近瓶颈上的刻度线1~2cm处
(3)若是定容时俯视容量瓶瓶颈上的刻度线会使所配制的溶液浓度
Ⅱ、测定混合溶液成分
向混合溶液中滴入上述配制的稀盐酸,滴入盐酸体积与产生气体体积(标准状况)如图所示:

(4)混合溶液的溶质为
(5)原
 溶液的物质的量浓度为
溶液的物质的量浓度为
您最近一年使用:0次
3 . 根据实验现象书写方程式:
Ⅰ.某同学进行如下实验:
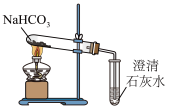
(1)加热NaHCO3的化学方程式:___________ 。
(2)一段时间后可以观察到澄清石灰水变浑浊,原因是___________ (用化学方程式表示,下同),再过一段时间后变澄清,发生的反应是___________ 。
Ⅱ.另一位同学进行如下实验:

(3)开始时,溶液的红色没有明显变化,也没有明显的气泡产生,反应的离子方程式为:___________ 。
(4)继续滴加盐酸,溶液的浅红色褪去,有大量气泡出现,反应的离子方程式为:___________ 。
Ⅲ.书写方程式:
(5)实验室检验Al3+的离子方程式:___________ 、___________ 。
(6)实验室制备Al(OH)3的离子方程式:___________ 、___________ (写出两种方法)
(7)除去Fe2O3中的Al2O3,可以选用的试剂是:___________ ,反应的离子方程式是___________ 。
(8)打磨过的铝条与NaOH反应的离子方程式:___________ 。
Ⅰ.某同学进行如下实验:

(1)加热NaHCO3的化学方程式:
(2)一段时间后可以观察到澄清石灰水变浑浊,原因是
Ⅱ.另一位同学进行如下实验:

(3)开始时,溶液的红色没有明显变化,也没有明显的气泡产生,反应的离子方程式为:
(4)继续滴加盐酸,溶液的浅红色褪去,有大量气泡出现,反应的离子方程式为:
Ⅲ.书写方程式:
(5)实验室检验Al3+的离子方程式:
(6)实验室制备Al(OH)3的离子方程式:
(7)除去Fe2O3中的Al2O3,可以选用的试剂是:
(8)打磨过的铝条与NaOH反应的离子方程式:
您最近一年使用:0次
名校
4 . 向含有10.6gNa2CO3的溶液中缓慢滴加盐酸,边滴加边搅拌。一开始没有气泡,一段时间后产生气泡。
(1)滴入含HCl___________ g的盐酸时,开始产生气泡。
(2)滴入盐酸至过量,共生成CO2___________ g。
(1)滴入含HCl
(2)滴入盐酸至过量,共生成CO2
您最近一年使用:0次
解题方法
5 . 完成下列问题:
(1)实验室金属钠应保存在___________ 中。钠长期置于空气中,最后形成的物质是___________ (填化学式)。
(2)金属钠在空气中燃烧生成 ,
, 是否属于碱性氧化物
是否属于碱性氧化物___________ (填“是”或“否”),检验其组成中所含阳离子的方法是:___________ 。 与足量的
与足量的 反应的化学方程式是
反应的化学方程式是___________ ,每消耗44克 ,
, 固体增重
固体增重___________ g。
(3) 固体中混有少量
固体中混有少量 固体,除杂方法是
固体,除杂方法是___________ ,化学方程式是___________ 。
(4) 和
和 在外观上相似,可用做家用洗涤剂,如清洗厨房用具的油污等。写出两种能区分二者的化学方法(产生不同化学现象)。
在外观上相似,可用做家用洗涤剂,如清洗厨房用具的油污等。写出两种能区分二者的化学方法(产生不同化学现象)。
方法一:___________ 。
方法二:___________ 。
(1)实验室金属钠应保存在
(2)金属钠在空气中燃烧生成
 ,
, 是否属于碱性氧化物
是否属于碱性氧化物 与足量的
与足量的 反应的化学方程式是
反应的化学方程式是 ,
, 固体增重
固体增重(3)
 固体中混有少量
固体中混有少量 固体,除杂方法是
固体,除杂方法是(4)
 和
和 在外观上相似,可用做家用洗涤剂,如清洗厨房用具的油污等。写出两种能区分二者的化学方法(产生不同化学现象)。
在外观上相似,可用做家用洗涤剂,如清洗厨房用具的油污等。写出两种能区分二者的化学方法(产生不同化学现象)。方法一:
方法二:
您最近一年使用:0次
解题方法
6 .  不稳定,受热易分解,现有2.96g未完全分解的碳酸氢钠样品,欲测定其分解率,将其完全溶于水制成溶液,然后向此溶液中缓慢滴加稀盐酸,并不断搅拌。溶液中有关离子的物质的量随盐酸加入的变化如图所示,则
不稳定,受热易分解,现有2.96g未完全分解的碳酸氢钠样品,欲测定其分解率,将其完全溶于水制成溶液,然后向此溶液中缓慢滴加稀盐酸,并不断搅拌。溶液中有关离子的物质的量随盐酸加入的变化如图所示,则
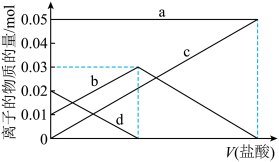
(1)a、d对应的离子分别是_______ (填离子符号);
(2)该样品中 的质量分数为
的质量分数为_______ ;(保留两位小数)
(3)原 的分解率为
的分解率为_______ 。
 不稳定,受热易分解,现有2.96g未完全分解的碳酸氢钠样品,欲测定其分解率,将其完全溶于水制成溶液,然后向此溶液中缓慢滴加稀盐酸,并不断搅拌。溶液中有关离子的物质的量随盐酸加入的变化如图所示,则
不稳定,受热易分解,现有2.96g未完全分解的碳酸氢钠样品,欲测定其分解率,将其完全溶于水制成溶液,然后向此溶液中缓慢滴加稀盐酸,并不断搅拌。溶液中有关离子的物质的量随盐酸加入的变化如图所示,则
(1)a、d对应的离子分别是
(2)该样品中
 的质量分数为
的质量分数为(3)原
 的分解率为
的分解率为
您最近一年使用:0次
7 . 为了使宇航员在飞船中得到一个稳定的、良好的生存环境,一般在飞船内安装盛有 颗粒的装置,它的用途是产生氧气。
颗粒的装置,它的用途是产生氧气。
(1)下列各组物质相互作用,生成物不随反应条件或反应物的用量变化而变化的是___________。
(2)写出 的电子式
的电子式___________ ,其晶体中存在的化学键类型是___________ 。
(3)下列关于 的叙述正确的是___________。
的叙述正确的是___________。
(4) 可用氢氧化钠溶液吸收,若将0.01mol的
可用氢氧化钠溶液吸收,若将0.01mol的 通入0.03mol的氢氧化钠溶液中,充分反应后,溶液中的溶质为
通入0.03mol的氢氧化钠溶液中,充分反应后,溶液中的溶质为___________ (写化学式)
(5)向(4)中反应后的溶液中逐滴加入0.1mol/L的盐酸,并及时振荡,以下哪张图符合产生的气体体积 与加入盐酸的体积
与加入盐酸的体积 的关系(其中B、C、D图中分别有
的关系(其中B、C、D图中分别有 、
、 、
、 )___________
)___________
 颗粒的装置,它的用途是产生氧气。
颗粒的装置,它的用途是产生氧气。(1)下列各组物质相互作用,生成物不随反应条件或反应物的用量变化而变化的是___________。
A.Na和 | B.NaOH和 | C. 和NaOH 和NaOH | D. 和HCl 和HCl |
 的电子式
的电子式(3)下列关于
 的叙述正确的是___________。
的叙述正确的是___________。A. 中正、负离子的个数比为1∶1 中正、负离子的个数比为1∶1 |
B. 分别与水及 分别与水及 反应产生相同量的 反应产生相同量的 时,需要水和 时,需要水和 的质量相等 的质量相等 |
C. 分别与水及 分别与水及 反应产生相同量的 反应产生相同量的 时,转移电子的物质的量相等 时,转移电子的物质的量相等 |
D. 的漂白原理与 的漂白原理与 的漂白原理相同 的漂白原理相同 |
 可用氢氧化钠溶液吸收,若将0.01mol的
可用氢氧化钠溶液吸收,若将0.01mol的 通入0.03mol的氢氧化钠溶液中,充分反应后,溶液中的溶质为
通入0.03mol的氢氧化钠溶液中,充分反应后,溶液中的溶质为(5)向(4)中反应后的溶液中逐滴加入0.1mol/L的盐酸,并及时振荡,以下哪张图符合产生的气体体积
 与加入盐酸的体积
与加入盐酸的体积 的关系(其中B、C、D图中分别有
的关系(其中B、C、D图中分别有 、
、 、
、 )___________
)___________A. | B. |
C. | D. |
您最近一年使用:0次
解题方法
8 . 依据图像特点判断溶液溶质成分


若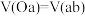 (即 (即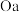 段与 段与 段消耗盐酸的体积相同) 段消耗盐酸的体积相同) | 溶液中的溶质为 | 涉及离子方程式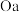 : : : : |
若 (即 (即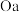 段消耗盐酸的体积大于 段消耗盐酸的体积大于 段消耗盐酸的体积) 段消耗盐酸的体积) | 溶液中的溶质为 | 涉及离子方程式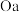 : : : : |
若 (即 (即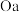 段消耗盐酸的体积小于 段消耗盐酸的体积小于 段消耗盐酸的体积) 段消耗盐酸的体积) | 溶液中的溶质为 | 涉及离子方程式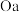 : : : : |
若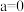 (即图像从原点开始) (即图像从原点开始) | 溶液中的溶质为 | 涉及离子方程式: |
您最近一年使用:0次
名校
9 . 某小组配制100mL 1.0mol/L  溶液并进行实验。
溶液并进行实验。
(1)配制溶液

①实验中使用玻璃棒的目的是___________ 。
②下列操作会导致最后所配溶液实际浓度比要求小的是___________ (填字母)
a.将烧杯中的溶液转移到容量瓶时不慎酒到容量瓶外
b.加水时不慎超过了刻度线,把液体倒出一些
c.干净的容量瓶未经干燥就用于配制溶液
(2)进行实验
①实现碳酸钠向碳酸氢钠转化的现象是___________ ,大量气泡产生时的离子方程式是___________ 。
②利用 可以实现碳酸钠向碳酸氢钠的转化,化学方程式是
可以实现碳酸钠向碳酸氢钠的转化,化学方程式是___________ 。
 溶液并进行实验。
溶液并进行实验。(1)配制溶液

①实验中使用玻璃棒的目的是
②下列操作会导致最后所配溶液实际浓度比要求小的是
a.将烧杯中的溶液转移到容量瓶时不慎酒到容量瓶外
b.加水时不慎超过了刻度线,把液体倒出一些
c.干净的容量瓶未经干燥就用于配制溶液
(2)进行实验
| 实验 | 现象 |
 | 开始时红色没有明显变化,也没有明显气泡产生; 继续滴加盐酸,当溶液红色明显变浅时,气泡也逐渐增多; 当溶液颜色变为浅红色,继续滴加盐酸,溶液浅红色褪去,有大量气泡产生。 |
②利用
 可以实现碳酸钠向碳酸氢钠的转化,化学方程式是
可以实现碳酸钠向碳酸氢钠的转化,化学方程式是
您最近一年使用:0次
2023-01-06更新
|
138次组卷
|
2卷引用:北京市顺义区2022-2023学年高一上学期期末考试化学试题
名校
解题方法
10 . 碳酸钠和碳酸氢钠是生活中常见的物质。
回答下列问题:
(1)向碳酸钠饱和溶液中通入 溶液变浑浊,反应的离子方程式为
溶液变浑浊,反应的离子方程式为___________ ;由此可知在相同温度下,碳酸钠的溶解度比碳酸氢钠的___________ (填“大”或“小”)。
(2)碳酸氢钠溶液与氢氧化钙溶液按溶质的物质的量之比为2∶1混合反应时,所得溶液中溶质为___________ (写化学式);检验所得溶液中溶质的阴离子的方法是___________ 。
(3)将27.4g 和
和 的混合物,加热到质量不再变化时,得残留固体21.2g.则原混合物中
的混合物,加热到质量不再变化时,得残留固体21.2g.则原混合物中 和
和 的质量之比为
的质量之比为___________ 。
(4)向碳酸钠溶液中逐滴滴入稀盐酸的微观示意图如下。由图可知向碳酸钠溶液中逐滴滴入稀盐酸时,实质是 依次与
依次与___________ 、___________ 发生反应(填微粒符号)。

回答下列问题:
(1)向碳酸钠饱和溶液中通入
 溶液变浑浊,反应的离子方程式为
溶液变浑浊,反应的离子方程式为(2)碳酸氢钠溶液与氢氧化钙溶液按溶质的物质的量之比为2∶1混合反应时,所得溶液中溶质为
(3)将27.4g
 和
和 的混合物,加热到质量不再变化时,得残留固体21.2g.则原混合物中
的混合物,加热到质量不再变化时,得残留固体21.2g.则原混合物中 和
和 的质量之比为
的质量之比为(4)向碳酸钠溶液中逐滴滴入稀盐酸的微观示意图如下。由图可知向碳酸钠溶液中逐滴滴入稀盐酸时,实质是
 依次与
依次与
您最近一年使用:0次



