名校
解题方法
1 . 食品工业经常使用 和
和 作膨松剂
作膨松剂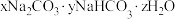 。室温下,向含3.07g某膨松剂试样的溶液中逐滴加入稀盐酸,反应过程中含碳元素微粒的物质的量随
。室温下,向含3.07g某膨松剂试样的溶液中逐滴加入稀盐酸,反应过程中含碳元素微粒的物质的量随 变化的图象如图所示。
变化的图象如图所示。 点溶液溶质的主要成分的化学式为
点溶液溶质的主要成分的化学式为___________ ;图中A点n(Na2CO3)=___________ mol。
(2)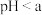 时发生反应的离子反应方程式为
时发生反应的离子反应方程式为___________ 。x:y:z=___________ 。
 和
和 作膨松剂
作膨松剂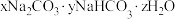 。室温下,向含3.07g某膨松剂试样的溶液中逐滴加入稀盐酸,反应过程中含碳元素微粒的物质的量随
。室温下,向含3.07g某膨松剂试样的溶液中逐滴加入稀盐酸,反应过程中含碳元素微粒的物质的量随 变化的图象如图所示。
变化的图象如图所示。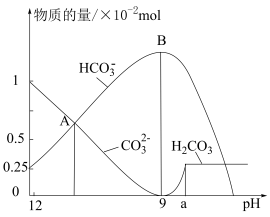
 点溶液溶质的主要成分的化学式为
点溶液溶质的主要成分的化学式为(2)
 时发生反应的离子反应方程式为
时发生反应的离子反应方程式为
您最近半年使用:0次
名校
解题方法
2 . 某实验小姐同学为了测定工业纯碱的纯度,进行了一系列实验。
(1)工业纯碱中常含有少量 杂质,检验是否含有氯化钠杂质的方法为
杂质,检验是否含有氯化钠杂质的方法为___________ 。
(2)使用滴定法测定炖碱的纯度,称量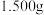 工业纯碱样品,溶解,用
工业纯碱样品,溶解,用 盐酸做标准液,逐滴滴入纯碱样品中,滴定过程中溶液
盐酸做标准液,逐滴滴入纯碱样品中,滴定过程中溶液 变化和生成
变化和生成 的量如图所示
的量如图所示 点前溶液中发生的反应
点前溶液中发生的反应___________ ,计算该工业纯碱样品的质量分数___________ 。(计算结果保留两位小数)
(1)工业纯碱中常含有少量
 杂质,检验是否含有氯化钠杂质的方法为
杂质,检验是否含有氯化钠杂质的方法为(2)使用滴定法测定炖碱的纯度,称量
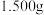 工业纯碱样品,溶解,用
工业纯碱样品,溶解,用 盐酸做标准液,逐滴滴入纯碱样品中,滴定过程中溶液
盐酸做标准液,逐滴滴入纯碱样品中,滴定过程中溶液 变化和生成
变化和生成 的量如图所示
的量如图所示 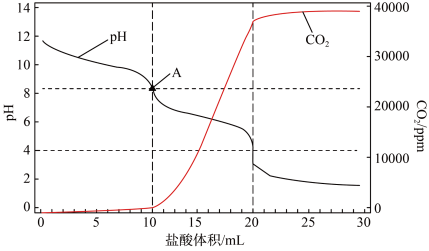
 点前溶液中发生的反应
点前溶液中发生的反应
您最近半年使用:0次
解题方法
3 . 完成下列离子方程式 。
(1)过氧化钠和水反应___________ ;
(2)稀H2SO4与Ba(OH)2溶液反应___________ ;
(3)稀盐酸和Na2CO3溶液反应___________ 。
(1)过氧化钠和水反应
(2)稀H2SO4与Ba(OH)2溶液反应
(3)稀盐酸和Na2CO3溶液反应
您最近半年使用:0次
名校
解题方法
4 . 现有一份 溶液,向其中通入一定量
溶液,向其中通入一定量 ,得到一份混合溶液,为测定溶液的成分,某小组同学做了以下实验:
,得到一份混合溶液,为测定溶液的成分,某小组同学做了以下实验:
Ⅰ.配制 的标准盐酸
的标准盐酸
实验室现有密度为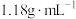 ,质量分数为36.5%的浓盐酸,若要配制
,质量分数为36.5%的浓盐酸,若要配制 标准盐酸,据此回答下列问题:
标准盐酸,据此回答下列问题:
(1)该浓盐酸的物质的量浓度为_____  ;应选用的容量瓶的规格为
;应选用的容量瓶的规格为_____ 。
(2)在配制稀盐酸溶液时,有如下操作,正确的操作顺序是_____ 。
A.用量筒量取浓盐酸注入烧杯中,再向烧杯中加入少量蒸馏水,慢慢搅动,使其混合均匀
B.用蒸馏水洗涤烧杯内壁及玻璃棒仪器各2~3次,将洗涤液全部注入容量瓶中,轻轻摇动容量瓶
C.盖好瓶塞,反复上下颠倒摇匀
D.将已恢复至室温的盐酸转移注入所选用的容量瓶中
E.用胶头滴管滴加蒸馏水,使溶液的凹液面恰好与容量瓶上的刻度线相切
F.继续往容量瓶中加蒸馏水,直到液面接近瓶颈上的刻度线1~2cm处
(3)若是定容时俯视容量瓶瓶颈上的刻度线会使所配制的溶液浓度_____ (填“偏低”“偏高”“无影响”,下同);容量瓶用蒸馏水洗净后,没烘干直接使用对实验的结果_____ 。
Ⅱ、测定混合溶液成分
向混合溶液中滴入上述配制的稀盐酸,滴入盐酸体积与产生气体体积(标准状况)如图所示:
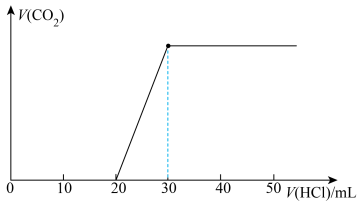
(4)混合溶液的溶质为_____ (填化学式)。
(5)原 溶液的物质的量浓度为
溶液的物质的量浓度为_____ 。
 溶液,向其中通入一定量
溶液,向其中通入一定量 ,得到一份混合溶液,为测定溶液的成分,某小组同学做了以下实验:
,得到一份混合溶液,为测定溶液的成分,某小组同学做了以下实验:Ⅰ.配制
 的标准盐酸
的标准盐酸实验室现有密度为
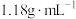 ,质量分数为36.5%的浓盐酸,若要配制
,质量分数为36.5%的浓盐酸,若要配制 标准盐酸,据此回答下列问题:
标准盐酸,据此回答下列问题:(1)该浓盐酸的物质的量浓度为
 ;应选用的容量瓶的规格为
;应选用的容量瓶的规格为(2)在配制稀盐酸溶液时,有如下操作,正确的操作顺序是
A.用量筒量取浓盐酸注入烧杯中,再向烧杯中加入少量蒸馏水,慢慢搅动,使其混合均匀
B.用蒸馏水洗涤烧杯内壁及玻璃棒仪器各2~3次,将洗涤液全部注入容量瓶中,轻轻摇动容量瓶
C.盖好瓶塞,反复上下颠倒摇匀
D.将已恢复至室温的盐酸转移注入所选用的容量瓶中
E.用胶头滴管滴加蒸馏水,使溶液的凹液面恰好与容量瓶上的刻度线相切
F.继续往容量瓶中加蒸馏水,直到液面接近瓶颈上的刻度线1~2cm处
(3)若是定容时俯视容量瓶瓶颈上的刻度线会使所配制的溶液浓度
Ⅱ、测定混合溶液成分
向混合溶液中滴入上述配制的稀盐酸,滴入盐酸体积与产生气体体积(标准状况)如图所示:

(4)混合溶液的溶质为
(5)原
 溶液的物质的量浓度为
溶液的物质的量浓度为
您最近半年使用:0次
2024高三·全国·专题练习
解题方法
5 . 下列关于Na2CO3和NaHCO3两种物质有关性质,说法正确的是______ 。
A.向Na2CO3和NaHCO3溶液中,滴入酚酞后溶液均变红,NaHCO3的颜色深
B.Na2CO3溶液中含有少量NaHCO3可用加热的方法除去
C.向等质量的Na2CO3和NaHCO3固体中加入足量稀盐酸,Na2CO3产生的气体较多
D.向盛有少量Na2CO3和NaHCO3的两支试管中各滴入几滴水,振荡后用温度计测量Na2CO3温度高于NaHCO3
E.热稳定性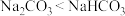
F.常温时水溶性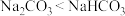
G.等浓度的溶液中滴入稀盐酸,放出气体的快慢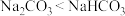
A.向Na2CO3和NaHCO3溶液中,滴入酚酞后溶液均变红,NaHCO3的颜色深
B.Na2CO3溶液中含有少量NaHCO3可用加热的方法除去
C.向等质量的Na2CO3和NaHCO3固体中加入足量稀盐酸,Na2CO3产生的气体较多
D.向盛有少量Na2CO3和NaHCO3的两支试管中各滴入几滴水,振荡后用温度计测量Na2CO3温度高于NaHCO3
E.热稳定性
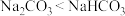
F.常温时水溶性
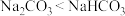
G.等浓度的溶液中滴入稀盐酸,放出气体的快慢
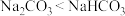
您最近半年使用:0次
6 . “侯氏制碱法”是我国化工专家侯德榜为世界制碱工业作出的突出贡献。请回答下列问题:
(1)某实验小组模拟“侯氏制碱法”制得的 晶体中可能含有少量
晶体中可能含有少量 、
、 等杂质,检验该晶体中是否含有氯离子杂质的操作方法是
等杂质,检验该晶体中是否含有氯离子杂质的操作方法是_______ 。
(2)常温下在10mL
 溶液中逐滴加入
溶液中逐滴加入
 溶液20mL,溶液中含碳元素的各种微粒的质量分数(纵轴)随溶液
溶液20mL,溶液中含碳元素的各种微粒的质量分数(纵轴)随溶液 变化的部分情况如图所示。根据图示回答下列问题:
变化的部分情况如图所示。根据图示回答下列问题:

①在同一溶液中, 、
、 、
、
_______ (填“能”或“不能”)大量共存。
②在滴加盐酸的过程中 的物质的量先增加后减少的原因是
的物质的量先增加后减少的原因是_______ ;_______ (请用离子方程式表示)。
(1)某实验小组模拟“侯氏制碱法”制得的
 晶体中可能含有少量
晶体中可能含有少量 、
、 等杂质,检验该晶体中是否含有氯离子杂质的操作方法是
等杂质,检验该晶体中是否含有氯离子杂质的操作方法是(2)常温下在10mL

 溶液中逐滴加入
溶液中逐滴加入
 溶液20mL,溶液中含碳元素的各种微粒的质量分数(纵轴)随溶液
溶液20mL,溶液中含碳元素的各种微粒的质量分数(纵轴)随溶液 变化的部分情况如图所示。根据图示回答下列问题:
变化的部分情况如图所示。根据图示回答下列问题:
①在同一溶液中,
 、
、 、
、
②在滴加盐酸的过程中
 的物质的量先增加后减少的原因是
的物质的量先增加后减少的原因是
您最近半年使用:0次
解题方法
7 . 按要求完成下列问题。
(1)过氧化钠可用于呼吸面具中作为氧气的来源。完成下列化学方程式: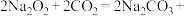
________ ;
(2)厨房中用的食盐和纯碱外观相似。某同学为区分这两种物质,各取少量置于玻璃杯中,滴加食醋,有气体产生的是___________ (填“食盐”或“纯碱”)。
(3)向盛有FeCl3溶液的试管中,滴加几滴KSCN溶液,溶液显___________ 色;
(4)Al2O3能溶于酸或强碱溶液生成盐和水,它是一种___________ (填“酸性”“碱性”或“两性”)氧化物;
(5)铁可以形成多种氧化物,其中常用作红色油漆和涂料的是___________ (填字母代号)。
A.FeO B.Fe2O3 C.Fe3O4
(1)过氧化钠可用于呼吸面具中作为氧气的来源。完成下列化学方程式:
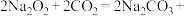
(2)厨房中用的食盐和纯碱外观相似。某同学为区分这两种物质,各取少量置于玻璃杯中,滴加食醋,有气体产生的是
(3)向盛有FeCl3溶液的试管中,滴加几滴KSCN溶液,溶液显
(4)Al2O3能溶于酸或强碱溶液生成盐和水,它是一种
(5)铁可以形成多种氧化物,其中常用作红色油漆和涂料的是
A.FeO B.Fe2O3 C.Fe3O4
您最近半年使用:0次
8 . 物质的分类是学习化学的一种重要方法,科学合理的分类对于系统掌握知识、提高学习效率、解决问题都有着重要的意义。
Ⅰ.厨房中有下列用品:

(1)水溶液呈碱性的是__________ (填序号)。
(2)写出②在水中的电离方程式__________ 。
(3)某同学将食盐、小苏打、纯碱划分为一类。该同学的分类依据为__________(填字母)。
(4)纯碱中含有少量 ,设计实验检验此混合物中的
,设计实验检验此混合物中的 、
、 。实验操作步骤:将少量混合物加水溶解后,分别置于两支试管中。向第一支试管中加入稀盐酸,可观察到产生无色气泡,该反应的离子方程式为
。实验操作步骤:将少量混合物加水溶解后,分别置于两支试管中。向第一支试管中加入稀盐酸,可观察到产生无色气泡,该反应的离子方程式为__________ ,说明溶液中存在 ;向第二支试管中先加入足量稀硝酸,再加入
;向第二支试管中先加入足量稀硝酸,再加入__________ 溶液,可观察到白色沉淀,说明溶液中存在 。
。
Ⅱ.如图是一种“纳米药物分子运输车”,该技术可提高肿瘤的治疗效果。
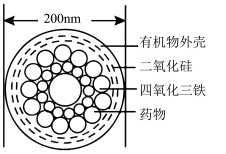
(5)“纳米药物分子车”分散于水中所得的分散系__________ 胶体(填“属于”或“不属于”)。
(6)“纳米药物分子车”的外壳属于有机物。酒精、蔗糖、冰醋酸这三种有机物中,属于电解质的是__________ 。
Ⅰ.厨房中有下列用品:

(1)水溶液呈碱性的是
(2)写出②在水中的电离方程式
(3)某同学将食盐、小苏打、纯碱划分为一类。该同学的分类依据为__________(填字母)。
| A.酸类 | B.盐类 | C.碱类 | D.含钠化合物 |
(4)纯碱中含有少量
 ,设计实验检验此混合物中的
,设计实验检验此混合物中的 、
、 。实验操作步骤:将少量混合物加水溶解后,分别置于两支试管中。向第一支试管中加入稀盐酸,可观察到产生无色气泡,该反应的离子方程式为
。实验操作步骤:将少量混合物加水溶解后,分别置于两支试管中。向第一支试管中加入稀盐酸,可观察到产生无色气泡,该反应的离子方程式为 ;向第二支试管中先加入足量稀硝酸,再加入
;向第二支试管中先加入足量稀硝酸,再加入 。
。Ⅱ.如图是一种“纳米药物分子运输车”,该技术可提高肿瘤的治疗效果。

(5)“纳米药物分子车”分散于水中所得的分散系
(6)“纳米药物分子车”的外壳属于有机物。酒精、蔗糖、冰醋酸这三种有机物中,属于电解质的是
您最近半年使用:0次
9 . 按要求填空
1.有下列物质:
①氢氧化钡;②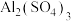 ;③液态 HCl;④稀硫酸;⑤二氧化碳;⑥铁;⑦碳酸钠;⑧蔗糖;⑨熔融氯化钠;⑩
;③液态 HCl;④稀硫酸;⑤二氧化碳;⑥铁;⑦碳酸钠;⑧蔗糖;⑨熔融氯化钠;⑩ .
.
请回答下列问题:
(1)属于电解质的有__________________________ (填序号)。
(2)②在水中的电离方程式为__________________________ 。
(3)请写出足量①与⑤反应的离子方程式______________________ 。
(4)请写出足量④与⑦反应的离子方程式______________________ 。
II.已知: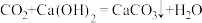 ,
,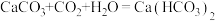 且
且 易溶于水,试根据如图所示装置回答下列问题:
易溶于水,试根据如图所示装置回答下列问题:
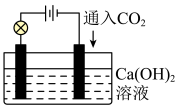
(5)通入 前,灯泡
前,灯泡_______ (填“亮”或“不亮”).
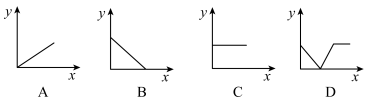
(6)下列四个图中,________ (填字线)能比较准确地反映出溶液的导电能力和通入 气体量的关系(x轴表示
气体量的关系(x轴表示 通入的量,y轴表示导电能力)
通入的量,y轴表示导电能力)
1.有下列物质:
①氢氧化钡;②
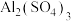 ;③液态 HCl;④稀硫酸;⑤二氧化碳;⑥铁;⑦碳酸钠;⑧蔗糖;⑨熔融氯化钠;⑩
;③液态 HCl;④稀硫酸;⑤二氧化碳;⑥铁;⑦碳酸钠;⑧蔗糖;⑨熔融氯化钠;⑩ .
.请回答下列问题:
(1)属于电解质的有
(2)②在水中的电离方程式为
(3)请写出足量①与⑤反应的离子方程式
(4)请写出足量④与⑦反应的离子方程式
II.已知:
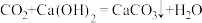 ,
,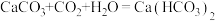 且
且 易溶于水,试根据如图所示装置回答下列问题:
易溶于水,试根据如图所示装置回答下列问题:
(5)通入
 前,灯泡
前,灯泡(6)下列四个图中,
 气体量的关系(x轴表示
气体量的关系(x轴表示 通入的量,y轴表示导电能力)
通入的量,y轴表示导电能力) 
您最近半年使用:0次
名校
10 . 某兴趣小组为探究 溶液的性质,需要
溶液的性质,需要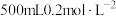 的
的 溶液。溶液的配制过程如图所示:
溶液。溶液的配制过程如图所示:
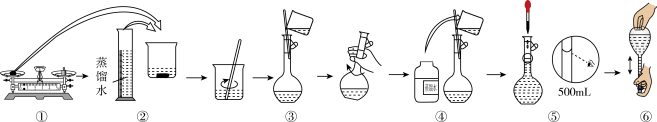
(1)配制过程中有一处明显错误为_____ (填序号)。
(2)若用 来配制溶液,需选择的玻璃仪器为量筒、玻璃棒、烧杯、
来配制溶液,需选择的玻璃仪器为量筒、玻璃棒、烧杯、__________________ 。
(3)用托盘天平称取
__________________  ;若所取的晶体已经有一部分失去了结晶水,则所配制的溶液浓度
;若所取的晶体已经有一部分失去了结晶水,则所配制的溶液浓度_____________ (填“偏大”、“偏小”或“无影响”)。
(4)若配制得到的 溶液中混有部分
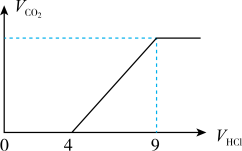
溶液中混有部分 ,为确定其纯度,取适量溶液,向溶液中滴加稀盐酸(边滴边振荡,假设生成的气体完全逸出),记录生成二氧化碳的体积和消耗盐酸的体积并绘制图像如图,
,为确定其纯度,取适量溶液,向溶液中滴加稀盐酸(边滴边振荡,假设生成的气体完全逸出),记录生成二氧化碳的体积和消耗盐酸的体积并绘制图像如图,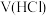 的体积为0-4阶段,发生反应的离子方程式为
的体积为0-4阶段,发生反应的离子方程式为_______________________ ;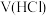 的体积为4-9阶段,发生反应的离子方程式为
的体积为4-9阶段,发生反应的离子方程式为_________ ;根据图计算可知,样品中纯碱和小苏打的物质的量之比为_____________ 。
 溶液的性质,需要
溶液的性质,需要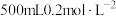 的
的 溶液。溶液的配制过程如图所示:
溶液。溶液的配制过程如图所示:
(1)配制过程中有一处明显错误为
(2)若用
 来配制溶液,需选择的玻璃仪器为量筒、玻璃棒、烧杯、
来配制溶液,需选择的玻璃仪器为量筒、玻璃棒、烧杯、(3)用托盘天平称取

 ;若所取的晶体已经有一部分失去了结晶水,则所配制的溶液浓度
;若所取的晶体已经有一部分失去了结晶水,则所配制的溶液浓度(4)若配制得到的
 溶液中混有部分
溶液中混有部分 ,为确定其纯度,取适量溶液,向溶液中滴加稀盐酸(边滴边振荡,假设生成的气体完全逸出),记录生成二氧化碳的体积和消耗盐酸的体积并绘制图像如图,
,为确定其纯度,取适量溶液,向溶液中滴加稀盐酸(边滴边振荡,假设生成的气体完全逸出),记录生成二氧化碳的体积和消耗盐酸的体积并绘制图像如图,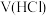 的体积为0-4阶段,发生反应的离子方程式为
的体积为0-4阶段,发生反应的离子方程式为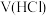 的体积为4-9阶段,发生反应的离子方程式为
的体积为4-9阶段,发生反应的离子方程式为
您最近半年使用:0次



