解题方法
1 . 阅读下列科普短文并填空:
海洋约占地球表面积的 ,其中水资源和其他化学资源具有巨大的开发潜力。海水中含有多种盐类,如
,其中水资源和其他化学资源具有巨大的开发潜力。海水中含有多种盐类,如 、
、 等。目前,通过海水晒盐可制得食盐晶体和苦卤,食盐精制后可制成饱和
等。目前,通过海水晒盐可制得食盐晶体和苦卤,食盐精制后可制成饱和 用以生产
用以生产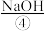 、
、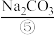 、
、 、
、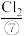 、
、 等,苦卤经过氯气氧化,热空气吹出、
等,苦卤经过氯气氧化,热空气吹出、 吸收等一系列操作可获得
吸收等一系列操作可获得 。海水淡化与化工生产、能源开发等相结合已经成为海水综合利用的重要方向。
。海水淡化与化工生产、能源开发等相结合已经成为海水综合利用的重要方向。
(1)上述标有序号的物质中属于电解质的是_______ (填序号,下同);属于非电解质的是_______ ;能导电的物质是_______ 。
(2)写出⑤溶于水的电离方程式:_______ 。将少量的⑤溶于装有50ml蒸馏水的烧杯中后,逐滴加入⑧观察到刚开始并没有出现气泡,一段时间后出现气泡,则出现该现象的原因是_______ ,写出对应反应的离子方程式:_______ ,_______ 。
海洋约占地球表面积的
 ,其中水资源和其他化学资源具有巨大的开发潜力。海水中含有多种盐类,如
,其中水资源和其他化学资源具有巨大的开发潜力。海水中含有多种盐类,如 、
、 等。目前,通过海水晒盐可制得食盐晶体和苦卤,食盐精制后可制成饱和
等。目前,通过海水晒盐可制得食盐晶体和苦卤,食盐精制后可制成饱和 用以生产
用以生产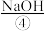 、
、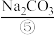 、
、 、
、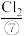 、
、 等,苦卤经过氯气氧化,热空气吹出、
等,苦卤经过氯气氧化,热空气吹出、 吸收等一系列操作可获得
吸收等一系列操作可获得 。海水淡化与化工生产、能源开发等相结合已经成为海水综合利用的重要方向。
。海水淡化与化工生产、能源开发等相结合已经成为海水综合利用的重要方向。(1)上述标有序号的物质中属于电解质的是
(2)写出⑤溶于水的电离方程式:
您最近一年使用:0次
解题方法
2 . 欲除去下列物质中的少量杂质,请填写所用方法及反应的化学方程式:
(1)Na2CO3固体中的NaHCO3:方法是_______ ,反应方程式为_______ 。
(2)NaCl溶液中的Na2CO3:方法是_______ ,反应方程式为_______ 。
(3)NaOH溶液中的Na2CO3:方法是_______ ,反应方程式为_______ 。
(1)Na2CO3固体中的NaHCO3:方法是
(2)NaCl溶液中的Na2CO3:方法是
(3)NaOH溶液中的Na2CO3:方法是
您最近一年使用:0次
3 . (1)标出下列微粒中划线元素的化合价。
①FeO___
②KClO3___
③Na2O2___
④H2S___
⑤NH
___
⑥MnO
___
(2)写出下列反应的化学方程式。
①金属铝与稀硫酸反应:___________
②氧化铁与稀盐酸反应:___________
③少量二氧化碳通入澄清石灰水:___________
④碳酸钠溶液与稀盐酸反应:___________
①FeO
②KClO3
③Na2O2
④H2S
⑤NH

⑥MnO

(2)写出下列反应的化学方程式。
①金属铝与稀硫酸反应:
②氧化铁与稀盐酸反应:
③少量二氧化碳通入澄清石灰水:
④碳酸钠溶液与稀盐酸反应:
您最近一年使用:0次
解题方法
4 . 按要求写出下列反应的方程式。
(1)Na2CO3溶液与足量稀盐酸的化学方程式:___________ ;
(2)BaCl2溶液与Na2SO4溶液的离子方程式:___________ ;
(3)制备漂白液的化学方程式为:___________ 。
(1)Na2CO3溶液与足量稀盐酸的化学方程式:
(2)BaCl2溶液与Na2SO4溶液的离子方程式:
(3)制备漂白液的化学方程式为:
您最近一年使用:0次
名校
解题方法
5 . 某小组探究Na2CO3和NaHCO3的性质,实验步骤及记录如下:
Ⅰ.分别向盛有0.5 g Na2CO3固体、0.5 g NaHCO3固体的烧杯中加入10 mL水(20 ℃),搅拌,测量温度为T1;
Ⅱ.静置恒温后测量温度为T2;
Ⅲ.分别加入10 mL 密度约为1.1 g·mL-120%的盐酸(20 ℃),搅拌,测量温度T3。
得到下表1的数据:
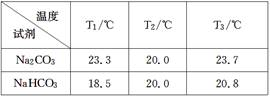
回答下列问题:
(1)Na2CO3溶于水显碱性,其原因是______________________ (用离子方程式表示)。
(2)根据试题后的附表判断:步骤Ⅰ中Na2CO3、NaHCO3固体分别是全部溶解还是部分溶解____________________________________ 。
(3)分析表1的数据得出:Na2CO3固体溶于水________ ,NaHCO3固体溶于水________ (填“放热”或“吸热”)。
(4)甲同学分析上述数据得出:Na2CO3和NaHCO3与盐酸反应都是放热反应。
乙同学认为应该增加一个实验,并补做如下实验:向盛有10 mL水(20 ℃)的烧杯中加入10 mL________ ,搅拌,测量温度为22.2 ℃。
(5)结合上述探究,下列说法正确的是________ 。
A.NaHCO3与盐酸的反应是吸热反应
B.不能用稀盐酸鉴别Na2CO3和NaHCO3固体
C.Na2CO3、NaHCO3固体与稀盐酸反应的能量变化还与物质的溶解等因素有关
(6)丙同学为测定一份NaHCO3和Na2CO3混合固体中NaHCO3的纯度,称取m1g混合物,加热至质量不变时,称其质量为m2g,则原混合物中NaHCO3的质量分数为________ (用代数式表示)。
附表:溶解度表
 .
.
Ⅰ.分别向盛有0.5 g Na2CO3固体、0.5 g NaHCO3固体的烧杯中加入10 mL水(20 ℃),搅拌,测量温度为T1;
Ⅱ.静置恒温后测量温度为T2;
Ⅲ.分别加入10 mL 密度约为1.1 g·mL-120%的盐酸(20 ℃),搅拌,测量温度T3。
得到下表1的数据:

回答下列问题:
(1)Na2CO3溶于水显碱性,其原因是
(2)根据试题后的附表判断:步骤Ⅰ中Na2CO3、NaHCO3固体分别是全部溶解还是部分溶解
(3)分析表1的数据得出:Na2CO3固体溶于水
(4)甲同学分析上述数据得出:Na2CO3和NaHCO3与盐酸反应都是放热反应。
乙同学认为应该增加一个实验,并补做如下实验:向盛有10 mL水(20 ℃)的烧杯中加入10 mL
(5)结合上述探究,下列说法正确的是
A.NaHCO3与盐酸的反应是吸热反应
B.不能用稀盐酸鉴别Na2CO3和NaHCO3固体
C.Na2CO3、NaHCO3固体与稀盐酸反应的能量变化还与物质的溶解等因素有关
(6)丙同学为测定一份NaHCO3和Na2CO3混合固体中NaHCO3的纯度,称取m1g混合物,加热至质量不变时,称其质量为m2g,则原混合物中NaHCO3的质量分数为
附表:溶解度表
 .
.
您最近一年使用:0次
2018-05-25更新
|
514次组卷
|
5卷引用:云南省文山州2018届高三毕业生复习统一检测理综化学试题
云南省文山州2018届高三毕业生复习统一检测理综化学试题2015届北京市石景山区高三上学期期末考试化学试卷2016届山东省德州中学高三上学期1月月考化学试卷(已下线)2018年高考题及模拟题汇编 专题13 元素及其化合物知识的综合应用河北省安平中学2021-2022学年高三上学期第二次月考化学试题



