1 . 某化学小组欲测定一份长期放置的补铁药品(有效成分是琥珀酸亚铁,化学式为FeC4H4O4)是否已变质,实验如下:
Ⅰ.取补铁药样品10.00g,碾碎,溶于100.0mL稀盐酸中,过滤,滤液呈浅黄绿色;
Ⅱ.取少量滤液,滴加KSCN溶液,溶液变为浅红色,再滴入3滴H2O2溶液,溶液红色加深;
Ⅲ.准确量取I中滤液20.00mL,加入足量H2O2溶液,再加入足量NaOH溶液,过滤、洗涤、常温晾干,获得Fe(OH)3固体0.642g;
Ⅳ.再准确量取I中滤液20.00mL于大试管中,加入1.00g铜粉,用胶塞塞紧试管口,充分振荡后过滤,最后得到干燥的铜粉0.936g。
(1)I中琥珀酸亚铁与稀盐酸反应生成FeCl2和琥珀酸(分子式为C4H6O4),说明酸性:C4H6O4_______ HCl(填“>”或“<”)。
(2)用离子方程式解释II中实验现象产生的原因:_______ 、Fe3++3SCN-=Fe(SCN)3。
(3)IV中发生反应的离子方程式为_______ 。
(4)该补铁药中琥珀酸亚铁变质程度为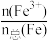 ×100%=
×100%=_______ (保留3位有效数字)。
(5)IV中溶液与铜粉反应时必须使用胶塞塞紧试管口,原因是_______ 。
Ⅰ.取补铁药样品10.00g,碾碎,溶于100.0mL稀盐酸中,过滤,滤液呈浅黄绿色;
Ⅱ.取少量滤液,滴加KSCN溶液,溶液变为浅红色,再滴入3滴H2O2溶液,溶液红色加深;
Ⅲ.准确量取I中滤液20.00mL,加入足量H2O2溶液,再加入足量NaOH溶液,过滤、洗涤、常温晾干,获得Fe(OH)3固体0.642g;
Ⅳ.再准确量取I中滤液20.00mL于大试管中,加入1.00g铜粉,用胶塞塞紧试管口,充分振荡后过滤,最后得到干燥的铜粉0.936g。
(1)I中琥珀酸亚铁与稀盐酸反应生成FeCl2和琥珀酸(分子式为C4H6O4),说明酸性:C4H6O4
(2)用离子方程式解释II中实验现象产生的原因:
(3)IV中发生反应的离子方程式为
(4)该补铁药中琥珀酸亚铁变质程度为
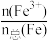 ×100%=
×100%=(5)IV中溶液与铜粉反应时必须使用胶塞塞紧试管口,原因是
您最近一年使用:0次
2023-08-26更新
|
169次组卷
|
5卷引用:山西省2023-2024学年高三上学期10月月考化学试题



