1 . 用下列仪器或装置(部分夹持装置略),能达到相应实验目的的是
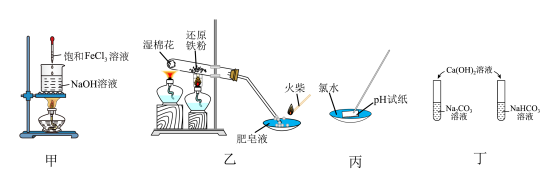

A.甲装置:制备 胶体 胶体 |
| B.乙装置:验证铁与水蒸气反应生成氢气 |
C.丙装置:用 试纸测定氯水的 试纸测定氯水的 |
D.丁装置:鉴别 溶液和 溶液和 溶液 溶液 |
您最近一年使用:0次
解题方法
2 . 下列实验中,利用图中装置不能达到实验目的的是
选项 | A | B | C | D |
装置 | 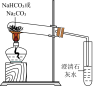 | 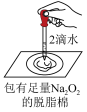 | 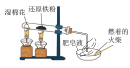 | 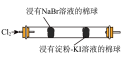 |
目的 | 鉴别碳酸钠和碳酸氢钠 | 证明 与水反应放热 与水反应放热 | 验证铁粉与水蒸气的反应 | 证明氧化性: |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
3 . 在一定条件下,用普通铁粉和水蒸气反应,可以得到铁的氧化物,该氧化物又可以经此反应的逆反应,生成颗粒很细的铁粉。某校化学小组利用下图所列装置进行铁与水反应的实验,并利用产物进一步与四氧化三铁反应制取铁粉。(装置中的铁架台、铁夹等必要的夹持仪器在图中均已略去)
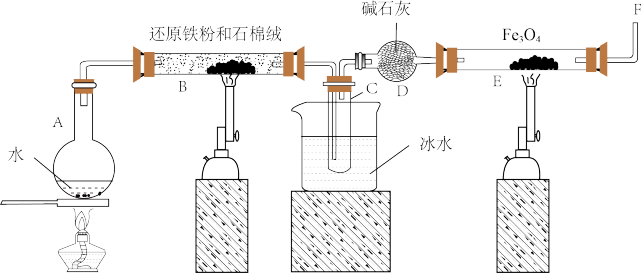
(1)烧瓶A中常加入碎瓷片,其作用是___________________ ,小试管C的作用是______________________________ 。
(2)为了安全,在E管中的反应发生前,在F出口处必须_________________ ,E管中的反应开始后,在F出口处应______________________ 。
(3)反应3Fe+4H2O(g) Fe3O4+4H2在一定条件下实际上为可逆反应,本实验中是如何实现Fe向Fe3O4的转变的?试用化学平衡移动原理加以解释
Fe3O4+4H2在一定条件下实际上为可逆反应,本实验中是如何实现Fe向Fe3O4的转变的?试用化学平衡移动原理加以解释_____________________ 。
(4)停止反应,待B管冷却后,取其中固体加入过量稀盐酸,充分反应后过滤。简述证明滤液中含有Fe3+的实验操作及现象______________________ 。
(5)若E管中反应按以下两步进行:Fe3O4+H2 3FeO+H2O,FeO+H2
3FeO+H2O,FeO+H2 Fe+H2O,假设实验开始时E管中的Fe3O4为23.2 g,反应一段时间后停止实验,冷却后取出其中固体干燥后称量,其质量变为20 g。通过计算分析其组成可能为
Fe+H2O,假设实验开始时E管中的Fe3O4为23.2 g,反应一段时间后停止实验,冷却后取出其中固体干燥后称量,其质量变为20 g。通过计算分析其组成可能为________ (填序号)
①Fe ②Fe和Fe3O4 ③FeO和Fe3O4④Fe和FeO ⑤Fe、FeO和Fe3O4
用此20 g固体与铝粉在一定条件下进行铝热反应,最多可消耗铝粉________ g。(不考虑空气中的成分参与反应)

(1)烧瓶A中常加入碎瓷片,其作用是
(2)为了安全,在E管中的反应发生前,在F出口处必须
(3)反应3Fe+4H2O(g)
 Fe3O4+4H2在一定条件下实际上为可逆反应,本实验中是如何实现Fe向Fe3O4的转变的?试用化学平衡移动原理加以解释
Fe3O4+4H2在一定条件下实际上为可逆反应,本实验中是如何实现Fe向Fe3O4的转变的?试用化学平衡移动原理加以解释(4)停止反应,待B管冷却后,取其中固体加入过量稀盐酸,充分反应后过滤。简述证明滤液中含有Fe3+的实验操作及现象
(5)若E管中反应按以下两步进行:Fe3O4+H2
 3FeO+H2O,FeO+H2
3FeO+H2O,FeO+H2 Fe+H2O,假设实验开始时E管中的Fe3O4为23.2 g,反应一段时间后停止实验,冷却后取出其中固体干燥后称量,其质量变为20 g。通过计算分析其组成可能为
Fe+H2O,假设实验开始时E管中的Fe3O4为23.2 g,反应一段时间后停止实验,冷却后取出其中固体干燥后称量,其质量变为20 g。通过计算分析其组成可能为①Fe ②Fe和Fe3O4 ③FeO和Fe3O4④Fe和FeO ⑤Fe、FeO和Fe3O4
用此20 g固体与铝粉在一定条件下进行铝热反应,最多可消耗铝粉
您最近一年使用:0次
解题方法
4 . 喷泉是一种常见的现象,其产生的原理是存在压强差。

试回答下列问题:
(1)实验室制取氨气的化学方程式为________ 。
①用图A装置进行喷泉实验,上部烧瓶已充满干燥的氨气,引发喷泉的操作是_______ 。
②利用图B装置引发喷泉的操作是___________ 。
(2)利用图C装置,在锥形瓶中分别加入足量的下列物质,反应后可能产生喷泉的有______ 。
A. 与稀盐酸 B.
与稀盐酸 B. 与稀硫酸
与稀硫酸
C. 与稀硝酸 D.
与稀硝酸 D. 溶液与
溶液与 溶液
溶液
(3)在图D装置的锥形瓶中加入乙醇,瓶外放一水槽,水槽中加入冷水后,再加入足量的下列物质,结果也形成了喷泉,水槽中加入的物质可能是_____ 。
A 浓硫酸 B 食盐 C 硝酸钾 D 硫酸铜
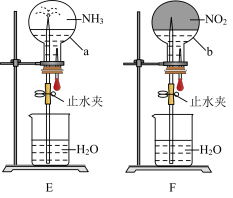
(4)同温同压下,两个等体积的干燥圆底烧瓶中分别充满 和
和 ,进行喷泉实验如图E、F所示,经充分反应后,发现烧瓶a中充满液体,b中有
,进行喷泉实验如图E、F所示,经充分反应后,发现烧瓶a中充满液体,b中有 体积的液体,则两烧瓶内溶质的物质的量浓度的关系是
体积的液体,则两烧瓶内溶质的物质的量浓度的关系是_______ 。
A.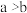 B.
B. C.
C. D.不能确定
D.不能确定

试回答下列问题:
(1)实验室制取氨气的化学方程式为
①用图A装置进行喷泉实验,上部烧瓶已充满干燥的氨气,引发喷泉的操作是
②利用图B装置引发喷泉的操作是
(2)利用图C装置,在锥形瓶中分别加入足量的下列物质,反应后可能产生喷泉的有
A.
 与稀盐酸 B.
与稀盐酸 B. 与稀硫酸
与稀硫酸C.
 与稀硝酸 D.
与稀硝酸 D. 溶液与
溶液与 溶液
溶液(3)在图D装置的锥形瓶中加入乙醇,瓶外放一水槽,水槽中加入冷水后,再加入足量的下列物质,结果也形成了喷泉,水槽中加入的物质可能是
A 浓硫酸 B 食盐 C 硝酸钾 D 硫酸铜
(4)同温同压下,两个等体积的干燥圆底烧瓶中分别充满
 和
和 ,进行喷泉实验如图E、F所示,经充分反应后,发现烧瓶a中充满液体,b中有
,进行喷泉实验如图E、F所示,经充分反应后,发现烧瓶a中充满液体,b中有 体积的液体,则两烧瓶内溶质的物质的量浓度的关系是
体积的液体,则两烧瓶内溶质的物质的量浓度的关系是
A.
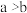 B.
B. C.
C. D.不能确定
D.不能确定
您最近一年使用:0次
2020-09-16更新
|
322次组卷
|
2卷引用:山西省运城市2019-2020学年高一上学期期末调研测试化学试题
名校
解题方法
5 . 工业上常用铁质容器盛装冷浓硫酸。为研究铁质材料与热浓硫酸的反应,某学习小组进行了以下探究活动:
(1)将已去除表面氧化物的铁钉(碳素钢)放入冷浓硫酸中,10分钟后移入硫酸铜溶液中,片刻后取出观察,铁钉表面无明显变化,其原因是___ 。
(2)另称取铁钉6.0g放入15.0ml浓硫酸中,加热,充分应后得到溶液X并收集到气体Y。
①甲同学认为X中除Fe3+外还可能含有Fe2+,若要确认其中的Fe2+,应选用___ (选填序号)。
a.KSCN溶液和氯水 b.K3Fe(CN)6溶液 c.浓氨水 d.酸性KMnO4溶液
②乙同学取336ml(标准状况)气体Y通入足量溴水中,发生反应:SO2+Br2+2H2O=2HBr+H2SO4,然后加入足量BaCl2溶液,经适当操作后得干燥固体2.33g。由此推知气体Y中SO2的体积分数为___ 。分析上述实验中SO2体积分数的结果,丙同学认为气体Y中还可能含有H2和Q气体(Q不考虑水蒸气)。为此设计了下列探究实验装置(图中夹持仪器省略)。
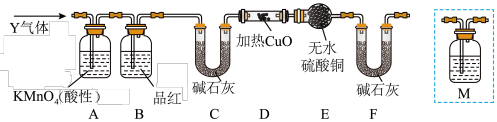
(3)装置B中试剂的作用是___ 。
(4)如果气体Y中含有H2,预计实验现象应是___ 。
(5)认为气体Y中还含有Q的理由是___ (用化学方程式表示)。
(6)为确认Q的存在,需在装置中添加M于___ (选填序号)。
a.A之前 b.A-B间 c.B-C间 d.C-D间
(1)将已去除表面氧化物的铁钉(碳素钢)放入冷浓硫酸中,10分钟后移入硫酸铜溶液中,片刻后取出观察,铁钉表面无明显变化,其原因是
(2)另称取铁钉6.0g放入15.0ml浓硫酸中,加热,充分应后得到溶液X并收集到气体Y。
①甲同学认为X中除Fe3+外还可能含有Fe2+,若要确认其中的Fe2+,应选用
a.KSCN溶液和氯水 b.K3Fe(CN)6溶液 c.浓氨水 d.酸性KMnO4溶液
②乙同学取336ml(标准状况)气体Y通入足量溴水中,发生反应:SO2+Br2+2H2O=2HBr+H2SO4,然后加入足量BaCl2溶液,经适当操作后得干燥固体2.33g。由此推知气体Y中SO2的体积分数为

(3)装置B中试剂的作用是
(4)如果气体Y中含有H2,预计实验现象应是
(5)认为气体Y中还含有Q的理由是
(6)为确认Q的存在,需在装置中添加M于
a.A之前 b.A-B间 c.B-C间 d.C-D间
您最近一年使用:0次
6 . 用下图装置(夹持、加热装置已略)进行实验,有②中现象,不能证实①中反应发生的是( )
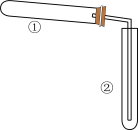

| ①中实验 | ②中现象 | |
| A | 铁粉与水蒸气加热 | 肥皂水冒泡 |
| B | 加热NH4Cl和Ca(OH)2混合物 | 酚酞溶液变红 |
| C | NaHCO3固体受热分解 | 澄清石灰水变浑浊 |
| D | 石蜡油在碎瓷片上受热分解 | Br2的CCl4溶液褪色 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2019-01-30更新
|
3245次组卷
|
8卷引用:山西省太原市第五十六中学2021-2022学年高三上学期第一次月考化学试题
7 . 下列有关化学图象表现的内容错误的是
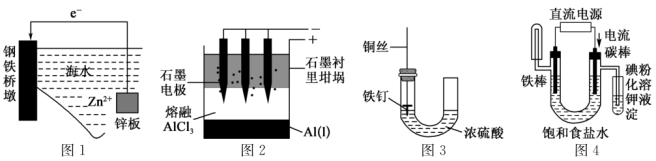

| A.图1表示牺牲阳极法 |
B.图2表示电解熔融 制备 制备 |
| C.图3所示装置中的铁钉几乎没被腐蚀 |
D.图4能验证 溶液(含酚酞)的电解产物 溶液(含酚酞)的电解产物 |
您最近一年使用:0次
2021-12-30更新
|
505次组卷
|
3卷引用:山西省运城市教育发展联盟2021-2022学年高二上学期12月月考化学试题
名校
解题方法
8 . 某同学看到“利用零价铁还原NO3-脱除地下水中硝酸盐”的相关资料后,利用如下装置探究铁粉与KNO3溶液的反应。实验步骤及现象如下:

(1)通入N2并保持后续反应均在N2氛围中进行的实验目的是______________________________ 。
(2)白色物质是__________ ,用化学方程式解释其变为红褐色的原因:____________________ 。
(3)为了探究滤液的成分,该同学进一步设计了下述实验:
(i)根据以上实验现象,可以判断滤液中存在____________________ 离子。
(ii)步骤2中滴加稀硫酸后溶液会由浅绿色变成红色,请用离子方程式解释其原因____________________ 。

| 实验步骤 | 实验现象 |
| 1、打开弹簧夹,缓慢通入N2 | |
| 2、加入pH为2.5的0.01mol/L酸性KNO3溶液100mL | 铁粉部分溶解,溶液呈浅绿色; 铁粉不再溶解后,剩余铁粉表面出现少量白色物质附着。 |
| 3、反应停止后,拔掉橡胶塞,将圆底烧瓶取下 | 烧瓶内气体的颜色没有发生变化。 |
| 4、将剩余固体过滤 | 表面的白色物质变为红褐色。 |
(2)白色物质是
(3)为了探究滤液的成分,该同学进一步设计了下述实验:
| 实验步骤 | 实验现象 |
| 1、取部分滤液于试管中,向其中加入KSCN溶液 | 溶液液无变化 |
| 2、将上述溶液分为两份,一份中滴入氯气;另一份中滴加稀硫酸 | 两份溶液均变为红色 |
| 3、另取部分滤液于试管中,向其中加入浓NaOH溶液并加热,在试管口放置湿润的红色石蕊试纸。 | 有气体生成,该气体使红色石蕊试纸变蓝。 |
(ii)步骤2中滴加稀硫酸后溶液会由浅绿色变成红色,请用离子方程式解释其原因
您最近一年使用:0次
2017-08-31更新
|
509次组卷
|
5卷引用:山西省太原师范学院附属中学、太原市师苑中学校2021-2022学年高一下学期3月月考化学试题
山西省太原师范学院附属中学、太原市师苑中学校2021-2022学年高一下学期3月月考化学试题北京市师范大学附属实验中学2015-2016学年高一下学期期末考试化学试题(已下线)3.3.3 硝酸的性质 人类活动对氮循环和环境的影响练习(1)——《高中新教材同步备课》(鲁科版 必修第一册)河北省三河市第一中学2020-2021学年高一下学期第一次阶段考化学试题广东省佛山市顺德区容山中学2022-2023学年高一下学期3月月考化学试题
解题方法
9 . 某实验小组利用如图所示装置进行“铁与水蒸气反应”的实验,并利用反应产物进一步制备FeCl3·6H2O晶体(夹持装置及尾气处理装置均已略去)。

请回答下列问题:
(1)装置B中发生反应的化学方程式是_______ 。
(2)装置B中石棉绒的作用是_______ 。
(3)E中出现的现象是_______ 。
(4)该小组把B中反应后的产物加入足量的盐酸中,用该溶液制备FeCl3·6H2O晶体。该实验小组同学用上述试剂没有检测到Fe3+,用离子方程式解释溶液中不存在Fe3+可能的原因:_______ 。
(5)将该溶液中FeCl2完全氧化为FeCl3最好选择下列物质中的_______。

请回答下列问题:
(1)装置B中发生反应的化学方程式是
(2)装置B中石棉绒的作用是
(3)E中出现的现象是
(4)该小组把B中反应后的产物加入足量的盐酸中,用该溶液制备FeCl3·6H2O晶体。该实验小组同学用上述试剂没有检测到Fe3+,用离子方程式解释溶液中不存在Fe3+可能的原因:
(5)将该溶液中FeCl2完全氧化为FeCl3最好选择下列物质中的_______。
| A.酸性溶液 | B.Cl2 | C.Na2O2 | D.FeCl3 |
您最近一年使用:0次
名校
解题方法
10 . 某研究性学习小组请你参与“研究铁与水反应所得固体物质的成分、性质及再利用”实验探 究,并共同回答下列问题:
探究一:设计如图所示装置进行“铁与水反应”的实验(夹持仪器略).
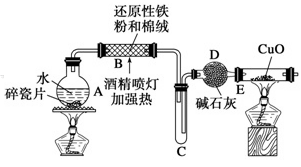
(1)硬质玻璃管 B 中发生反应的化学方程式为:________________________________ .。
(2)反应前 A 中投放碎瓷片的目的是___________________ .。
(3)装置 E 中的现象是_______________________ 。
探究二:设计如下实验方案确定反应后硬质玻璃管 B 中黑色固体的成分。
(4)待硬质玻璃管 B 冷却后,取少许其中的固体物质溶于___________________ 后,将所得溶液分成两份。
(5)一份滴加几滴 KSCN 溶液。若溶液变血红色,推断硬质玻璃管 B 中固体物质的成分为______________________ (选 填序号,下同);若溶液未变血红色,推断硬质玻璃管 B 中固体物质的成分为__________________________________ 。
①一定有 Fe3O4 ②一定有 Fe ③只有 Fe3O4 ④只有 Fe
(6)另一份用_____ (填仪器名称)加入_____ (填试剂和现象),可以 证明溶液中存在 Fe2+。
探究三:设计如下流程测定反应后硬质玻璃管 B 中固体含铁元素的质量分数。

(7)试剂 b 的化学式是_____ 。
(8)计算反应后 B 装置中铁元素的质量分数为_____ 。
探究一:设计如图所示装置进行“铁与水反应”的实验(夹持仪器略).

(1)硬质玻璃管 B 中发生反应的化学方程式为:
(2)反应前 A 中投放碎瓷片的目的是
(3)装置 E 中的现象是
探究二:设计如下实验方案确定反应后硬质玻璃管 B 中黑色固体的成分。
(4)待硬质玻璃管 B 冷却后,取少许其中的固体物质溶于
(5)一份滴加几滴 KSCN 溶液。若溶液变血红色,推断硬质玻璃管 B 中固体物质的成分为
①一定有 Fe3O4 ②一定有 Fe ③只有 Fe3O4 ④只有 Fe
(6)另一份用
探究三:设计如下流程测定反应后硬质玻璃管 B 中固体含铁元素的质量分数。

(7)试剂 b 的化学式是
(8)计算反应后 B 装置中铁元素的质量分数为
您最近一年使用:0次
2016-12-09更新
|
1139次组卷
|
6卷引用:【全国百强校】山西省实验中学2018-2019学年高一上学期12月月考化学试题



