广东省深圳市重点中学2021-2022学年高二上学期期末考试化学试题
广东
高二
期末
2022-09-23
791次
整体难度:
容易
考查范围:
化学与STSE、常见无机物及其应用、化学反应原理、认识化学科学、有机化学基础、化学实验基础、物质结构与性质
广东省深圳市重点中学2021-2022学年高二上学期期末考试化学试题
广东
高二
期末
2022-09-23
791次
整体难度:
容易
考查范围:
化学与STSE、常见无机物及其应用、化学反应原理、认识化学科学、有机化学基础、化学实验基础、物质结构与性质
一、单选题 添加题型下试题
单选题
|
较易(0.85)
1. 2021年世界环境日主题是“人与自然和谐共生”。下列行为符合该主题的是
| A.推广植树造林计划 | B.提倡秸秆就地焚烧 |
| C.实施远海废水排放 | D.填埋法处理废电池 |
您最近一年使用:0次
2021-12-24更新
|
160次组卷
|
2卷引用:江苏省百校大联考2021-2022学年高三上学期第二次考试化学试题
单选题
|
较易(0.85)
名校
2. 化学与生产、生活密切相关,生活中处处有化学,化学让世界更美好。下列叙述正确的是
| A.“84”消毒液等含氯消毒剂、过氧乙酸、体积分数为75%的酒精等均可以有效灭活新型冠状病毒,所以将“84”消毒液与75%酒精1:1混合,消毒效果更好 |
| B.钢铁制品和纯铜制品均既能发生吸氧腐蚀又能发生析氢腐蚀 |
| C.CO、SO2、NO、NO2均为大气污染物,“燃煤固硫”、“汽车尾气催化净化”都能提高空气质量 |
| D.“嫦娥五号”使用的太阳能电池阵和锂离子电池组,均可将化学能转变成电能 |
您最近一年使用:0次
2021-12-01更新
|
800次组卷
|
6卷引用:山东省济南市山东师范大学附属中学2021-2022学年高三上学期期中考试化学试题
单选题
|
容易(0.94)
名校
解题方法
3. 下列物质的化学用语表达错误的是
A.甲烷的比例模型: | B.乙醚的结构简式:CH3OCH3 |
| C.乙酸乙酯的实验式:C2H4O | D.羟基的电子式: |
您最近一年使用:0次
2021-10-29更新
|
327次组卷
|
3卷引用:【石家庄新东方】2020年石家庄一中高二上期末考试化学试题
单选题
|
适中(0.65)
4. 实验室制备溴苯的装置如图所示。下列关于实验操作或叙述错误的是
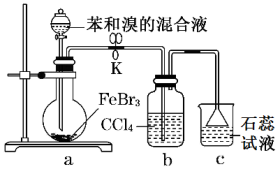

| A.FeBr3作催化剂,可用铁屑代替FeBr3 |
| B.装置b的作用是吸收挥发的苯和溴蒸气 |
| C.装置c中石蕊溶液变为红色,可证明苯与溴发生取代反应 |
| D.反应后的混合液经稀碱溶液洗涤、结晶,得到溴苯 |
您最近一年使用:0次
2021-11-09更新
|
359次组卷
|
3卷引用:安徽省滁州市定远县民族中学2021-2022学年高三上学期10月教学质量检测化学试题
安徽省滁州市定远县民族中学2021-2022学年高三上学期10月教学质量检测化学试题(已下线)专题36 物质的制备及实验方案的设计与评价(热点讲义)-2022年高三毕业班化学常考点归纳与变式演练广东省深圳市重点中学2021-2022学年高二上学期期末考试化学试题
单选题
|
适中(0.65)
名校
5. 由下列实验事实所得出的结论正确的是
| 选项 | 实验事实 | 结论 |
| A | 其它条件相同时,升高温度,Na2S2O3溶液与硫酸反应,析出硫的时间变短 | 其他条件相同下,升高温度化学反应速率增大 |
| B | 密闭容器中发生反应 ,压缩容器体积,气体颜色变深 ,压缩容器体积,气体颜色变深 | 增大压强,平衡向逆反应方向移动 |
| C | 浓度相同的盐酸和醋酸分别与等质量的形状相同的锌粒反应,前者反应速率快 | 金属与酸的反应中,酸的浓度对反应速率无影响 |
| D | 在化学反应前后,催化剂的质量和化学性质都没有发生改变 | 催化剂一定不参与化学反应 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2021-10-17更新
|
541次组卷
|
9卷引用:广东省广州市北师大附中为明学校2021-2022学年高二10月月考化学试题
广东省广州市北师大附中为明学校2021-2022学年高二10月月考化学试题(已下线)必考点05 电离平衡-【对点变式题】2021-2022学年高二化学上学期期中期末必考题精准练(人教版选择性必修1)河北省衡水市第十四中学(西校区)2021-2022学年高二上学期二调考试化学试题安徽省六安市第一中学2021-2022学年高二上学期期中考试化学试题广东省深圳市重点中学2021-2022学年高二上学期期末考试化学试题广东省佛山市顺德区东逸湾实验学校2022-2023学年高二上学期9月份检测化学试题重庆市2022-2023学年高二上学期12月调研考试化学试题河南省许昌市2022-2023学年高二上学期期末教学质量检测化学试题四川省眉山市仁寿县校际2023-2024学年高二上学期10月联考化学试题
6. 下列有关化学图象表现的内容错误的是
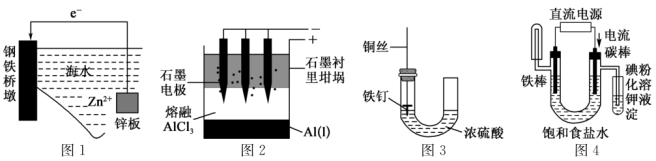

| A.图1表示牺牲阳极法 |
B.图2表示电解熔融 制备 制备 |
| C.图3所示装置中的铁钉几乎没被腐蚀 |
D.图4能验证 溶液(含酚酞)的电解产物 溶液(含酚酞)的电解产物 |
您最近一年使用:0次
2021-12-30更新
|
508次组卷
|
3卷引用:山西省运城市教育发展联盟2021-2022学年高二上学期12月月考化学试题
单选题
|
适中(0.65)
名校
解题方法
7. 研究表明CO与 在
在 作用下发生反应的能量变化及反应历程如图所示,两步反应分别为:①
作用下发生反应的能量变化及反应历程如图所示,两步反应分别为:①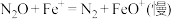 ;②
;② 。下列说法正确的是
。下列说法正确的是
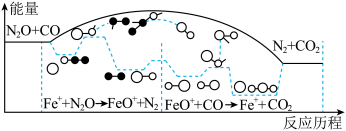
 在
在 作用下发生反应的能量变化及反应历程如图所示,两步反应分别为:①
作用下发生反应的能量变化及反应历程如图所示,两步反应分别为:①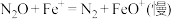 ;②
;② 。下列说法正确的是
。下列说法正确的是
| A.反应①是氧化还原反应,反应②是非氧化还原反应 |
| B.两步反应均为放热反应,总反应的化学反应速率由反应②决定 |
C.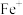 使反应的活化能减小, 使反应的活化能减小,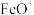 是中间产物 是中间产物 |
D.若转移1mol电子,则消耗11.2L |
您最近一年使用:0次
2022-12-03更新
|
413次组卷
|
26卷引用:【市级联考】湖南省岳阳市2019届高三上学期教学质量检测(一模)化学试题
【市级联考】湖南省岳阳市2019届高三上学期教学质量检测(一模)化学试题2020届全国II卷高考化学模拟卷(三)(已下线)专题6.1 化学能与热能(练)——2020年高考化学一轮复习讲练测宁夏回族自治区银川市第一中学2020届高三第四次模拟考试理综化学试题陕西省西安中学2020届高三仿真考试(一)化学试题河南省洛阳市新安县第一高级中学2021届高三入学测试化学试题四川省阆中中学2021届高三上学期9月月考理综化学试题湖南省永州市2021届高三第一次模拟化学试题黑龙江省鹤岗市第一中学2021届高三上学期第二次月考化学试题江西省南昌市第二中学2020-2021学年高二上学期第三次月考化学试题江西省抚州市黎川县第一中学2020-2021学年高二上学期第三次月考化学试题江西省景德镇一中2020-2021学年高一下学期期末考试化学(2班)试题甘肃省嘉峪关市第一中学2021届高三上学期二模考试化学试题福建省福州格致中学2021-2022学年高二上学期第一阶段测试化学试题(10月)(已下线)专题10 化学反应机理分析-【微专题·大素养】备战2022年高考化学讲透提分要点江西省奉新县第一中学2021-2022学年上学期高三第一次月考化学试题河南省重点高中2021-2022学年高二下学期阶段性调研联考一化学试题广东省深圳市重点中学2021-2022学年高二上学期期末考试化学试题江西省丰城市第九中学2021-2022学年高二上学期第二次月考(日新班)化学试题湖北省武汉市部分重点中学2022-2023学年高二上学期10月联考化学试题福建省龙岩市永定区坎市中学2022-2023学年高三上学期期中化学试题福建省晋江市第一中学2021-2022学年高二上学期线上学习诊断暨单元测试(第一次月考)化学试题湖北省公安县第三中学2021-2022学年高三上学期10月质量检测化学试题(已下线)题型22 反应历程—活化能—催化剂的定性和定量分析广东省广州市执信中学2021届高三第五次月考化学试题四川省凉山州宁南中学2023-2024学年高二上学期第一次月考化学试题
单选题
|
较易(0.85)
8. 试剂生产中,常用双环戊二烯通入水蒸气解聚成环戊二烯,下列说法不正确 的是


| A.双环戊二烯的分子式为C10H12 |
| B.双环戊二烯和环戊二烯均能使酸性KMnO4溶液褪色 |
| C.环戊二烯的一氯代物有3种 |
| D.环戊二烯所有原子均能共平面 |
您最近一年使用:0次
2021-01-20更新
|
246次组卷
|
2卷引用:广东省“百越名校联盟”2021届高三12月普通高中学业质量检测化学试题
单选题
|
较易(0.85)
名校
解题方法
9. 下列说法中错误的是
| A.红外光谱仪、核磁共振仪都可用于有机物的结构分析 |
B. 中含有的4种官能团 中含有的4种官能团 |
C.1mol 最多能和4molH2发生加成反应 最多能和4molH2发生加成反应 |
| D.2,5—二甲基己烷的核磁共振氢谱中出现了三个峰 |
【知识点】 红外光谱解读 核磁共振氢谱解读 有机官能团的性质及结构
您最近一年使用:0次
2022-09-07更新
|
429次组卷
|
3卷引用:广东省深圳市重点中学2021-2022学年高二上学期期末考试化学试题
广东省深圳市重点中学2021-2022学年高二上学期期末考试化学试题浙江省舟山市普陀中学2022-2023学年高三上学期9月月考化学试题(已下线)专题02 研究有机化合物的一般方法(知识串讲+专题过关)-2022-2023学年高二化学下学期期中期末考点大串讲(人教版2019)
单选题
|
适中(0.65)
名校
解题方法
10. 设NA为阿伏加德罗常数的值。下列说法正确的是
| A.25℃时,1LpH=1的H2SO4溶液中H+的数目为0.2NA |
B.1L0.1mol/L的Na2CO3溶液中含有 的数目为0.1NA 的数目为0.1NA |
| C.25℃时,pH=13的NaOH溶液中含有OH-的个数为0.1NA |
| D.25℃时,1LpH=10的CH3COONa溶液中,水电离出的H+的数目为10-4NA |
您最近一年使用:0次
2021-12-31更新
|
307次组卷
|
5卷引用:河北省石家庄市正中实验中学2021-2022学年高二上学期第三次月考化学试题
单选题
|
适中(0.65)
名校
解题方法
11. 常温下,下列叙述正确的是
A.新制氯水中加入NaOH固体恰好反应: |
B. 的 的 溶液: 溶液: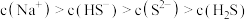 |
C. 溶液加水稀释后,溶液中 溶液加水稀释后,溶液中 的值减小 的值减小 |
D.等物质的量的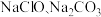 混合溶液中: 混合溶液中: |
您最近一年使用:0次
2021-11-13更新
|
240次组卷
|
3卷引用:安徽省六安市第一中学2021-2022学年高二上学期期中考试化学试题
单选题
|
适中(0.65)
名校
解题方法
12. 一定条件下, ,
, 平衡转化率随温度变化如图所示,对a、b、c 三点对应情况的分析,合理的是
平衡转化率随温度变化如图所示,对a、b、c 三点对应情况的分析,合理的是

 ,
, 平衡转化率随温度变化如图所示,对a、b、c 三点对应情况的分析,合理的是
平衡转化率随温度变化如图所示,对a、b、c 三点对应情况的分析,合理的是
A. 物质的量分数: 物质的量分数: | B. 体积分数: 体积分数: |
C.平衡常数: | D.反应速率: |
您最近一年使用:0次
2021-11-13更新
|
232次组卷
|
2卷引用:安徽省六安市第一中学2021-2022学年高二上学期期中考试化学试题
单选题
|
适中(0.65)
13. 钴( )的合金材料广泛应用于航空航天、机械制造等领域。如图为水溶液中电解制备金属钴的装置示意图。下列说法正确的是
)的合金材料广泛应用于航空航天、机械制造等领域。如图为水溶液中电解制备金属钴的装置示意图。下列说法正确的是
 )的合金材料广泛应用于航空航天、机械制造等领域。如图为水溶液中电解制备金属钴的装置示意图。下列说法正确的是
)的合金材料广泛应用于航空航天、机械制造等领域。如图为水溶液中电解制备金属钴的装置示意图。下列说法正确的是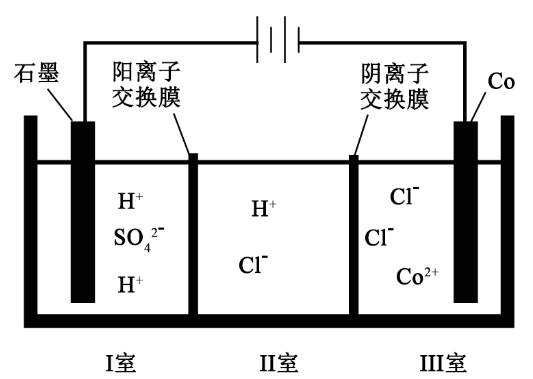
A.工作时,Ⅰ室和Ⅱ室溶液的 均增大 均增大 |
B.生成 ,Ⅰ室溶液质量理论上减少 ,Ⅰ室溶液质量理论上减少 |
| C.移除两交换膜后,石墨电极上发生的反应不变 |
D.电解总反应: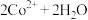  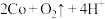 |
您最近一年使用:0次
2021-06-11更新
|
17987次组卷
|
58卷引用:2021年新高考广东化学高考真题
2021年新高考广东化学高考真题(已下线)课时31 新型电解池装置-2022年高考化学一轮复习小题多维练(全国通用)(已下线)考点22 电解池 金属的腐蚀与防护-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点22 电解池 金属的腐蚀与防护-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)第17讲 电解池 金属的腐蚀与防护(讲)— 2022年高考化学一轮复习讲练测(新教材新高考)(已下线)专题讲座(四)新型电源及电极反应式的书写 (讲) — 2022年高考化学一轮复习讲练测(新教材新高考)(已下线)考向20 电解池 金属的腐蚀与防护-备战2022年高考化学一轮复习考点微专题山东省枣庄市薛城区2021-2022学年高二上学期期中考试化学试题(已下线)专题08 电化学之电解池-【微专题·大素养】备战2022年高考化学讲透提分要点河北省石家庄市第二中学2022届高三上学期11月第三次考试化学试题(已下线)专题11 电化学-备战2022年高考化学学霸纠错(全国通用)2021年广东省高考化学试卷变式题11-21山东省济南市莱芜第一中学2021-2022学年高三上学期期中考试化学试题(已下线)解密08 化学反应与能量(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)(已下线)解密08 化学反应与能量(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)专题06 电化学原理应用—2022年高考化学二轮复习讲练测(全国版)-讲义(已下线)专题11 电化学-2022年高考化学二轮复习重点专题常考点突破练(已下线)专题06 电化学原理应用—2022年高考化学二轮复习讲练测(全国版)-练习山西省晋城市第一中学2021-2022学年高二上学期12月月考化学试题(已下线)卷08 电化学及其应用-【小题小卷】冲刺2022年高考化学小题限时集训(新高考专用)(已下线)回归教材重难点03 电化学基础知识-【查漏补缺】2022年高考化学三轮冲刺过关(新高考专用)(已下线)押新高考卷12题 电化学基础-备战2022年高考化学临考题号押题(新高考通版)湖南省岳阳市湘阴县第一中学2021-2022学年高三下学期期中考试化学试题江苏省镇江市五校2021-2022学年高二下学期期末考试化学试题(已下线)专题08 电化学及其应用-三年(2020-2022)高考真题分项汇编(已下线)微专题10 “守恒法”在氧化还原反应计算中的应用-备战2023年高考化学一轮复习考点微专题(已下线)考点19 电解池-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)第35练 电解池-2023年高考化学一轮复习小题多维练(全国通用)(已下线)微专题32 电化学中的交换膜-备战2023年高考化学一轮复习考点微专题(已下线)微专题33 四步敲定高考新情景电池电极反应式的书写-备战2023年高考化学一轮复习考点微专题广东省深圳市重点中学2021-2022学年高二上学期期末考试化学试题第二节 电解池 第2课时 电解原理的应用(已下线)微专题35 电化学“多池和多室”串联问题及计算-备战2023年高考化学一轮复习考点微专题(已下线)第17讲 电解池 金属的腐蚀与防护 (讲)-2023年高考化学一轮复习讲练测(新教材新高考)陕西省渭南高级中学2021-2022学年高一下学期第三阶段考试化学试题山东省青岛第一中学2022-2023学年高二上学期期中考试化学试题重庆市永川北山中学校2022-2023学年高三上学期期中质量监测化学试题(已下线)专题05 化学能与电能的转化(练)-2023年高考化学二轮复习讲练测(新高考专用)广东省广州大学附属中学2022-2023学年高二上学期期末考试化学试题(已下线)专题16 新型电化学装置分析-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)(已下线)第六章 化学反应与能量 第39讲 多池、多室的电化学装置(已下线)题型21 三室膜电解装置及其应用(已下线)专题七 电化学中“离子交换膜”的应用(练习)吉林省吉林市普通高中友好学校2022-2023学年高二上学期期末考试化学试题(已下线)专题卷16 离子隔膜在电化学中的应用-【小题小卷】冲刺2023年高考化学小题限时集训(新高考专用)(已下线)题型20 三室膜电解装置及其应用(已下线)专题12 电化学的综合应用(已下线)专题12 电化学的综合应用微专题(16) 电解在物质制备和提纯中的应用(已下线)考点19 电解池(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)第4讲 电解池 金属的电化学腐蚀与防护(已下线)考点2 原电池 新型电源(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)(已下线)考点3 电解池 金属的腐蚀与防护(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)福建省三明第一中学2022-2023学年高三上学期期中考试化学试题云南省中央民族大学附属中学昆明五华实验学校2023-2024学年高二上学期期中考试化学试题北京市中国人民大学附属中学2021-2022学年高三下学期开学考试化学试卷四川省绵阳市东辰学校2023-2024学年高二上学期第四次月考化学试题 2023届河南省南阳市六校高三下学期第一次联考化学试卷
单选题
|
较易(0.85)
解题方法
14. 利用废铁屑(主要成分为Fe,还含有C、S、P等)制取高效净水剂 ,流程如图:
,流程如图:
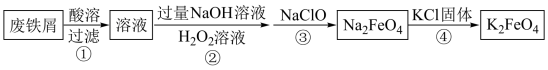
下列说法不正确的是
 ,流程如图:
,流程如图:
下列说法不正确的是
| A.废铁屑在酸溶前可用少量稀硫酸溶液预处理去除油污 |
B.步骤②中发生反应的离子方程式为 |
C.步骤③中每生成8.3g  转移0.15mol 转移0.15mol  |
| D.步骤④中发生的反应类型为复分解反应 |
您最近一年使用:0次
2021-11-04更新
|
385次组卷
|
3卷引用:山西省吕梁市2021-2022学年高三上学期11月月考化学试题
单选题
|
适中(0.65)
15. 用如图所示实验装置进行相应的实验,不能达到实验目的的是


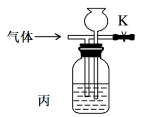





| A.图甲装置中将C管位置提高可用于检验装置气密性 |
| B.图乙用于洗气,可以除去HCl中的Cl2气体 |
| C.关闭丙装置中弹簧夹K,该装置可用于临时储存气体 |
| D.用丁装置蒸干次氯酸钠溶液制备次氯酸钠晶体 |
您最近一年使用:0次
单选题
|
容易(0.94)
名校
16. 在恒容密闭容器中充入一定量的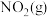 和
和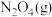 ,发生反应
,发生反应
 ,体系中各物质的百分含量与温度的变化关系如图所示,下列说法错误的是
,体系中各物质的百分含量与温度的变化关系如图所示,下列说法错误的是

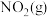 和
和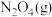 ,发生反应
,发生反应
 ,体系中各物质的百分含量与温度的变化关系如图所示,下列说法错误的是
,体系中各物质的百分含量与温度的变化关系如图所示,下列说法错误的是
A.曲线①表示 的百分含量 的百分含量 |
B. 的键能总和大于 的键能总和大于 的键能总和 的键能总和 |
C.若 点为反应平衡点,此时平衡常数 点为反应平衡点,此时平衡常数 |
| D.反应达到平衡后,保持其他条件不变,往该容器中充入少量稀有气体,反应速率不改变 |
您最近一年使用:0次
2021-07-07更新
|
651次组卷
|
5卷引用:湖北省十堰市2020-2021学年高二下学期期末调研考试化学试题
湖北省十堰市2020-2021学年高二下学期期末调研考试化学试题(已下线)周末培优1 化学反应速率与化学平衡图像问题-2021-2022学年高二化学课后培优练(人教版选修4)河南省豫南重点高中2021-2022学年高二上学期精英对抗赛化学试题四川省绵阳南山中学2021-2022学年高二上学期12月月考化学试题广东省深圳市重点中学2021-2022学年高二上学期期末考试化学试题
二、解答题 添加题型下试题
解答题-原理综合题
|
适中(0.65)
解题方法
17. 氮氧化物是大气污染物之一,可用活性炭还原处理氮氧化物,有关反应为C(s)+2NO(g) N2(g)+CO2(g)。
N2(g)+CO2(g)。
(1)已知①N2(g)+O2(g)=2NO(g)ΔH1=+akJ·mol-1;②C(s)的燃烧热为ΔH2=-bkJ·mol-1.反应C(s)+2NO(g) N2(g)+CO2(g)的ΔH=
N2(g)+CO2(g)的ΔH=___________ kJ·mol-1(用含a、b的代数式表示)。
(2)对比研究活性炭、负载钙、镧氧化物的反应活性。在三个反应器中分别加入C、CaO/C、La2O3/C,通入相同浓度的NO,不同温度下测得反应2小时时NO去除率如图所示:

据图分析,温度在500℃以内,三种情况下反应的活化能最小的是___________ (填“C”“CaO/C”或“La2O3/C”)。A点___________ (填“是”或“不是”)平衡点,原因是___________ 。
(3)某温度下,若向2L体积恒定的密闭容器中充入等物质的量的N2和CO2发生反应:N2(g)+CO2(g) C(s)+2NO(g);其中N2、NO物质的量随时间变化的曲线如图所示:
C(s)+2NO(g);其中N2、NO物质的量随时间变化的曲线如图所示:

①图中B点v正___________ v逆(填“>”“<”或“=”)。
②第10min时,外界改变的条件可能是___________ (填字母)。
A.加催化剂
B.增大C(s)的物质的量
C.减小CO2的物质的量
D.升温
E.降温
③12分钟后反应N2(g)+CO2(g) C(s)+2NO(g)的平衡常数K=
C(s)+2NO(g)的平衡常数K=___________ (保留小数点后2位)。
 N2(g)+CO2(g)。
N2(g)+CO2(g)。(1)已知①N2(g)+O2(g)=2NO(g)ΔH1=+akJ·mol-1;②C(s)的燃烧热为ΔH2=-bkJ·mol-1.反应C(s)+2NO(g)
 N2(g)+CO2(g)的ΔH=
N2(g)+CO2(g)的ΔH=(2)对比研究活性炭、负载钙、镧氧化物的反应活性。在三个反应器中分别加入C、CaO/C、La2O3/C,通入相同浓度的NO,不同温度下测得反应2小时时NO去除率如图所示:

据图分析,温度在500℃以内,三种情况下反应的活化能最小的是
(3)某温度下,若向2L体积恒定的密闭容器中充入等物质的量的N2和CO2发生反应:N2(g)+CO2(g)
 C(s)+2NO(g);其中N2、NO物质的量随时间变化的曲线如图所示:
C(s)+2NO(g);其中N2、NO物质的量随时间变化的曲线如图所示:
①图中B点v正
②第10min时,外界改变的条件可能是
A.加催化剂
B.增大C(s)的物质的量
C.减小CO2的物质的量
D.升温
E.降温
③12分钟后反应N2(g)+CO2(g)
 C(s)+2NO(g)的平衡常数K=
C(s)+2NO(g)的平衡常数K=
您最近一年使用:0次
2022-09-07更新
|
392次组卷
|
2卷引用:广东省深圳市重点中学2021-2022学年高二上学期期末考试化学试题
解答题-实验探究题
|
适中(0.65)
解题方法
18. 席夫碱在有机合成、液晶材料、植物生长调节等多个领域有重要用途。学习小组在实验室中探究由对甲基苯胺(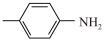 )与苯甲醛(
)与苯甲醛(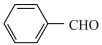 )在酸催化下制备对甲基苯胺缩苯甲醛席夫碱(
)在酸催化下制备对甲基苯胺缩苯甲醛席夫碱(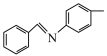 ,M
,M ,有关信息和装置如表。
,有关信息和装置如表。
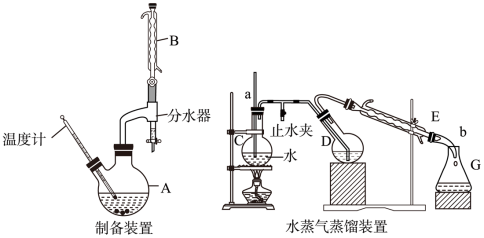
回答下列问题:
(1)实验步骤:
①按图安装好制备装置,检验装置的气密性。向A中加入6.0g对甲基苯胺、5.0mL苯甲醛、50mL乙醇和适量乙酸。其中分水器可接收并分离生成的水。乙醇的作用为___________ 。
②控制反应温度为50℃,加热回流至反应结束。合适的加热方式为___________ ;装置B的作用是___________ 。
(2)纯化产品:
①按图安装好水蒸气蒸馏装置,检验装置的气密性。将A中反应后余液转移至D中,在C中加入适量水,进行蒸馏,将产品中的乙醇、对甲基苯胺和苯甲醛蒸出。管a的作用为___________ ;仪器b的名称为___________ 。
②蒸馏操作结束后,需先打开止水夹再停止加热的原因为___________ 。
③实验后将D中固体洗涤、干燥后,进一步通过___________ (填操作名称)纯化后,得到纯品6.0g。本实验的产品产率为___________ (保留三位有效数字)。
 )与苯甲醛(
)与苯甲醛( )在酸催化下制备对甲基苯胺缩苯甲醛席夫碱(
)在酸催化下制备对甲基苯胺缩苯甲醛席夫碱( ,M
,M ,有关信息和装置如表。
,有关信息和装置如表。| 物质 | 相对分子质量 | 密度/(gcm-3) | 熔点/℃ | 沸点/℃ | 溶解性 |
| 对甲基苯胺 | 107 | 0.96 | 44 | 200 | 微溶于水,易溶于乙醇 |
| 乙醇 | 46 | 0.78 | -114 | 78 | 溶于水 |
| 苯甲醛 | 106 | 1.0 | -26 | 179 | 微溶于水,与乙醇互溶 |

回答下列问题:
(1)实验步骤:
①按图安装好制备装置,检验装置的气密性。向A中加入6.0g对甲基苯胺、5.0mL苯甲醛、50mL乙醇和适量乙酸。其中分水器可接收并分离生成的水。乙醇的作用为
②控制反应温度为50℃,加热回流至反应结束。合适的加热方式为
(2)纯化产品:
①按图安装好水蒸气蒸馏装置,检验装置的气密性。将A中反应后余液转移至D中,在C中加入适量水,进行蒸馏,将产品中的乙醇、对甲基苯胺和苯甲醛蒸出。管a的作用为
②蒸馏操作结束后,需先打开止水夹再停止加热的原因为
③实验后将D中固体洗涤、干燥后,进一步通过
您最近一年使用:0次
解答题-工业流程题
|
适中(0.65)
解题方法
19. 工业上利用废镍催化剂(主要成分为Ni,还含有一定量的Zn、Fe、SiO2、CaO等)制备草酸镍晶体的流程如下:

(1)请写出一种能提高“酸浸”速率的措施:___________ ;滤渣I的成分是___________ (填化学式)。
(2)除铁时,控制不同的条件可以得到不同的滤渣II。已知滤渣II的成分与温度、pH关系如图所示:

①写出除铁步骤中次氯酸钠发生反应的离子方程式___________ 。
②若控制温度25℃、pH=4时除去铁,此时溶液中c(Fe3+)=___________ 。(已知25℃时,Fe(OH)3的Ksp[Fe(OH)3]=2.64×10-39)
(3)加入有机萃取剂除掉的金属阳离子主要是___________ 。
(4)某化学镀镍试剂的化学式为(NH4)xNi(SO4)y(Ni为+2价,,x、y均为正整数)。为测定该镀镍试剂的组成,进行如下实验:
I、称量28.7g镀镍试剂,配制100mL溶液A;
Ⅱ、准确量取10.00mL溶液A,用0.40mol·L-1的EDTA(Na2H2Y)标准溶液滴定其中的Ni2+(离子方程式为Ni2++H2Y2-=NiY2-+2H+),消耗EDTA标准溶液25.00mL;
Ⅲ、另取10.00mL溶液A,加入足量的BaCl2溶液,得到白色沉淀4.66g。
①配制100mL镀镍试剂时,需要的仪器除药匙、托盘天平、玻璃棒、烧杯、量筒、胶头滴管外,还需要___________ 。
②该镀镍试剂的化学式为___________ 。

(1)请写出一种能提高“酸浸”速率的措施:
(2)除铁时,控制不同的条件可以得到不同的滤渣II。已知滤渣II的成分与温度、pH关系如图所示:

①写出除铁步骤中次氯酸钠发生反应的离子方程式
②若控制温度25℃、pH=4时除去铁,此时溶液中c(Fe3+)=
(3)加入有机萃取剂除掉的金属阳离子主要是
(4)某化学镀镍试剂的化学式为(NH4)xNi(SO4)y(Ni为+2价,,x、y均为正整数)。为测定该镀镍试剂的组成,进行如下实验:
I、称量28.7g镀镍试剂,配制100mL溶液A;
Ⅱ、准确量取10.00mL溶液A,用0.40mol·L-1的EDTA(Na2H2Y)标准溶液滴定其中的Ni2+(离子方程式为Ni2++H2Y2-=NiY2-+2H+),消耗EDTA标准溶液25.00mL;
Ⅲ、另取10.00mL溶液A,加入足量的BaCl2溶液,得到白色沉淀4.66g。
①配制100mL镀镍试剂时,需要的仪器除药匙、托盘天平、玻璃棒、烧杯、量筒、胶头滴管外,还需要
②该镀镍试剂的化学式为
您最近一年使用:0次
解答题-有机推断题
|
较易(0.85)
20. 有机化学反应因反应条件不同,可生成不同的有机产品。例如:
①HX+CH3-CH=CH2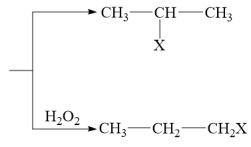 (X为卤素原子)
(X为卤素原子)
②苯的同系物与卤素单质混合,若在光照条件下,侧链上氢原子被卤素原子取代;若在催化剂作用下,苯环上的氢原子被卤素原子取代。
③—CH2—OH可在Cu做催化剂的条件下被O2氧化成—CHO
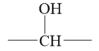 可在Cu做催化剂的条件下被O2氧化成
可在Cu做催化剂的条件下被O2氧化成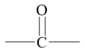
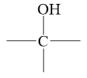 不能在Cu做催化剂的条件下被O2氧化
不能在Cu做催化剂的条件下被O2氧化
工业上利用上述信息,按下列路线合成结构简式为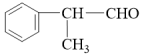 的物质,该物质是一种香料。
的物质,该物质是一种香料。
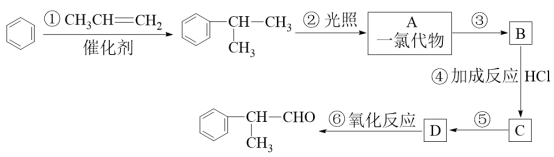
请根据上述路线,回答下列问题:
(1)A的结构简式可能为___________ 。
(2)反应①、③的反应类型分别为___________ 、___________ 。
(3)反应④的化学方程式为(有机物写结构简式,并注明反应条件):___________ 。
(4)工业生产中,中间产物A须经反应③④⑤得D,而不采取直接转化为D的方法,其原因是___________ 。
(5)写出以乙苯为原料制备苯基乙二醇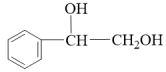 的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干)
的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干)___________ 。
①HX+CH3-CH=CH2
 (X为卤素原子)
(X为卤素原子)②苯的同系物与卤素单质混合,若在光照条件下,侧链上氢原子被卤素原子取代;若在催化剂作用下,苯环上的氢原子被卤素原子取代。
③—CH2—OH可在Cu做催化剂的条件下被O2氧化成—CHO
 可在Cu做催化剂的条件下被O2氧化成
可在Cu做催化剂的条件下被O2氧化成
 不能在Cu做催化剂的条件下被O2氧化
不能在Cu做催化剂的条件下被O2氧化工业上利用上述信息,按下列路线合成结构简式为
 的物质,该物质是一种香料。
的物质,该物质是一种香料。
请根据上述路线,回答下列问题:
(1)A的结构简式可能为
(2)反应①、③的反应类型分别为
(3)反应④的化学方程式为(有机物写结构简式,并注明反应条件):
(4)工业生产中,中间产物A须经反应③④⑤得D,而不采取直接转化为D的方法,其原因是
(5)写出以乙苯为原料制备苯基乙二醇
 的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干)
的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干)
您最近一年使用:0次
试卷分析
整体难度:适中
考查范围:化学与STSE、常见无机物及其应用、化学反应原理、认识化学科学、有机化学基础、化学实验基础、物质结构与性质
试卷题型(共 20题)
题型
数量
单选题
16
解答题
4
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.85 | 大气污染来源及危害 大气污染的治理原理及方法 绿色化学与可持续发展 | |
| 2 | 0.85 | 漂白粉和漂粉精 金属的电化学腐蚀与防护 化学科学对人类文明发展的意义 大气污染的治理原理及方法 | |
| 3 | 0.94 | 有机物的结构式、结构简式、比例模型、球棍模型、最简式 原子、离子、原子团及其电子式的书写与判断 有机物结构的表示方法 | |
| 4 | 0.65 | 苯的取代反应 物质的分离、提纯 物质分离、提纯的常见化学方法 常见有机物的制备 | |
| 5 | 0.65 | 影响化学反应速率的因素 化学平衡的移动及其影响因素 一元强酸与一元弱酸的比较 | |
| 6 | 0.65 | 电冶金 氯碱工业 金属的防护 铁的钝化 | |
| 7 | 0.65 | 碰撞理论及活化能 活化能及其对反应速率的影响 催化剂对化学反应速率的影响 | |
| 8 | 0.85 | 同分异构体的数目的确定 烯烃 烯烃与强氧化性物质的反应 有机分子中原子共面的判断 | |
| 9 | 0.85 | 红外光谱 核磁共振氢谱 有机官能团的性质及结构 | |
| 10 | 0.65 | 阿伏加德罗常数的应用 水溶液中水的电离程度及的计算 pH定义式及计算 盐类水解规律理解及应用 | |
| 11 | 0.65 | 弱电解质电离平衡的影响因素 盐溶液中微粒间的电荷守恒、物料守恒、质子守恒原理 盐溶液中离子浓度大小的比较 | |
| 12 | 0.65 | 影响化学反应速率的外因 化学平衡的移动及其影响因素 化学平衡常数的影响因素及应用 与转化率变化有关图像的分析 | |
| 13 | 0.65 | 电化学计算 电解原理的应用 电解池电极反应式及化学方程式的书写与判断 | |
| 14 | 0.85 | 离子方程式的书写 有关铁及其化合物转化的流程题型 物质分离、提纯综合应用 电子转移计算 | |
| 15 | 0.65 | 盐类水解的应用 相似相溶原理及应用 仪器使用与实验安全 | |
| 16 | 0.94 | 化学平衡题中基于图表数据的相关计算 与物质百分含量变化有关图像的分析 | |
| 二、解答题 | |||
| 17 | 0.65 | 化学反应原理综合考查 盖斯定律与热化学方程式 化学反应速率计算 化学平衡常数的有关计算 | 原理综合题 |
| 18 | 0.65 | 化学实验基础操作 蒸馏与分馏 常见有机物的制备 综合实验设计与评价 | 实验探究题 |
| 19 | 0.65 | 酸碱中和滴定原理的应用 溶度积常数相关计算 配制一定物质的量浓度的溶液实验的仪器 常见无机物的制备 | 工业流程题 |
| 20 | 0.85 | 加成反应 根据题给物质选择合适合成路线 多官能团有机物的结构与性质 有机推断综合考查 | 有机推断题 |



