名校
解题方法
1 . 我校高一化学兴趣小组的同学们为探究铁与浓硫酸的反应,设计了如图所示装置进行实验。
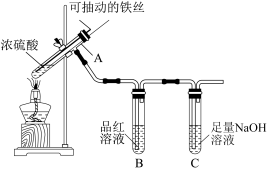
(1)实验过程中,观察到B中的实验现象是_______________ ;写出C中发生反应的离子方程式_________________________ 。
(2)浓硫酸与足量的铁丝反应一段时间后,若观察到从C中有少量的气泡冒出,此气泡的成分是___________ 。试分析产生该气体的原因____________________ 。
(3)用“可抽动的铁丝”代替“直接投入铁片”的优点是_____________________ ;
(4)反应一段时间后,他们对A中溶液的金属阳离子进行了探究
①提出假设:
假设1:_____________ ;
假设2:_____________ ;
假设3:溶液中存在Fe2+和Fe3+。
②已知假设3是正确的,选择合适的试剂,设计实验验证上述假设3,写出实验操作步骤、实验现象及结论。限选试剂:稀HNO3、氯水、酸性KMnO4溶液、NaOH溶液、KSCN溶液。

(1)实验过程中,观察到B中的实验现象是
(2)浓硫酸与足量的铁丝反应一段时间后,若观察到从C中有少量的气泡冒出,此气泡的成分是
(3)用“可抽动的铁丝”代替“直接投入铁片”的优点是
(4)反应一段时间后,他们对A中溶液的金属阳离子进行了探究
①提出假设:
假设1:
假设2:
假设3:溶液中存在Fe2+和Fe3+。
②已知假设3是正确的,选择合适的试剂,设计实验验证上述假设3,写出实验操作步骤、实验现象及结论。限选试剂:稀HNO3、氯水、酸性KMnO4溶液、NaOH溶液、KSCN溶液。
| 实验操作步骤 | 实验现象 | 结论 |
| Ⅰ | 溶液中存在Fe3+; | |
| Ⅱ |
您最近一年使用:0次
2016-12-09更新
|
890次组卷
|
2卷引用:2015-2016学年山西省太原五中高一上学期期末化学试卷
13-14高三·全国·课时练习
名校
解题方法
2 . 某研究性学习小组请你参与“研究铁与水反应所得固体物质的成分、性质及再利用”实验探 究,并共同回答下列问题:
探究一:设计如图所示装置进行“铁与水反应”的实验(夹持仪器略).
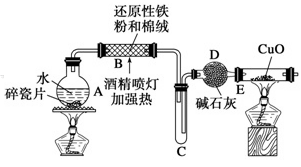
(1)硬质玻璃管 B 中发生反应的化学方程式为:________________________________ .。
(2)反应前 A 中投放碎瓷片的目的是___________________ .。
(3)装置 E 中的现象是_______________________ 。
探究二:设计如下实验方案确定反应后硬质玻璃管 B 中黑色固体的成分。
(4)待硬质玻璃管 B 冷却后,取少许其中的固体物质溶于___________________ 后,将所得溶液分成两份。
(5)一份滴加几滴 KSCN 溶液。若溶液变血红色,推断硬质玻璃管 B 中固体物质的成分为______________________ (选 填序号,下同);若溶液未变血红色,推断硬质玻璃管 B 中固体物质的成分为__________________________________ 。
①一定有 Fe3O4 ②一定有 Fe ③只有 Fe3O4 ④只有 Fe
(6)另一份用_____ (填仪器名称)加入_____ (填试剂和现象),可以 证明溶液中存在 Fe2+。
探究三:设计如下流程测定反应后硬质玻璃管 B 中固体含铁元素的质量分数。

(7)试剂 b 的化学式是_____ 。
(8)计算反应后 B 装置中铁元素的质量分数为_____ 。
探究一:设计如图所示装置进行“铁与水反应”的实验(夹持仪器略).

(1)硬质玻璃管 B 中发生反应的化学方程式为:
(2)反应前 A 中投放碎瓷片的目的是
(3)装置 E 中的现象是
探究二:设计如下实验方案确定反应后硬质玻璃管 B 中黑色固体的成分。
(4)待硬质玻璃管 B 冷却后,取少许其中的固体物质溶于
(5)一份滴加几滴 KSCN 溶液。若溶液变血红色,推断硬质玻璃管 B 中固体物质的成分为
①一定有 Fe3O4 ②一定有 Fe ③只有 Fe3O4 ④只有 Fe
(6)另一份用
探究三:设计如下流程测定反应后硬质玻璃管 B 中固体含铁元素的质量分数。

(7)试剂 b 的化学式是
(8)计算反应后 B 装置中铁元素的质量分数为
您最近一年使用:0次
2016-12-09更新
|
1142次组卷
|
6卷引用:【全国百强校】山西省实验中学2018-2019学年高一上学期12月月考化学试题
3 . (1)向某NaOH溶液中投入一块Al箔,先无明显现象,随后逐渐产生气泡,则产生气泡的离子反应方程式为______ 。
(2)实验室常用还原性Fe粉与水蒸气反应的实验来研究Fe的还原性,则该反应的化学反应方程式为______
(3)Fe(OH)2制备时,采用的方法是“长滴管、液面下”的实验操作,但在实验时,由于操作不当,依旧会出现白色沉淀、灰绿色沉淀直至最终变为红褐色沉淀,写出白色沉淀最终转化为红褐色沉淀的化学反应方程式为______
(4)实验时制备Al(OH)3时,常用可溶性铝盐(如Al2(SO4)3与氨水反应进行制备。某课外小组在实验时不慎向Al2(SO4)3溶液中加入了过量NaOH溶液,最终并没有制出白色沉淀Al(OH)3,则该小组同学实验时发生的总离子反应方程式为____ 。
(2)实验室常用还原性Fe粉与水蒸气反应的实验来研究Fe的还原性,则该反应的化学反应方程式为
(3)Fe(OH)2制备时,采用的方法是“长滴管、液面下”的实验操作,但在实验时,由于操作不当,依旧会出现白色沉淀、灰绿色沉淀直至最终变为红褐色沉淀,写出白色沉淀最终转化为红褐色沉淀的化学反应方程式为
(4)实验时制备Al(OH)3时,常用可溶性铝盐(如Al2(SO4)3与氨水反应进行制备。某课外小组在实验时不慎向Al2(SO4)3溶液中加入了过量NaOH溶液,最终并没有制出白色沉淀Al(OH)3,则该小组同学实验时发生的总离子反应方程式为
您最近一年使用:0次
2017-03-01更新
|
502次组卷
|
3卷引用:山西省运城市景胜中学2019-2020学年高一12月月考化学试题



