(1)向某NaOH溶液中投入一块Al箔,先无明显现象,随后逐渐产生气泡,则产生气泡的离子反应方程式为______ 。
(2)实验室常用还原性Fe粉与水蒸气反应的实验来研究Fe的还原性,则该反应的化学反应方程式为______
(3)Fe(OH)2制备时,采用的方法是“长滴管、液面下”的实验操作,但在实验时,由于操作不当,依旧会出现白色沉淀、灰绿色沉淀直至最终变为红褐色沉淀,写出白色沉淀最终转化为红褐色沉淀的化学反应方程式为______
(4)实验时制备Al(OH)3时,常用可溶性铝盐(如Al2(SO4)3与氨水反应进行制备。某课外小组在实验时不慎向Al2(SO4)3溶液中加入了过量NaOH溶液,最终并没有制出白色沉淀Al(OH)3,则该小组同学实验时发生的总离子反应方程式为____ 。
(2)实验室常用还原性Fe粉与水蒸气反应的实验来研究Fe的还原性,则该反应的化学反应方程式为
(3)Fe(OH)2制备时,采用的方法是“长滴管、液面下”的实验操作,但在实验时,由于操作不当,依旧会出现白色沉淀、灰绿色沉淀直至最终变为红褐色沉淀,写出白色沉淀最终转化为红褐色沉淀的化学反应方程式为
(4)实验时制备Al(OH)3时,常用可溶性铝盐(如Al2(SO4)3与氨水反应进行制备。某课外小组在实验时不慎向Al2(SO4)3溶液中加入了过量NaOH溶液,最终并没有制出白色沉淀Al(OH)3,则该小组同学实验时发生的总离子反应方程式为
更新时间:2017-03-01 18:44:44
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】按要求回答下列问题
(1)近年来,国家围绕“资源节约型和环境友好型”这一主题,积极谋求社会的和谐发展。请你根据这一主题和题意,用下列选项的字母代号进行填空。
a.造成温室效应和全球气候变暖的主要物质是_________ ;
b.以煤炭为主的能源结构易导致酸雨的形成,形成这类酸雨的主要物质是________ ;
c.处理含有Hg2+等重金属离子的废水常用的一种方法是__________ ;
d.人类正面临着石油资源短缺的难题,解决能源短缺问题的一种方法___________ 。
(2)服用含有小苏打的药品以中和过多的胃酸,离子方程式是_________________ 。
(3)Al片溶于NaOH溶液中同时产生的现象是____________ ,反应的化学方程式为: _____________ 。
(1)近年来,国家围绕“资源节约型和环境友好型”这一主题,积极谋求社会的和谐发展。请你根据这一主题和题意,用下列选项的字母代号进行填空。
| A.二氧化硫 | B.二氧化碳 | C.开发新能源 | D.沉淀法 |
a.造成温室效应和全球气候变暖的主要物质是
b.以煤炭为主的能源结构易导致酸雨的形成,形成这类酸雨的主要物质是
c.处理含有Hg2+等重金属离子的废水常用的一种方法是
d.人类正面临着石油资源短缺的难题,解决能源短缺问题的一种方法
(2)服用含有小苏打的药品以中和过多的胃酸,离子方程式是
(3)Al片溶于NaOH溶液中同时产生的现象是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】化学来源于生活,且应用于生活。请根据题意填空:
(1)钠有多种化合物,其中加工馒头、面包等产品时,可作膨松剂的是___________ (填“ ”或“NaCl”)。
”或“NaCl”)。
(2)开盖后的铁强化酱油(铁元素以 表示)久置于空气中易导致补铁效果不佳,主要原因是其中的铁元素由
表示)久置于空气中易导致补铁效果不佳,主要原因是其中的铁元素由 价升高到
价升高到 价,此转化过程体现了
价,此转化过程体现了 的
的___________ (填“氧化性”或“还原性”)。
(3)中国古代最早的指南针“司南”,其具有磁性作用是因为主要含有___________ (填“Fe2O3”或“Fe3O4”)。
(4)铝制餐具不宜用来蒸煮或长时间存放酸性或碱性食物,是因为Al和Al2O3均能与酸、碱反应。则Al2O3属于___________ (填“碱性”或“两性”)氧化物。
(5)我国发行的第五套人民币中,1角硬币的材质为铝合金。铝合金的硬度比纯铝的___________ (填“大”或“小”)。
(1)钠有多种化合物,其中加工馒头、面包等产品时,可作膨松剂的是
 ”或“NaCl”)。
”或“NaCl”)。(2)开盖后的铁强化酱油(铁元素以
 表示)久置于空气中易导致补铁效果不佳,主要原因是其中的铁元素由
表示)久置于空气中易导致补铁效果不佳,主要原因是其中的铁元素由 价升高到
价升高到 价,此转化过程体现了
价,此转化过程体现了 的
的(3)中国古代最早的指南针“司南”,其具有磁性作用是因为主要含有
(4)铝制餐具不宜用来蒸煮或长时间存放酸性或碱性食物,是因为Al和Al2O3均能与酸、碱反应。则Al2O3属于
(5)我国发行的第五套人民币中,1角硬币的材质为铝合金。铝合金的硬度比纯铝的
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】请回答:
(1)CO2的电子式是______ ;光导纤维的主要成分的化学式是______ 。
(2)将新制氯水滴到pH试纸上,观察到的现象是______ 。
(3)向氯化铝溶液中加入过量氨水的离子方程式______ 。
(1)CO2的电子式是
(2)将新制氯水滴到pH试纸上,观察到的现象是
(3)向氯化铝溶液中加入过量氨水的离子方程式
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】请在横线部分写出正确的化学方程式或离子方程式。
(1)镁在二氧化碳中燃烧___________________________ 。
(2)铝与碱溶液反应的离子方程式___________________________ 。
(3)实验室制氢氧化铝的离子方程式___________________________ 。
(4)铝与四氧化三铁高温反应___________________________ 。
(5)氢氧化亚铁在空气中变质___________________________ 。
(6)少量铁在氯气中燃烧___________________________ 。
(1)镁在二氧化碳中燃烧
(2)铝与碱溶液反应的离子方程式
(3)实验室制氢氧化铝的离子方程式
(4)铝与四氧化三铁高温反应
(5)氢氧化亚铁在空气中变质
(6)少量铁在氯气中燃烧
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】a、钠、铝和铁均是重要的金属。
(1)金属钠着火,应用__________ 灭火;
(2)过氧化钠可做呼吸面具的供氧剂,有关化学方程式____________________________ ;
(3)除去NaHCO3溶液中的Na2CO3溶液,应向混合溶液中通入过量的_________ ,有关化学方程式为________________________________________________________ ;
(4)实验室用可溶性铝盐制氢氧化铝的离子方程式为______________________________ ;
(5)向盛有H2O2溶液的试管中加入几滴酸化的FeCl2溶液,溶液变成棕黄色,发生反应的离子方程式为____________________________________ 。
(6)检验溶液中含Fe2+的操作方法______________________________________________ 。
(7)向装FeCl2溶液的试管中滴加NaOH溶液的现象为___________________________ ,有关氧化还原反应方程式为_____________________________________ 。
b、我国古代炼丹中经常使用到丹红,俗称铅丹。其化学式Pb3O4可写成2PbO·PbO2,结合氧化物的分类可知PbO是碱性氧化物,而PbO2不是碱性氧化物。
(8)写出PbO(难溶于水)与盐酸反应的离子方程式______________________________ ;
(9)已知PbO2与浓盐酸混合后可得到PbCl2、黄绿色气体等物质,请写出相应的化学方程式_______________________________________ ;当生成2.24L(标准状况下)黄绿色气体时,转移的电子数目为_____ NA。
(1)金属钠着火,应用
(2)过氧化钠可做呼吸面具的供氧剂,有关化学方程式
(3)除去NaHCO3溶液中的Na2CO3溶液,应向混合溶液中通入过量的
(4)实验室用可溶性铝盐制氢氧化铝的离子方程式为
(5)向盛有H2O2溶液的试管中加入几滴酸化的FeCl2溶液,溶液变成棕黄色,发生反应的离子方程式为
(6)检验溶液中含Fe2+的操作方法
(7)向装FeCl2溶液的试管中滴加NaOH溶液的现象为
b、我国古代炼丹中经常使用到丹红,俗称铅丹。其化学式Pb3O4可写成2PbO·PbO2,结合氧化物的分类可知PbO是碱性氧化物,而PbO2不是碱性氧化物。
(8)写出PbO(难溶于水)与盐酸反应的离子方程式
(9)已知PbO2与浓盐酸混合后可得到PbCl2、黄绿色气体等物质,请写出相应的化学方程式
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】下表是元素周期表的一部分,针对表中用字母标出的元素,回答下列问题:

(1)地壳中含量最高的金属元素是___________ (填标号);化学性质最不活泼的元素是___________ (填元素符号)。
(2)A分别与G、H、I形成的最简单化合物中,稳定性最强的是___________ (填化学式)。
(3)B、C、E、H四种元素对应的简单离子半径由大到小的顺序是___________ (用离子符号表示)。
(4)B、C形成的最高价氧化物对应水化物的碱性从强到弱的顺序为___________ (填化学式)。
(5)用电子式表示J与C形成化合物的过程:___________ 。
(6)请写出B、E的最高价氧化物对应的水化物发生反应的化学方程式:___________ 。

(1)地壳中含量最高的金属元素是
(2)A分别与G、H、I形成的最简单化合物中,稳定性最强的是
(3)B、C、E、H四种元素对应的简单离子半径由大到小的顺序是
(4)B、C形成的最高价氧化物对应水化物的碱性从强到弱的顺序为
(5)用电子式表示J与C形成化合物的过程:
(6)请写出B、E的最高价氧化物对应的水化物发生反应的化学方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】按要求书写下列反应的离子方程式:
(1) 溶液和
溶液和 溶液
溶液
①向 溶液中逐滴滴加
溶液中逐滴滴加 溶液直至过量:
溶液直至过量:_______ ,_______ 。
②向 溶液中逐滴滴加
溶液中逐滴滴加 溶液直至过量:
溶液直至过量:_______ ,_______ 。
③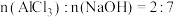 :
:_______ 。
(2) 溶液和稀盐酸
溶液和稀盐酸
①向 溶液中逐滴滴入稀盐酸直至过量:
溶液中逐滴滴入稀盐酸直至过量:_______ ,_______ 。
②向稀盐酸中滴入 溶液:
溶液:_______ 。
(1)
 溶液和
溶液和 溶液
溶液①向
 溶液中逐滴滴加
溶液中逐滴滴加 溶液直至过量:
溶液直至过量:②向
 溶液中逐滴滴加
溶液中逐滴滴加 溶液直至过量:
溶液直至过量:③
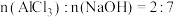 :
:(2)
 溶液和稀盐酸
溶液和稀盐酸①向
 溶液中逐滴滴入稀盐酸直至过量:
溶液中逐滴滴入稀盐酸直至过量:②向稀盐酸中滴入
 溶液:
溶液:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】牙膏是日常生活中常用的清洁用品,由粉状摩擦剂、湿润剂、表面活性剂、黏合剂、香料、甜味剂及其他特殊成分构成。下表列出了三种牙膏中的摩擦剂:

(1)将上述摩擦剂所属物质的正确类别填入空格_________ 、______________ 、_____________ 。
(2)你推测上述三种摩擦剂都__________ (填“溶于”或者“不溶于”)水,理由是_____________ 。
(3)已知二氧化硅的化学式为SiO2,该物质能与NaOH溶液反应,反应方程式为2NaOH+SiO2=Na2SiO3+H2O,Na2SiO3属于____________ (填“酸”“碱”或‘盐”)类。由此可知SiO2属于_________ (填“酸性”或“碱性”)氧化物。非金属氧化物SO2也具有类似的性质,请你写出SO2与NaOH溶液反应的化学方程式___________ 。
(4)已知Al(OH)3可以与盐酸反应:①A1(OH)3+3HCl=A1Cl3+3H2O,也可以与NaOH反应;②Al(OH)3+NaOH=Na[Al(OH)4],由此可知Al(OH)3具有_______ (填“酸性”、“碱性”、“两性”、“还原性”或“氧化性”)将反应①和②改写成离子方程式_________________ 。

| 牙膏 | X牙膏 | Y牙膏 | Z牙膏 |
| 摩擦剂 | 氢氧化铝 | 碳酸钙 | 二氧化硅 |
| 摩擦剂物质类别(指酸、碱、盐、氧化物) | ________ | ________ | ________ |
(1)将上述摩擦剂所属物质的正确类别填入空格
(2)你推测上述三种摩擦剂都
(3)已知二氧化硅的化学式为SiO2,该物质能与NaOH溶液反应,反应方程式为2NaOH+SiO2=Na2SiO3+H2O,Na2SiO3属于
(4)已知Al(OH)3可以与盐酸反应:①A1(OH)3+3HCl=A1Cl3+3H2O,也可以与NaOH反应;②Al(OH)3+NaOH=Na[Al(OH)4],由此可知Al(OH)3具有
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】有A、B、C三种常见的金属单质,A在空气中燃烧生成淡黄色固体;B也能在空气中剧烈燃烧,发出耀眼的白光;C在一定条件下与水蒸气反应生成H2和一种黑色固体。根据以上信息回答下列问题:
(1)写出化学式:A_______ ;B_______ ;C_______ ;
(2)写出化学方程式:
①A与水反应_______ ;
②B在空气中燃烧_______ 。
(1)写出化学式:A
(2)写出化学方程式:
①A与水反应
②B在空气中燃烧
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】(1)①写出小苏打的化学名称______ ;②写出漂白液有效成分的化学式_____ 。
(2)写出高温下Fe与水蒸气反应的化学方程式________ 。
(3)写出过氧化钠与水反应的化学方程式______ 。
(2)写出高温下Fe与水蒸气反应的化学方程式
(3)写出过氧化钠与水反应的化学方程式
您最近一年使用:0次

 后,再往罐内注入足量的
后,再往罐内注入足量的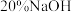 溶液,立即用胶布严封罐口,不多会儿就会听到罐内“咔、咔”作响,发现易拉罐变瘪,再过一会儿易拉罐又鼓涨起来,解释上述变化的实验现象.
溶液,立即用胶布严封罐口,不多会儿就会听到罐内“咔、咔”作响,发现易拉罐变瘪,再过一会儿易拉罐又鼓涨起来,解释上述变化的实验现象.

