我校高一化学兴趣小组的同学们为探究铁与浓硫酸的反应,设计了如图所示装置进行实验。
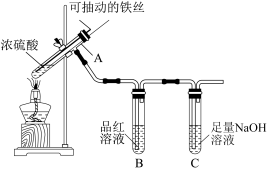
(1)实验过程中,观察到B中的实验现象是_______________ ;写出C中发生反应的离子方程式_________________________ 。
(2)浓硫酸与足量的铁丝反应一段时间后,若观察到从C中有少量的气泡冒出,此气泡的成分是___________ 。试分析产生该气体的原因____________________ 。
(3)用“可抽动的铁丝”代替“直接投入铁片”的优点是_____________________ ;
(4)反应一段时间后,他们对A中溶液的金属阳离子进行了探究
①提出假设:
假设1:_____________ ;
假设2:_____________ ;
假设3:溶液中存在Fe2+和Fe3+。
②已知假设3是正确的,选择合适的试剂,设计实验验证上述假设3,写出实验操作步骤、实验现象及结论。限选试剂:稀HNO3、氯水、酸性KMnO4溶液、NaOH溶液、KSCN溶液。

(1)实验过程中,观察到B中的实验现象是
(2)浓硫酸与足量的铁丝反应一段时间后,若观察到从C中有少量的气泡冒出,此气泡的成分是
(3)用“可抽动的铁丝”代替“直接投入铁片”的优点是
(4)反应一段时间后,他们对A中溶液的金属阳离子进行了探究
①提出假设:
假设1:
假设2:
假设3:溶液中存在Fe2+和Fe3+。
②已知假设3是正确的,选择合适的试剂,设计实验验证上述假设3,写出实验操作步骤、实验现象及结论。限选试剂:稀HNO3、氯水、酸性KMnO4溶液、NaOH溶液、KSCN溶液。
| 实验操作步骤 | 实验现象 | 结论 |
| Ⅰ | 溶液中存在Fe3+; | |
| Ⅱ |
更新时间:2016-12-09 10:54:12
|
相似题推荐
【推荐1】探究SO2的性质。甲组同学将SO2分别通入下列3种溶液中。
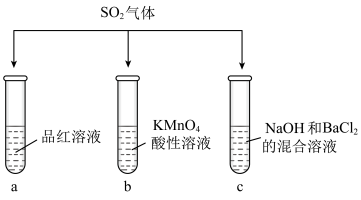
(1)试管a中观察到的现象是_____________ 。
(2)试管b中观察到紫色褪去,说明SO2具有的性质是_____________ 。
(3)试管c中产生了能溶于稀盐酸的白色沉淀,该白色沉淀是_____________ 。
(4)乙组同学多做了一组实验,他们将SO2通入盛有1.0 mol/L Fe(NO3)3和BaCl2的混合溶液(已 知1.0 mol/L Fe(NO3)3溶液中c(H+)=0.1 mol/L)的试管d中,得到了不溶于稀盐酸的白色沉淀。分析产生该白色沉淀的原因:
观点1:SO2与Fe3+反应
观点2:在酸性条件下SO2与 反应
反应
观点3:__________ 。
欲证明观点2,只需将试管d中Fe(NO3)3溶液替换为等体积的下列溶液,在相同条件下进行实验。应选择的试剂是__________ (填字母)。
a. 0.1 mol/L稀硝酸
b. 1.5 mol/L Ba(NO3)2和0.1 mol/L HNO3的混合溶液
c. 6.0 mol/L NaNO3和0.2 mol/L盐酸等体积混合的溶液

(1)试管a中观察到的现象是
(2)试管b中观察到紫色褪去,说明SO2具有的性质是
(3)试管c中产生了能溶于稀盐酸的白色沉淀,该白色沉淀是
(4)乙组同学多做了一组实验,他们将SO2通入盛有1.0 mol/L Fe(NO3)3和BaCl2的混合溶液(已 知1.0 mol/L Fe(NO3)3溶液中c(H+)=0.1 mol/L)的试管d中,得到了不溶于稀盐酸的白色沉淀。分析产生该白色沉淀的原因:
观点1:SO2与Fe3+反应
观点2:在酸性条件下SO2与
 反应
反应观点3:
欲证明观点2,只需将试管d中Fe(NO3)3溶液替换为等体积的下列溶液,在相同条件下进行实验。应选择的试剂是
a. 0.1 mol/L稀硝酸
b. 1.5 mol/L Ba(NO3)2和0.1 mol/L HNO3的混合溶液
c. 6.0 mol/L NaNO3和0.2 mol/L盐酸等体积混合的溶液
您最近一年使用:0次
解答题-实验探究题
|
困难
(0.15)
解题方法
【推荐2】某化学实验小组的同学为探究和比较SO2和氯水的漂白性,设计了如下的实验装置。
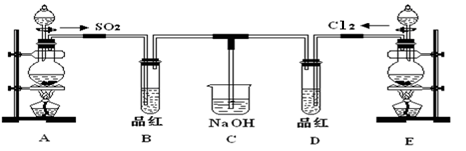
(1)实验室用装置A制备SO2。从物质类别看,SO2属于____________ (填“酸性”、“两性”或“碱性”)氧化物;
(2)实验室用装置E制备Cl2,写出该反应的化学方程式:___________________ 。反应中的液体反应物在反应中所表现出的性质为:_________________ ;
(3)反应开始一段时间后,观察到B、D两个试管中的品红溶液均褪色。停止通气后,再给B、D两个试管分别加热,两个试管中的现象分别为B:________________ ,D:_________________ 。
(4)另一个实验小组的同学认为SO2和氯水都有漂白性,二者混合后的漂白性肯定会更强,他们将制得的SO2和Cl2按1:1同时通入到品红溶液中,结果发现褪色效果并不像想象那样。请你分析该现象的原因(用化学方程式表示)_______________________ 。
(5)C装置是尾气处理装置,写出C装置处理氯气的离子方程式_________________ 。

(1)实验室用装置A制备SO2。从物质类别看,SO2属于
(2)实验室用装置E制备Cl2,写出该反应的化学方程式:
(3)反应开始一段时间后,观察到B、D两个试管中的品红溶液均褪色。停止通气后,再给B、D两个试管分别加热,两个试管中的现象分别为B:
(4)另一个实验小组的同学认为SO2和氯水都有漂白性,二者混合后的漂白性肯定会更强,他们将制得的SO2和Cl2按1:1同时通入到品红溶液中,结果发现褪色效果并不像想象那样。请你分析该现象的原因(用化学方程式表示)
(5)C装置是尾气处理装置,写出C装置处理氯气的离子方程式
您最近一年使用:0次
解答题-无机推断题
|
困难
(0.15)
解题方法
【推荐1】A~H是纯净物或溶液中的溶质,其中A是日常生活中应用最广、用量最大的金属单质。它们之间有如图关系:(部分产物和反应条件略)
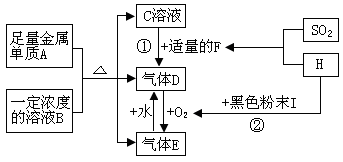
根据上述信息,回答下列问题:
(1)写出下列物质的化学式B_______ ,E_______ 。
(2)H和 SO2生成强酸F,此反应中氧化剂是_______ 。
(3)写出①的离子方程式:_______ 。
(4)写出②的化学方程式:_______ 。
(5)C溶液中滴入NaOH溶液有何现象_______ 。所发生反应的化学方程式为_______ ,_______ 。

根据上述信息,回答下列问题:
(1)写出下列物质的化学式B
(2)H和 SO2生成强酸F,此反应中氧化剂是
(3)写出①的离子方程式:
(4)写出②的化学方程式:
(5)C溶液中滴入NaOH溶液有何现象
您最近一年使用:0次
解答题-实验探究题
|
困难
(0.15)
【推荐1】水煤气的主要成分是CO、H2,还含有少量的CO2和H2O蒸气。如图所示装置设计一个实验,以证明水煤气中含有CO和H2。试回答:
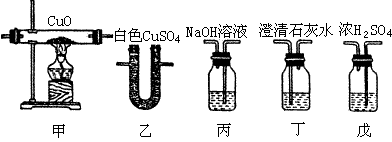
(1)连接上述各装置的正确顺序是(将甲、乙、丙、丁、戊填入方框内):水煤气→_____________ (点燃尾气)
(2)各装置的作用是:
A.乙装置________________________________ 。
B.丙装置________________________________ 。
C.丁装置________________________________ 。
D.戊装置________________________________ 。
(3)写出丙中的离子方程式______________________ 。
写出丁中的离子方程式__________________ 。

(1)连接上述各装置的正确顺序是(将甲、乙、丙、丁、戊填入方框内):水煤气→
(2)各装置的作用是:
A.乙装置
B.丙装置
C.丁装置
D.戊装置
(3)写出丙中的离子方程式
写出丁中的离子方程式
您最近一年使用:0次
解答题-实验探究题
|
困难
(0.15)
名校
解题方法
【推荐2】某研究小组设计如下所示实验装置(夹持装置已略去)分别探究NO与铜粉、Na2O2的反应。
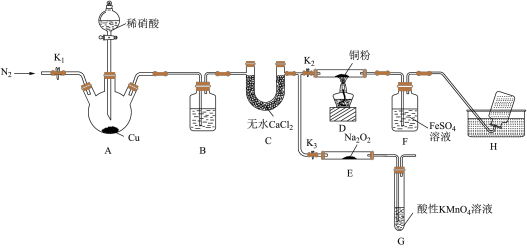
已知:①NO与Na2O2可发生反应2NO+Na2O2===2NaNO2。
②NO能被酸性高锰酸钾溶液氧化为NO3-
③在溶液中存在平衡FeSO4+NO Fe(NO)SO4(棕色)
Fe(NO)SO4(棕色)
I.关闭K3,打开K2,探究NO与铜粉的反应并检验NO。
(1)反应开始前,打开K1,通入一段时间N2,其目的是______________________ 。
(2)装置B中盛放的试剂为水,其作用是______________________ 。
(3)装置F中的实验现象为___________ 。装置H中收集的气体为___________ (填化学式)。
Ⅱ.关闭K2,打开K3,探究NO与Na2O2的反应并制备NaNO2。
(4)装置G的作用是______________________ 。
(5)若省略装置C,则进入装置G中的气体除N2、NO外,可能还有___________ (填化学式)。
(6)测定反应后装置E中NaNO2的含量。已知;在酸性条件下,NO2-可将MnO4-还原为Mn2+,为测定样品中亚硝酸钠的含量,该小组同学称取ag样品溶于水配制成250mL溶液,取25.00mL所得溶液于锥形瓶中,用0.100mol·L-1的酸性KMnO4溶液滴定至终点时,消耗bmL酸性KMnO4溶液。
①滴定过程中发生反应的离子方程式为______________________ 。
②滴定过程中酸性KMnO4溶液的作用是___________ 。
③样品中NaNO2的质量分数为___________ 用含有a、b的代数式表示)

已知:①NO与Na2O2可发生反应2NO+Na2O2===2NaNO2。
②NO能被酸性高锰酸钾溶液氧化为NO3-
③在溶液中存在平衡FeSO4+NO
 Fe(NO)SO4(棕色)
Fe(NO)SO4(棕色)I.关闭K3,打开K2,探究NO与铜粉的反应并检验NO。
(1)反应开始前,打开K1,通入一段时间N2,其目的是
(2)装置B中盛放的试剂为水,其作用是
(3)装置F中的实验现象为
Ⅱ.关闭K2,打开K3,探究NO与Na2O2的反应并制备NaNO2。
(4)装置G的作用是
(5)若省略装置C,则进入装置G中的气体除N2、NO外,可能还有
(6)测定反应后装置E中NaNO2的含量。已知;在酸性条件下,NO2-可将MnO4-还原为Mn2+,为测定样品中亚硝酸钠的含量,该小组同学称取ag样品溶于水配制成250mL溶液,取25.00mL所得溶液于锥形瓶中,用0.100mol·L-1的酸性KMnO4溶液滴定至终点时,消耗bmL酸性KMnO4溶液。
①滴定过程中发生反应的离子方程式为
②滴定过程中酸性KMnO4溶液的作用是
③样品中NaNO2的质量分数为
您最近一年使用:0次
解答题-原理综合题
|
困难
(0.15)
名校
解题方法
【推荐3】用化学方法降解水中有机物已成为污水处理领域的重要研究方向。
(1)酸性条件下,铁炭混合物处理污水中硝基苯时的物质转化示意图如图1所示。
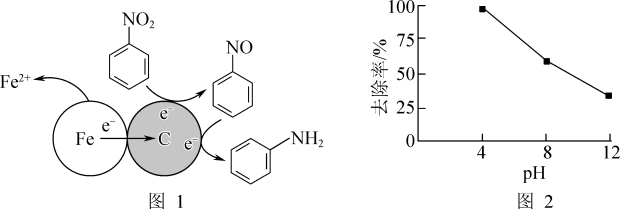
①该物质转化示意图可以描述为_______ 。
②其他条件一定,反应相同时间,硝基苯的去除率与pH的关系如图2所示。pH越大,硝基苯的去除率越低的原因是_______ 。
(2)向含Fe2+和苯胺(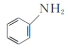 )的酸性溶液中加入双氧水,会发生如下反应:Fe2++H++H2O2=Fe3++HO·+H2O
)的酸性溶液中加入双氧水,会发生如下反应:Fe2++H++H2O2=Fe3++HO·+H2O
①HO·(羟基自由基)具有强氧化性,能将溶液中的苯胺氧化成CO2和N2。写出该反应的离子方程式:_______ 。
②H2O2也具有氧化性,设计验证苯胺是被HO·氧化而不是被H2O2氧化的实验方案:_______ 。
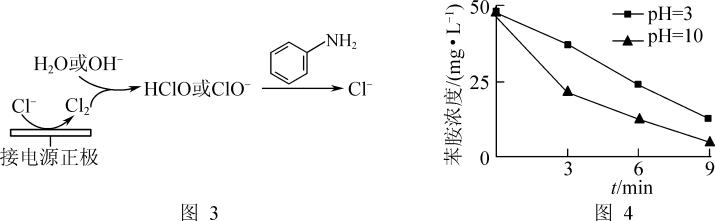
(3)利用电化学装置通过间接氧化法能氧化含苯胺的污水,其原理如图3所示。其他条件一定,测得不同初始pH条件下,溶液中苯胺的浓度与时间的关系如图4所示。反应相同时间,初始溶液pH=3时苯胺浓度大于pH=10时的原因是_______ 。[已知氧化性:HClO(H+)>ClO-(OH-)]
(1)酸性条件下,铁炭混合物处理污水中硝基苯时的物质转化示意图如图1所示。

①该物质转化示意图可以描述为
②其他条件一定,反应相同时间,硝基苯的去除率与pH的关系如图2所示。pH越大,硝基苯的去除率越低的原因是
(2)向含Fe2+和苯胺(
 )的酸性溶液中加入双氧水,会发生如下反应:Fe2++H++H2O2=Fe3++HO·+H2O
)的酸性溶液中加入双氧水,会发生如下反应:Fe2++H++H2O2=Fe3++HO·+H2O①HO·(羟基自由基)具有强氧化性,能将溶液中的苯胺氧化成CO2和N2。写出该反应的离子方程式:
②H2O2也具有氧化性,设计验证苯胺是被HO·氧化而不是被H2O2氧化的实验方案:
(3)利用电化学装置通过间接氧化法能氧化含苯胺的污水,其原理如图3所示。其他条件一定,测得不同初始pH条件下,溶液中苯胺的浓度与时间的关系如图4所示。反应相同时间,初始溶液pH=3时苯胺浓度大于pH=10时的原因是

您最近一年使用:0次



