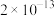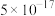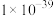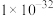用化学方法降解水中有机物已成为污水处理领域的重要研究方向。
(1)酸性条件下,铁炭混合物处理污水中硝基苯时的物质转化示意图如图1所示。
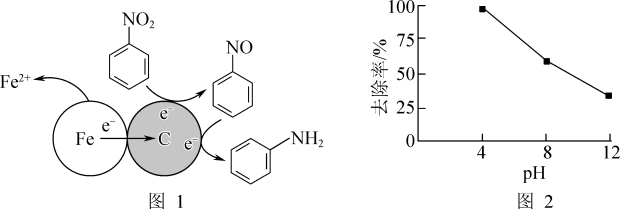
①该物质转化示意图可以描述为_______ 。
②其他条件一定,反应相同时间,硝基苯的去除率与pH的关系如图2所示。pH越大,硝基苯的去除率越低的原因是_______ 。
(2)向含Fe2+和苯胺(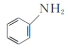 )的酸性溶液中加入双氧水,会发生如下反应:Fe2++H++H2O2=Fe3++HO·+H2O
)的酸性溶液中加入双氧水,会发生如下反应:Fe2++H++H2O2=Fe3++HO·+H2O
①HO·(羟基自由基)具有强氧化性,能将溶液中的苯胺氧化成CO2和N2。写出该反应的离子方程式:_______ 。
②H2O2也具有氧化性,设计验证苯胺是被HO·氧化而不是被H2O2氧化的实验方案:_______ 。
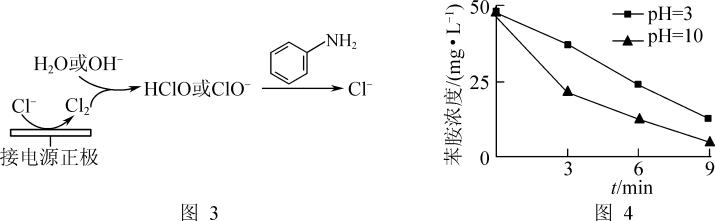
(3)利用电化学装置通过间接氧化法能氧化含苯胺的污水,其原理如图3所示。其他条件一定,测得不同初始pH条件下,溶液中苯胺的浓度与时间的关系如图4所示。反应相同时间,初始溶液pH=3时苯胺浓度大于pH=10时的原因是_______ 。[已知氧化性:HClO(H+)>ClO-(OH-)]
(1)酸性条件下,铁炭混合物处理污水中硝基苯时的物质转化示意图如图1所示。

①该物质转化示意图可以描述为
②其他条件一定,反应相同时间,硝基苯的去除率与pH的关系如图2所示。pH越大,硝基苯的去除率越低的原因是
(2)向含Fe2+和苯胺(
 )的酸性溶液中加入双氧水,会发生如下反应:Fe2++H++H2O2=Fe3++HO·+H2O
)的酸性溶液中加入双氧水,会发生如下反应:Fe2++H++H2O2=Fe3++HO·+H2O①HO·(羟基自由基)具有强氧化性,能将溶液中的苯胺氧化成CO2和N2。写出该反应的离子方程式:
②H2O2也具有氧化性,设计验证苯胺是被HO·氧化而不是被H2O2氧化的实验方案:
(3)利用电化学装置通过间接氧化法能氧化含苯胺的污水,其原理如图3所示。其他条件一定,测得不同初始pH条件下,溶液中苯胺的浓度与时间的关系如图4所示。反应相同时间,初始溶液pH=3时苯胺浓度大于pH=10时的原因是

21-22高三上·江苏南通·期末 查看更多[4]
江苏省盐城中学2022-2023学年高三上学期期末考试化学试题(已下线)回归教材重难点09 化学反应原理综合-【查漏补缺】2022年高考化学三轮冲刺过关(全国通用)(已下线)回归教材重难点09 化学反应原理综合-【查漏补缺】2022年高考化学三轮冲刺过关(新高考专用)(已下线)江苏省如皋市2021-2022学年高三上学期期末考试化学试题
更新时间:2022-02-15 18:07:24
|
相似题推荐
解答题-原理综合题
|
困难
(0.15)
名校
【推荐1】请完成下列填空:
(Ⅰ)A、B、C、D、E五种溶液分别为NaOH、NH3·H2O、CH3COOH、HCl、NH4HSO4中的一种。常温下进行下列实验:
①将1LpH=3的A溶液分别与0.001mol/L xLB溶液、0.001mol/L yLD溶液充分反应至中性,x、y大小关系为:y<x;
②浓度均为0.1mol/L A和E溶液,pH:A<E
③浓度均为0.1mol/L C与D溶液等体积混合,溶液呈酸性。
回答下列问题:
(1)D是_____________ 溶液
(2)用水稀释0.1mol/LB时,溶液中随着水量的增加而减小的是_____________ (填写序号)
① ;②
;② ;③c(H+)和c(OH-)的乘积;④OH-的物质的量
;③c(H+)和c(OH-)的乘积;④OH-的物质的量
(3)OH-浓度相同的等体积的两份溶液A和E,分别和锌粉反应,若最后仅有一份溶液中存在锌,放出氢气的质量相同,则下列说法正确的是_____________ (填写序号)
①反应所需要的时间E>A ②开始反应时的速率A>E
③参加反应的锌粉物质的量A=E ④反应过程的平均速率E>A
⑤A溶液里有锌粉剩余 ⑥E溶液里有锌粉剩余
(4)将等体积、等物质的量浓度B和C混合后溶液,升高温度(溶质不会分解)溶液pH随温度变化如图中的_____________ 曲线(填写序号).

(5)室温下,向0.01mol/LC溶液中滴加0.01mol/LD溶液至中性,得到的溶液中所有离子的物质的量浓度由大到小的顺序为_____________ .
(Ⅱ)如下图所示 ,横坐标为溶液的pH值,纵坐标为Zn2+离子或Zn(OH) 离子物质的量浓度的对数,回答下列问题。
离子物质的量浓度的对数,回答下列问题。
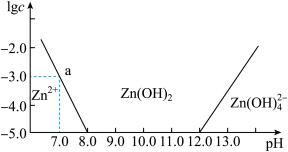
(6)往ZnCl2溶液中加入足量的氢氧化钠溶液,反应的离子方程式可表示为:_______________ 。
(7)从图中数据计算可得Zn(OH)2的溶度积(Ksp)=_______________ 。
(8)某废液中含Zn2+离子,为提取Zn2+离子可以控制溶液中pH值的范围是________________________ 。
(Ⅰ)A、B、C、D、E五种溶液分别为NaOH、NH3·H2O、CH3COOH、HCl、NH4HSO4中的一种。常温下进行下列实验:
①将1LpH=3的A溶液分别与0.001mol/L xLB溶液、0.001mol/L yLD溶液充分反应至中性,x、y大小关系为:y<x;
②浓度均为0.1mol/L A和E溶液,pH:A<E
③浓度均为0.1mol/L C与D溶液等体积混合,溶液呈酸性。
回答下列问题:
(1)D是
(2)用水稀释0.1mol/LB时,溶液中随着水量的增加而减小的是
①
 ;②
;② ;③c(H+)和c(OH-)的乘积;④OH-的物质的量
;③c(H+)和c(OH-)的乘积;④OH-的物质的量(3)OH-浓度相同的等体积的两份溶液A和E,分别和锌粉反应,若最后仅有一份溶液中存在锌,放出氢气的质量相同,则下列说法正确的是
①反应所需要的时间E>A ②开始反应时的速率A>E
③参加反应的锌粉物质的量A=E ④反应过程的平均速率E>A
⑤A溶液里有锌粉剩余 ⑥E溶液里有锌粉剩余
(4)将等体积、等物质的量浓度B和C混合后溶液,升高温度(溶质不会分解)溶液pH随温度变化如图中的

(5)室温下,向0.01mol/LC溶液中滴加0.01mol/LD溶液至中性,得到的溶液中所有离子的物质的量浓度由大到小的顺序为
(Ⅱ)如下图所示 ,横坐标为溶液的pH值,纵坐标为Zn2+离子或Zn(OH)
 离子物质的量浓度的对数,回答下列问题。
离子物质的量浓度的对数,回答下列问题。
(6)往ZnCl2溶液中加入足量的氢氧化钠溶液,反应的离子方程式可表示为:
(7)从图中数据计算可得Zn(OH)2的溶度积(Ksp)=
(8)某废液中含Zn2+离子,为提取Zn2+离子可以控制溶液中pH值的范围是
您最近一年使用:0次
解答题-工业流程题
|
困难
(0.15)
名校
解题方法
【推荐2】我国煤储量居世界第一,对煤的综合、高效、无害化利用是二十一世纪能源战略的重要组成部分,利用含铁元素的粉煤灰获得纳米 等重要物质的工艺流程如下。
等重要物质的工艺流程如下。
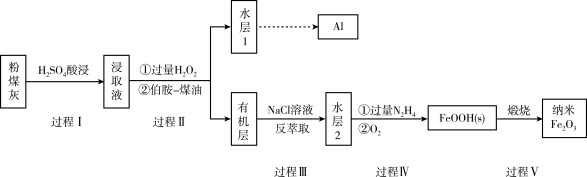
已知:i:伯胺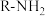 能与
能与 反应:
反应: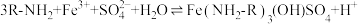 生成易溶于煤油的产物。
生成易溶于煤油的产物。
ii: 在水溶液中易与
在水溶液中易与 反应:
反应: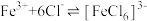
(1)写出过程I中 发生反应的离子方程式:
发生反应的离子方程式:_______ 。
(2)过程Ⅱ加入过量 的作用是
的作用是_______ 。
(3)过程Ⅱ加入伯胺-煤油对浸取液进行分离,该操作的名称是_______ 。
(4)从化学平衡角度解释过程Ⅱ利用 溶液进行反萃取的原理:
溶液进行反萃取的原理:_______ 。
(5) 具有碱性,可与
具有碱性,可与 结合生成
结合生成 ,其中氮原子的杂化类型为
,其中氮原子的杂化类型为_______ 从结构角度分析,它比 配位能力
配位能力_______ (“强”或“弱”),过程Ⅳ中先用过量的 将水层2中
将水层2中 转化为
转化为 并生成
并生成 ,反应的离子方程式为
,反应的离子方程式为_______ ,得到的 再被
再被 氧化为
氧化为 。
。
(6)以 溶液作为吸收剂对燃煤烟气进行一体化“脱硫”、“脱硝”。控制溶液的
溶液作为吸收剂对燃煤烟气进行一体化“脱硫”、“脱硝”。控制溶液的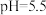 ,将烟气中的
,将烟气中的 、
、 转化为
转化为 、
、 ,均为放热反应。
,均为放热反应。
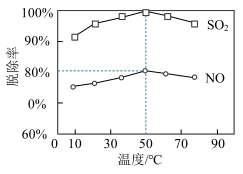
①一定时间内,温度对硫、硝脱除率的影响曲线如下图, 的脱除率高于
的脱除率高于 ,可能的原因是
,可能的原因是_______ (写出1种即可)。
②烟气中 和
和 的体积比为
的体积比为 ,
, 时的脱除率见图,则此吸收液中烟气转化生成的
时的脱除率见图,则此吸收液中烟气转化生成的 和
和 的物质的量之比为
的物质的量之比为_______ 。
 等重要物质的工艺流程如下。
等重要物质的工艺流程如下。
已知:i:伯胺
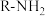 能与
能与 反应:
反应: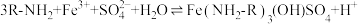 生成易溶于煤油的产物。
生成易溶于煤油的产物。ii:
 在水溶液中易与
在水溶液中易与 反应:
反应: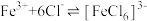
(1)写出过程I中
 发生反应的离子方程式:
发生反应的离子方程式:(2)过程Ⅱ加入过量
 的作用是
的作用是(3)过程Ⅱ加入伯胺-煤油对浸取液进行分离,该操作的名称是
(4)从化学平衡角度解释过程Ⅱ利用
 溶液进行反萃取的原理:
溶液进行反萃取的原理:(5)
 具有碱性,可与
具有碱性,可与 结合生成
结合生成 ,其中氮原子的杂化类型为
,其中氮原子的杂化类型为 配位能力
配位能力 将水层2中
将水层2中 转化为
转化为 并生成
并生成 ,反应的离子方程式为
,反应的离子方程式为 再被
再被 氧化为
氧化为 。
。(6)以
 溶液作为吸收剂对燃煤烟气进行一体化“脱硫”、“脱硝”。控制溶液的
溶液作为吸收剂对燃煤烟气进行一体化“脱硫”、“脱硝”。控制溶液的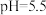 ,将烟气中的
,将烟气中的 、
、 转化为
转化为 、
、 ,均为放热反应。
,均为放热反应。①一定时间内,温度对硫、硝脱除率的影响曲线如下图,
 的脱除率高于
的脱除率高于 ,可能的原因是
,可能的原因是②烟气中
 和
和 的体积比为
的体积比为 ,
, 时的脱除率见图,则此吸收液中烟气转化生成的
时的脱除率见图,则此吸收液中烟气转化生成的 和
和 的物质的量之比为
的物质的量之比为
您最近一年使用:0次
解答题-工业流程题
|
困难
(0.15)
名校
【推荐3】碳酸锰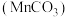 是制造电信器材软磁铁氧体的重要原料。工业上用硫锰矿(主要成分为
是制造电信器材软磁铁氧体的重要原料。工业上用硫锰矿(主要成分为 ,还含少量
,还含少量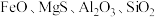 等)制备高纯
等)制备高纯 的流程如下:
的流程如下:
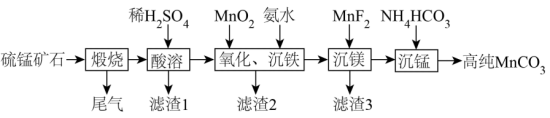
已知:(1)室温下,部分金属氢氧化物的 如下表:
如下表:
(2)室温下,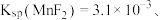
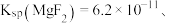
 。
。
回答下列问题:
(1) 中,S元素位于元素周期表的
中,S元素位于元素周期表的______ 区,基态 原子中能量最高的电子所占的轨道形状是
原子中能量最高的电子所占的轨道形状是______ ,其电子云在空间有______ 个取向。基态 的电子排布式为
的电子排布式为______ 。
(2)为了提高硫锰矿在空气中“煅烧”的反应速率,可采取的措施是____________ (任写一种)“尾气”中含有由“煅烧”生成的有害气体的化学式为______ 。
(3)加入 主要是氧化酸性溶液中的
主要是氧化酸性溶液中的 ,发生反应的离子方程式为
,发生反应的离子方程式为______ 。
(4)加入氨水调节溶液 为5.0,则溶液中
为5.0,则溶液中
______ (填“>”“<”或“=”)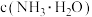 ;溶液中能够完全沉淀的金属离子为
;溶液中能够完全沉淀的金属离子为______ (填离子符号,金属离子浓度 时,视为沉淀完全)。
时,视为沉淀完全)。
(5)室温下“沉镁”时,离子反应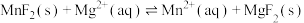 的化学平衡常数
的化学平衡常数
______ 。
(6)加入 “沉锰”时发生反应的离子方程式为
“沉锰”时发生反应的离子方程式为______ ,“沉锰”时控制溶液的 不能过高或过低,原因是
不能过高或过低,原因是______ .
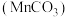 是制造电信器材软磁铁氧体的重要原料。工业上用硫锰矿(主要成分为
是制造电信器材软磁铁氧体的重要原料。工业上用硫锰矿(主要成分为 ,还含少量
,还含少量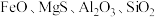 等)制备高纯
等)制备高纯 的流程如下:
的流程如下:
已知:(1)室温下,部分金属氢氧化物的
 如下表:
如下表:物质 |
|
|
|
|
|
|
|
|
|
|
|

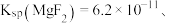
 。
。回答下列问题:
(1)
 中,S元素位于元素周期表的
中,S元素位于元素周期表的 原子中能量最高的电子所占的轨道形状是
原子中能量最高的电子所占的轨道形状是 的电子排布式为
的电子排布式为(2)为了提高硫锰矿在空气中“煅烧”的反应速率,可采取的措施是
(3)加入
 主要是氧化酸性溶液中的
主要是氧化酸性溶液中的 ,发生反应的离子方程式为
,发生反应的离子方程式为(4)加入氨水调节溶液
 为5.0,则溶液中
为5.0,则溶液中
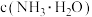 ;溶液中能够完全沉淀的金属离子为
;溶液中能够完全沉淀的金属离子为 时,视为沉淀完全)。
时,视为沉淀完全)。(5)室温下“沉镁”时,离子反应
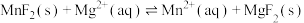 的化学平衡常数
的化学平衡常数
(6)加入
 “沉锰”时发生反应的离子方程式为
“沉锰”时发生反应的离子方程式为 不能过高或过低,原因是
不能过高或过低,原因是
您最近一年使用:0次
解答题-工业流程题
|
困难
(0.15)
名校
解题方法
【推荐1】五氧化二钒用作有机化工的催化剂。从废钒催化剂(主要成分为V2O5、V2O4、K2SO4、SiO2、Fe2O3和Al2O3)中回收V2O5,既避免污染环境又有利于资源综合利用,该工艺流程如下:
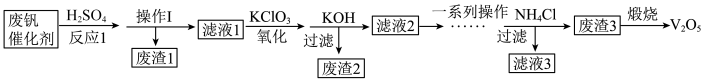
已知:金属钒的氧化物能与酸反应;SiO2不溶于水也不溶于初中常见的酸。回答下列问题:
(1)实验室进行操作Ⅰ时,需要用到的玻璃仪器有漏斗、烧杯和___________ 。
(2)加入KClO3的作用是将VO2+转化为VO ,则该转化过程中钒元素的化合价分别为
,则该转化过程中钒元素的化合价分别为___________ 。
(3)加入KOH的作用之一是保证钒存在于溶液中时,把Fe3+与Al3+转化为沉淀,则“废渣2”的主要成分是___________ 。
(4)滤渣3的成分是偏钒酸铵(NH4VO3)沉淀,煅烧偏钒酸铵(NH4VO3)还有氨气和水生成,写出“煅烧”过程中发生反应的化学方程式:___________ 。
(5)25℃时,取样进行实验分析,得到钒沉淀率和溶液pH之间关系如下表:
结合上表,在实际生产中,加入氯化铵调节溶液的最佳pH范围为___________ 。

已知:金属钒的氧化物能与酸反应;SiO2不溶于水也不溶于初中常见的酸。回答下列问题:
(1)实验室进行操作Ⅰ时,需要用到的玻璃仪器有漏斗、烧杯和
(2)加入KClO3的作用是将VO2+转化为VO
 ,则该转化过程中钒元素的化合价分别为
,则该转化过程中钒元素的化合价分别为(3)加入KOH的作用之一是保证钒存在于溶液中时,把Fe3+与Al3+转化为沉淀,则“废渣2”的主要成分是
(4)滤渣3的成分是偏钒酸铵(NH4VO3)沉淀,煅烧偏钒酸铵(NH4VO3)还有氨气和水生成,写出“煅烧”过程中发生反应的化学方程式:
(5)25℃时,取样进行实验分析,得到钒沉淀率和溶液pH之间关系如下表:
| pH | 1.3 | 1.4 | 1.5 | 1.6 | 1.7 | 1.8 | 1.9 | 2.0 | 2.1 |
| 钒沉淀率/% | 88.1 | 94.8 | 96.5 | 98.0 | 98.8 | 98.8 | 96.4 | 93.1 | 89.3 |
您最近一年使用:0次
解答题-工业流程题
|
困难
(0.15)
【推荐2】氧化铈(CeO2)是一种应用非常广 泛的稀土氧化物。现以氟碳铺矿(含CeFCO3、BaO、SiO2等)为原料制备氧化铈,其工艺流程如图所示:
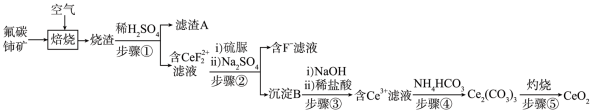
已知:
①稀土离子易与 形成复盐沉淀,Ce3+和
形成复盐沉淀,Ce3+和 发生反应:Ce2(SO4)3+ Na2SO4 +nH2O=Ce2(SO4)3·Na2SO4·nH2O↓;
发生反应:Ce2(SO4)3+ Na2SO4 +nH2O=Ce2(SO4)3·Na2SO4·nH2O↓;
②硫脲: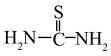 具有还原性,酸性条件下易被氧化为(SCN2H3)2;
具有还原性,酸性条件下易被氧化为(SCN2H3)2;
③Ce3+在空气中易被氧化为Ce4+,两者均能形成氢氧化物沉淀;
④Ce2(CO3)2为白色粉末,难溶于水。
回答下列问题:
(1)滤渣A的主要成分是_______ (填写化学式)。
(2)在另一种生产工艺中,在氟碳铈矿矿石粉中加入碳酸氢钠同时通入氧气焙烧,焙烧得到NaF和CeO2两种固体以及两种高温下的气态物质,请写出焙烧过程中相应的化学方程式_______ 。
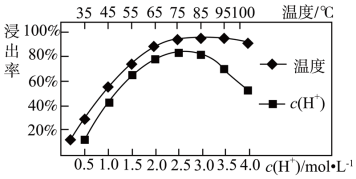
(3)焙烧后加入稀硫酸浸出,Ce的浸出率和稀硫酸浓度、温度有关,其关系如图所示,图示中H+浓度大于2.5mol·L-1时,浸出率降低的原因是_______ 。
(4)加入硫脲的目的是将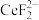 还原为Ce3+,反应的 离子方程式为
还原为Ce3+,反应的 离子方程式为_______ 。
(5)步骤③加入盐酸后,通常还需加入另一种化学试剂X,根据题中信息推测,加入X的作用为_______ 。
(6)下列关于步骤④的说法错误的是_______ (填字 母)。
(7)取所得产品CeO2 8.00g溶解后配成250mL溶液。取25.00 mL该溶液用0.20 mol·L-1硫酸亚铁铵[(NH4)2Fe(SO4)2]溶液滴定,滴定时发生反应Fe2++Ce4+=Fe3+ +Ce3+,达到滴定终点时消耗硫酸亚铁铵溶液20.50mL,则该产品的纯度为_______ 。(保留两位小数)。

已知:
①稀土离子易与
 形成复盐沉淀,Ce3+和
形成复盐沉淀,Ce3+和 发生反应:Ce2(SO4)3+ Na2SO4 +nH2O=Ce2(SO4)3·Na2SO4·nH2O↓;
发生反应:Ce2(SO4)3+ Na2SO4 +nH2O=Ce2(SO4)3·Na2SO4·nH2O↓;②硫脲:
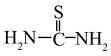 具有还原性,酸性条件下易被氧化为(SCN2H3)2;
具有还原性,酸性条件下易被氧化为(SCN2H3)2;③Ce3+在空气中易被氧化为Ce4+,两者均能形成氢氧化物沉淀;
④Ce2(CO3)2为白色粉末,难溶于水。
回答下列问题:
(1)滤渣A的主要成分是
(2)在另一种生产工艺中,在氟碳铈矿矿石粉中加入碳酸氢钠同时通入氧气焙烧,焙烧得到NaF和CeO2两种固体以及两种高温下的气态物质,请写出焙烧过程中相应的化学方程式
(3)焙烧后加入稀硫酸浸出,Ce的浸出率和稀硫酸浓度、温度有关,其关系如图所示,图示中H+浓度大于2.5mol·L-1时,浸出率降低的原因是

(4)加入硫脲的目的是将
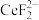 还原为Ce3+,反应的 离子方程式为
还原为Ce3+,反应的 离子方程式为(5)步骤③加入盐酸后,通常还需加入另一种化学试剂X,根据题中信息推测,加入X的作用为
(6)下列关于步骤④的说法错误的是_______ (填字 母)。
A.该步骤发生的反应是2Ce3+ +6 =Ce2(CO3)3↓ +3CO2↑+3H2O =Ce2(CO3)3↓ +3CO2↑+3H2O |
| B.可以用(NH4)2CO3溶液代替NH4 HCO3溶液,不影响产品纯度 |
| C.过滤时选择减压过滤能够大大提高过滤效率 |
| D.过滤后的滤液中仍含有较多Ce3+,需要将滤液循环以提高产率 |
您最近一年使用:0次
【推荐3】四氧化三锰是一种重要的电子和新能源基础原材料,可以用于生产软磁锰锌铁氧体、锂电正极材料锰酸锂和负温度系数热敏电阻等。以软锰矿(主要成分为 还含少量Fe、Si、Al等的氧化物)和硫铁矿(主要成分
还含少量Fe、Si、Al等的氧化物)和硫铁矿(主要成分 )为原料制备大颗粒的电池
)为原料制备大颗粒的电池 。
。
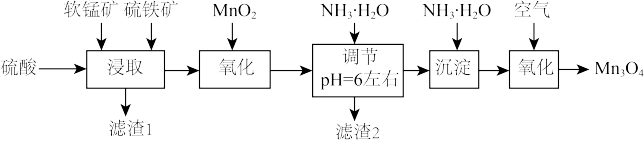
说明:
Ⅰ.“浸取”:研究发现,酸浸时 和
和 颗粒反应的原理如图1所示(部分产物未标出)。
颗粒反应的原理如图1所示(部分产物未标出)。
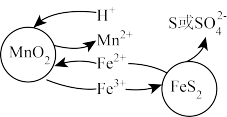
图1
Ⅱ.通空气“氧化”:将“沉淀”步骤所得含少量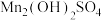 的
的 固体滤出,洗净,加水打成浆,浆液边加热边持续通入空气,制得
固体滤出,洗净,加水打成浆,浆液边加热边持续通入空气,制得 。
。
Ⅲ.氢氧化物形式完全沉淀时溶液的pH见表:
(1)滤渣1中主要成分的化学式为_______ 。
(2)随硫铁矿的增加,锰的浸出率降低,可能的原因是_______ 。
(3)写出“浸取”时 与
与 反应的离子方程式为
反应的离子方程式为_______ 。
(4)加入 “氧化”的目的是
“氧化”的目的是_______ 。
(5)检验“沉淀”已洗净的操作是_______ 。
(6)“沉淀”加热通空气过程中溶液pH随时间变化如图2所示,其中pH先基本不变后迅速下降的原因是_______ 。
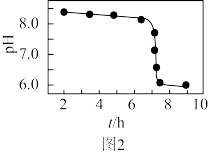
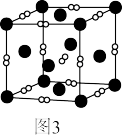
(7)一个立方体结构的 晶胞如图3所示,距离
晶胞如图3所示,距离 最近的
最近的 有
有_______ 个,已知阿伏加德罗数值为 ,则
,则 的晶体密度为
的晶体密度为 ,则晶胞的边长为
,则晶胞的边长为_______ nm(用含ρ、 的代数式表示)。
的代数式表示)。
 还含少量Fe、Si、Al等的氧化物)和硫铁矿(主要成分
还含少量Fe、Si、Al等的氧化物)和硫铁矿(主要成分 )为原料制备大颗粒的电池
)为原料制备大颗粒的电池 。
。
说明:
Ⅰ.“浸取”:研究发现,酸浸时
 和
和 颗粒反应的原理如图1所示(部分产物未标出)。
颗粒反应的原理如图1所示(部分产物未标出)。
图1
Ⅱ.通空气“氧化”:将“沉淀”步骤所得含少量
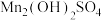 的
的 固体滤出,洗净,加水打成浆,浆液边加热边持续通入空气,制得
固体滤出,洗净,加水打成浆,浆液边加热边持续通入空气,制得 。
。Ⅲ.氢氧化物形式完全沉淀时溶液的pH见表:
| 沉淀物 |  |  |  |  |
| 开始沉淀的pH | 3.4 | 2.2 | 6.3 | 8.1 |
| 完全沉淀的pH | 5.2 | 3.2 | 9.7 | 10.4 |
(2)随硫铁矿的增加,锰的浸出率降低,可能的原因是
(3)写出“浸取”时
 与
与 反应的离子方程式为
反应的离子方程式为(4)加入
 “氧化”的目的是
“氧化”的目的是(5)检验“沉淀”已洗净的操作是
(6)“沉淀”加热通空气过程中溶液pH随时间变化如图2所示,其中pH先基本不变后迅速下降的原因是

(7)一个立方体结构的
 晶胞如图3所示,距离
晶胞如图3所示,距离 最近的
最近的 有
有 ,则
,则 的晶体密度为
的晶体密度为 ,则晶胞的边长为
,则晶胞的边长为 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
解答题-工业流程题
|
困难
(0.15)
解题方法
【推荐1】金属钒及其化合物有着广泛的应用,现有如下回收利用含钒催化剂[含有V2O5、VOSO4(强电解质)及不溶性残渣]的工艺的主要流程:
部分含钒物质在水中的溶解性如下表所示:
请回答下列问题:
(1)工业上常用铝热反应由V2O5冶炼金属钒,化学方程式为__________ 。
(2)反应①、②、③、④中,发生氧化还原反应的是__________ (填序号),写出反应①的离子方程式____ 。操作1、操作2用到的玻璃仪器是___________ 。
(3)反应③的沉淀率(又称沉钒率)是回收钒的关键之一,下图是反应温度与沉钒率的关系图,则控制温度的方法是_____________ 。
(4)反应④在焙烧过程中随温度的升高发生了两步反应。已知234gNH4VO3固体质量的减少值△W随温度(T)变化的曲线如图。试写出300℃~350℃时反应的化学方程式___________ 。
(5)全钒电池的电解质溶液为VOSO4溶液,电池的工作原理为VO2++V2++2H+ VO2++H2O+V3+。电池充电时阳极的电极反应式为
VO2++H2O+V3+。电池充电时阳极的电极反应式为____________ 。

部分含钒物质在水中的溶解性如下表所示:
| 物质 | VOSO4 | V2O5 | NH4VO3 | (VO2)2SO4 | HVO3 |
| 溶解性 | 可溶 | 难溶 | 难溶 | 易溶 | 难溶 |
请回答下列问题:
(1)工业上常用铝热反应由V2O5冶炼金属钒,化学方程式为
(2)反应①、②、③、④中,发生氧化还原反应的是
(3)反应③的沉淀率(又称沉钒率)是回收钒的关键之一,下图是反应温度与沉钒率的关系图,则控制温度的方法是

(4)反应④在焙烧过程中随温度的升高发生了两步反应。已知234gNH4VO3固体质量的减少值△W随温度(T)变化的曲线如图。试写出300℃~350℃时反应的化学方程式
(5)全钒电池的电解质溶液为VOSO4溶液,电池的工作原理为VO2++V2++2H+
 VO2++H2O+V3+。电池充电时阳极的电极反应式为
VO2++H2O+V3+。电池充电时阳极的电极反应式为
您最近一年使用:0次
解答题-工业流程题
|
困难
(0.15)
【推荐2】1902年德国化学家哈博研究出合成氨的方法,其反应原理为:
N2(g)+3H2(g) 2NH3(g);△H(△H<0)
2NH3(g);△H(△H<0)
一种工业合成氨的简易流程图如下:

完成下列填空:
(1)天然气中的H2S杂质常用氨水吸收,产物为NH4HS。一定条件下向NH4HS溶液中通入空气,得到单质硫并使吸收液再生。NH4HS的电子式是___________ ,写出再生反应的化学方程式:__________________ 。NH3的沸点高于H2S,是因为NH3分子之间存在着一种比_________ 力更强的作用力。
(2)室温下,0.1 mol/L的氯化铵溶液和0.1 mol/L的硫酸氢铵溶液,酸性更强的是_______ ,其原因是___________________________________________________________ 。
已知:H2SO4:H2SO4 = H++HSO4-;
HSO4- H++SO42- :
H++SO42- :
K =1.2×10-2 NH3·H2O:K=1.8×10-5
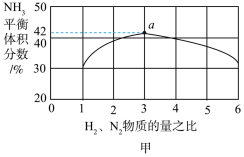
(3)图甲表示500℃、60.0MPa条件下,原料气投料比与平衡时NH3体积分数的关系。根据图中a点数据计算N2的平衡体积分数:______ (保留3位有效数字)。
(4)依据温度对合成氨反应的影响,在图乙坐标系中,画出一定条件下的密闭容器内,从常温下通入原料气开始,随温度不断升高,NH3物质的量变化的曲线示意图。

(5)上述流程图中,使合成氨放出的能量得到充分利用的主要步骤是(填序号)________ 。
简述本流程中提高合成氨原料总转化率的方法(只答一种即可):_________________ 。
N2(g)+3H2(g)
 2NH3(g);△H(△H<0)
2NH3(g);△H(△H<0)一种工业合成氨的简易流程图如下:

完成下列填空:
(1)天然气中的H2S杂质常用氨水吸收,产物为NH4HS。一定条件下向NH4HS溶液中通入空气,得到单质硫并使吸收液再生。NH4HS的电子式是
(2)室温下,0.1 mol/L的氯化铵溶液和0.1 mol/L的硫酸氢铵溶液,酸性更强的是
已知:H2SO4:H2SO4 = H++HSO4-;
HSO4-
 H++SO42- :
H++SO42- :K =1.2×10-2 NH3·H2O:K=1.8×10-5
(3)图甲表示500℃、60.0MPa条件下,原料气投料比与平衡时NH3体积分数的关系。根据图中a点数据计算N2的平衡体积分数:
(4)依据温度对合成氨反应的影响,在图乙坐标系中,画出一定条件下的密闭容器内,从常温下通入原料气开始,随温度不断升高,NH3物质的量变化的曲线示意图。


(5)上述流程图中,使合成氨放出的能量得到充分利用的主要步骤是(填序号)
简述本流程中提高合成氨原料总转化率的方法(只答一种即可):
您最近一年使用:0次
解答题-原理综合题
|
困难
(0.15)
解题方法
【推荐3】运用化学反应原理研究碳、氮、硫的化合物的反应对缓解环境污染、能源危机具有重要意义。
(1)汽车尾气脱硝脱碳主要原理为2NO(g) + 2CO(g) N2(g) + 2CO2(g) ΔH <0。
N2(g) + 2CO2(g) ΔH <0。
①该反应在______ (填“低温”或“高温”)下可自发反应。
②一定条件下的密闭容器中,充入10 mol CO和8 mol NO, 发生上述反应,如图为平衡时NO的体积分数与温度、压强的关系。

Ⅰ.该反应达到平衡后,为在提高反应速率同时提高NO的转化率,可采取的措施有______ (填字母序号)。
a.缩小容器的体积 b.改用高效催化剂
c.升高温度 d.增加CO的浓度
Ⅱ.压强为10 MPa、温度为T1下,若反应进行到30 min达到平衡状态,容器的体积为4L,该温度下平衡常数Kp=______ (压强以MPa为单位进行计算,用平衡分压代替平衡浓度计算,分压=总压×物质的量分数;保留两位有效数字)。
③氨气易溶于水可电离出 NH4+和 OH-、易液化,液氨也与水一样发生微弱的双聚电离,但比水弱,能溶解一些金属等性质。下列说法中不正确的是_______
a.NH3可看作比水弱的电解质
b.NH3的双聚电离可表示为:2NH3 NH4++NH2-
NH4++NH2-
c.NH3易溶于水是由于与水形成氢键
d.NH3可与Na 反应: 2NH3+2Na=2NaNH2+H2↑
(2)冶金工业、硝酸工业的废气废液中含氮化合物污染严重,必须处理达标后才能排放。用活性炭处理工厂尾气中的氮氧化物。
①已知:Ⅰ. 4NH3(g)+5O2(g)=4NO(g)+6H2O(l) ΔH1=a kJ·mol-1
Ⅱ. 4NH3(g)+3O2(g)=2N2(g)+6H2O(l) ΔH2=b kJ·mol-1
Ⅲ. C(s)+O2(g)=CO2(g) ΔH3=c kJ·mol-1
则反应C(s)+2NO(g) N2(g)+CO2(g)的ΔH =
N2(g)+CO2(g)的ΔH =_____ kJ·mol-1(用a、 b 、c表示)。
②在容积不变的密闭容器中,一定量的NO与足量的C发生反应:C(s)+2NO(g) N2(g)+CO2(g) ΔH=Q kJ·mol-1,平衡时c(NO)与温度T的关系如图所示,下列说法正确的是
N2(g)+CO2(g) ΔH=Q kJ·mol-1,平衡时c(NO)与温度T的关系如图所示,下列说法正确的是______ 。

a.其他条件不变,容器内压强不再改变时,反应达到平衡状态
b.温度为T2时,若反应体系处于状态D,则此时v正>v逆
c.该反应的Q>0,所以T1、T2、T3对应的平衡常数:K1<K2<K3
d.若状态B、C、D体系的压强分别为p(B)、p(C)、p(D),则p(D)=p(C)>p(B)
③已知某温度时,反应C(s)+2NO(g) N2(g)+CO2(g)的平衡常数K=9/16,在该温度下的2 L密闭容器中投入足量的活性炭和2.0 mol NO发生反应,t1时刻达到平衡,请在图中画出反应过程中c(NO)随时间t的变化曲线。
N2(g)+CO2(g)的平衡常数K=9/16,在该温度下的2 L密闭容器中投入足量的活性炭和2.0 mol NO发生反应,t1时刻达到平衡,请在图中画出反应过程中c(NO)随时间t的变化曲线。

____________
④工业上实际处理废气时,常用活性炭作催化剂,用NH3还原NO,同时通入一定量的O2以提高处理效果。当n(NH3)=n(NO)时,写出体系中总反应的化学方程式:__________________ 。
(1)汽车尾气脱硝脱碳主要原理为2NO(g) + 2CO(g)
 N2(g) + 2CO2(g) ΔH <0。
N2(g) + 2CO2(g) ΔH <0。①该反应在
②一定条件下的密闭容器中,充入10 mol CO和8 mol NO, 发生上述反应,如图为平衡时NO的体积分数与温度、压强的关系。

Ⅰ.该反应达到平衡后,为在提高反应速率同时提高NO的转化率,可采取的措施有
a.缩小容器的体积 b.改用高效催化剂
c.升高温度 d.增加CO的浓度
Ⅱ.压强为10 MPa、温度为T1下,若反应进行到30 min达到平衡状态,容器的体积为4L,该温度下平衡常数Kp=
③氨气易溶于水可电离出 NH4+和 OH-、易液化,液氨也与水一样发生微弱的双聚电离,但比水弱,能溶解一些金属等性质。下列说法中不正确的是
a.NH3可看作比水弱的电解质
b.NH3的双聚电离可表示为:2NH3
 NH4++NH2-
NH4++NH2-c.NH3易溶于水是由于与水形成氢键
d.NH3可与Na 反应: 2NH3+2Na=2NaNH2+H2↑
(2)冶金工业、硝酸工业的废气废液中含氮化合物污染严重,必须处理达标后才能排放。用活性炭处理工厂尾气中的氮氧化物。
①已知:Ⅰ. 4NH3(g)+5O2(g)=4NO(g)+6H2O(l) ΔH1=a kJ·mol-1
Ⅱ. 4NH3(g)+3O2(g)=2N2(g)+6H2O(l) ΔH2=b kJ·mol-1
Ⅲ. C(s)+O2(g)=CO2(g) ΔH3=c kJ·mol-1
则反应C(s)+2NO(g)
 N2(g)+CO2(g)的ΔH =
N2(g)+CO2(g)的ΔH =②在容积不变的密闭容器中,一定量的NO与足量的C发生反应:C(s)+2NO(g)
 N2(g)+CO2(g) ΔH=Q kJ·mol-1,平衡时c(NO)与温度T的关系如图所示,下列说法正确的是
N2(g)+CO2(g) ΔH=Q kJ·mol-1,平衡时c(NO)与温度T的关系如图所示,下列说法正确的是
a.其他条件不变,容器内压强不再改变时,反应达到平衡状态
b.温度为T2时,若反应体系处于状态D,则此时v正>v逆
c.该反应的Q>0,所以T1、T2、T3对应的平衡常数:K1<K2<K3
d.若状态B、C、D体系的压强分别为p(B)、p(C)、p(D),则p(D)=p(C)>p(B)
③已知某温度时,反应C(s)+2NO(g)
 N2(g)+CO2(g)的平衡常数K=9/16,在该温度下的2 L密闭容器中投入足量的活性炭和2.0 mol NO发生反应,t1时刻达到平衡,请在图中画出反应过程中c(NO)随时间t的变化曲线。
N2(g)+CO2(g)的平衡常数K=9/16,在该温度下的2 L密闭容器中投入足量的活性炭和2.0 mol NO发生反应,t1时刻达到平衡,请在图中画出反应过程中c(NO)随时间t的变化曲线。
④工业上实际处理废气时,常用活性炭作催化剂,用NH3还原NO,同时通入一定量的O2以提高处理效果。当n(NH3)=n(NO)时,写出体系中总反应的化学方程式:
您最近一年使用:0次
解答题-实验探究题
|
困难
(0.15)
名校
【推荐1】某小组探究Na2SO3溶液和KIO3溶液的反应。
实验I:向某浓度的KIO3酸性溶液(过量)中加入Na2SO3溶液(含淀粉),一段时间(t秒)后,溶液突然变蓝。
资料:IO3-在酸性溶液氧化I-,反应为IO3- + 5I- + 6H+ = 3I2 + 3H2O
(1)溶液变蓝,说明Na2SO3具有_________ 性。
(2)针对t秒前溶液未变蓝,小组做出如下假设:
i.t秒前未生成I2,是由于反应的活化能______ (填“大”或“小”),反应速率慢导致的。
ii.t秒前生成了I2,但由于存在Na2SO3,_____ (用离子方程式表示),I2被消耗。
(3)下述实验证实了假设ii合理。
实验II:向实验I的蓝色溶液中加入_______ ,蓝色迅速消失,后再次变蓝。
(4)进一步研究Na2SO3溶液和KIO3溶液反应的过程,装置如下。
实验III:K闭合后,电流表的指针偏转情况记录如下表:
① K闭合后,取b极区溶液加入盐酸酸化的BaCl2溶液,现象是______ 。
② 0~t1时,从a极区取溶液于试管中,滴加淀粉溶液,溶液变蓝;直接向a极区滴加淀粉溶液,溶液未变蓝。判断IO3-在a极放电的产物是_______ 。
③ 结合反应解释t2~t3时指针回到“0”处的原因:________ 。
(5)综合实验I、II、III,下列说法正确的是_______ 。
A.对比实验I、II,t秒后溶液变蓝,I中SO32-被完全氧化
B.对比实验I、III,t秒前IO3- 未发生反应
C.实验III中指针返回X处的原因,可能是I2氧化SO32-
实验I:向某浓度的KIO3酸性溶液(过量)中加入Na2SO3溶液(含淀粉),一段时间(t秒)后,溶液突然变蓝。
资料:IO3-在酸性溶液氧化I-,反应为IO3- + 5I- + 6H+ = 3I2 + 3H2O
(1)溶液变蓝,说明Na2SO3具有
(2)针对t秒前溶液未变蓝,小组做出如下假设:
i.t秒前未生成I2,是由于反应的活化能
ii.t秒前生成了I2,但由于存在Na2SO3,
(3)下述实验证实了假设ii合理。
实验II:向实验I的蓝色溶液中加入
(4)进一步研究Na2SO3溶液和KIO3溶液反应的过程,装置如下。
实验III:K闭合后,电流表的指针偏转情况记录如下表:
| 表盘 |  |  | ||
| 时间/min | 0~t1 | t2~t3 | t4 | |
| 偏转 位置 | 右偏至Y | 指针回到“0”处,又返至“X”处;如此周期性往复多次…… | 指针 归零 | |
② 0~t1时,从a极区取溶液于试管中,滴加淀粉溶液,溶液变蓝;直接向a极区滴加淀粉溶液,溶液未变蓝。判断IO3-在a极放电的产物是
③ 结合反应解释t2~t3时指针回到“0”处的原因:
(5)综合实验I、II、III,下列说法正确的是
A.对比实验I、II,t秒后溶液变蓝,I中SO32-被完全氧化
B.对比实验I、III,t秒前IO3- 未发生反应
C.实验III中指针返回X处的原因,可能是I2氧化SO32-
您最近一年使用:0次
解答题-实验探究题
|
困难
(0.15)
【推荐2】实验室中用下列装置制FeCl3,可供选择的试剂有:①MnO2 ②NaOH溶液 ③饱和NaCl溶液 ④浓硫酸 ⑤浓盐酸。
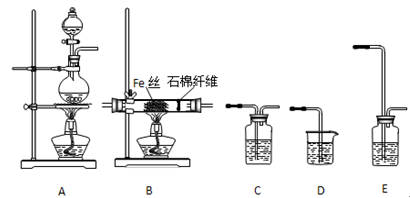
按气体流向由左到右排列,各装置的连接顺序为(填写A—E序号):
( ) 接( ) 接( ) 接( ) 接( )
(2)装置连接好后,应该首先进行的实验操作是________________ 。
(3)A装置烧瓶中反应的离子方程式是_________________________ 。
(4)E中盛装的试剂是____________ ,其作用是_____________________ 。
(5)停止反应后,还有铁丝剩余。为检验FeCl3生成,并最终得到FeCl3溶液,甲同学设计以下实验步骤:
a.待B装置玻璃管冷却后,将管中物质用水溶解,除去不溶物;
b.取少量滤液,滴加溶液,溶液呈现红色,以此检验Fe3+;
c.取少量滤液,滴加硝酸酸化的AgNO3溶液,检验Cl-。
①采取的操作方法是______ ;②中所加试剂为__________ 。
(6)乙同学认为甲的实验设计不能最终得到FeCl3溶液,其理由是(写出相应的离子反应方程式)_____________________ 。
你认为还选择下列哪些试剂才能制得较为纯净的FeCl3溶液( ) 。
E.HNO3
F.盐酸
G.O3

按气体流向由左到右排列,各装置的连接顺序为(填写A—E序号):
(2)装置连接好后,应该首先进行的实验操作是
(3)A装置烧瓶中反应的离子方程式是
(4)E中盛装的试剂是
(5)停止反应后,还有铁丝剩余。为检验FeCl3生成,并最终得到FeCl3溶液,甲同学设计以下实验步骤:
a.待B装置玻璃管冷却后,将管中物质用水溶解,除去不溶物;
b.取少量滤液,滴加溶液,溶液呈现红色,以此检验Fe3+;
c.取少量滤液,滴加硝酸酸化的AgNO3溶液,检验Cl-。
①采取的操作方法是
(6)乙同学认为甲的实验设计不能最终得到FeCl3溶液,其理由是(写出相应的离子反应方程式)
你认为还选择下列哪些试剂才能制得较为纯净的FeCl3溶液
| A.KMnO4(H+) |
| B.Fe |
| C.H2O2 |
| D.Cl2 |
F.盐酸
G.O3
您最近一年使用:0次
解答题-实验探究题
|
困难
(0.15)
【推荐3】某实验小组的同学为了探究CuSO4溶液与Na2CO3溶液的反应原理并验证产物,进行如下实验。
实验I:将CuSO4溶液与Na2CO3溶液混合,一定温度下充分反应至不产生气泡为止,
过滤、冷水洗涤、低温干燥,得到蓝绿色固体。该小组同学猜想此固体为xCuCO3·yCu(OH)2。
(1)为了验证猜想,先进行定性实验。
(2)为进一步确定蓝绿色固体的组成,使用如下装置再进行定量实验。

实验Ⅲ:称取5.190g样品,充分加热至不再产生气体为止,并使分解产生的气体全部进入装置C和D中。
①装置C中盛放的试剂是________________ ,装置E的作用是____________________ ,反应结束时要通入适量的空气,其作用是____________________________________ 。
②实验结束后,测得装置C增重0.270g,装置D增重1.320g。则该蓝绿色固体的化学式为____________ 。
(3)若x=y=1,写出CuSO4溶液与Na2CO3溶液混合时反应的化学方程式______________ 。
(4)已知20℃时溶解度数据:S[Ca(OH)2] =" 0.16" g,S[Ba(OH)2] =" 3.89" g。有同学据此提出可将装置D中的澄清石灰水换成等体积的饱和Ba(OH)2溶液,其可能的依据之一是_________________________ 。
(5)有同学为了降低实验误差,提出如下建议,其中合理的是______ (填字母序号)。
A.加热装置B前,先通空气一段时间后再称量C、D的初始质量
B.将D换为盛有碱石灰的U形管
C.将C、D颠倒并省去E装置
实验I:将CuSO4溶液与Na2CO3溶液混合,一定温度下充分反应至不产生气泡为止,
过滤、冷水洗涤、低温干燥,得到蓝绿色固体。该小组同学猜想此固体为xCuCO3·yCu(OH)2。
(1)为了验证猜想,先进行定性实验。
| 实验序号 | 实验步骤 | 实验现象 | 结论 |
| 实验Ⅱ | 取适量蓝绿色固体,加入足量稀硫酸 | 固体溶解,生成蓝色溶液, | 蓝绿色固体中含有CO32- |

实验Ⅲ:称取5.190g样品,充分加热至不再产生气体为止,并使分解产生的气体全部进入装置C和D中。
①装置C中盛放的试剂是
②实验结束后,测得装置C增重0.270g,装置D增重1.320g。则该蓝绿色固体的化学式为
(3)若x=y=1,写出CuSO4溶液与Na2CO3溶液混合时反应的化学方程式
(4)已知20℃时溶解度数据:S[Ca(OH)2] =" 0.16" g,S[Ba(OH)2] =" 3.89" g。有同学据此提出可将装置D中的澄清石灰水换成等体积的饱和Ba(OH)2溶液,其可能的依据之一是
(5)有同学为了降低实验误差,提出如下建议,其中合理的是
A.加热装置B前,先通空气一段时间后再称量C、D的初始质量
B.将D换为盛有碱石灰的U形管
C.将C、D颠倒并省去E装置
您最近一年使用:0次