名校
1 . 下列关于铁及其化合物的叙述中,错误的是
| A.铁是地壳中含量最多的金属元素 |
| B.铁具有延展性和导热性,可制作炊具 |
| C.Fe2O3是一种红棕色粉末,俗称铁红,常用作红色颜料 |
| D.Fe3O4是具有磁性的黑色晶体,铁的化合价有+2价和+3价 |
您最近一年使用:0次
2023-03-01更新
|
505次组卷
|
5卷引用:山西运城盐湖五中2023-2024学年高一上学期期末练兵卷(一)化学试题
2 . 人类很早就学会了使用铁器。下列某同学对铁元素的认识中正确的是
| A.铁有两种不溶于水的氢氧化物 | B.铁在自然界中不存在单质形态 |
| C.元素是地壳中含量最多的金属元素 | D.自然界存在的铁元素均显+3价 |
您最近一年使用:0次
3 . 在生产和生活中,钢铁和铝合金已经成为大量使用的金属材料,下列说法错误的是
| A.钢铁的主要成分为铁 |
| B.在地壳中,铝的含量高于铁 |
| C.一定条件下,单质铝可与铁的某种化合物发生置换反应 |
| D.铝餐具可用来长时间存放酸性食物 |
您最近一年使用:0次
解题方法
4 . X、Y、Z、W、Q五种元素的原子序数依次增大,X原子的半径最小;Y的单质在空气中含量最大;元素Z的焰色在浓雾中最具穿透性;含元素W的化合物很多具有漂白性;Q是最常见金属,位于周期表过渡区。回答问题:
(1)X与Z的化合物 与水反应转移的电子数为
与水反应转移的电子数为____________ 。
(2)用Y的某化合物可检查输送液态W单质的管道是否泄漏,其化学方程式为____________ 。
(3)检查某常见固体物质为 的操作为
的操作为_______________ 。
(4)Q位于周期表的第_________ 周期第________ 族,其单质 溶于
溶于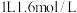 稀硝酸中(只被还原为
稀硝酸中(只被还原为 )的化学方程式为
)的化学方程式为______________ 。
(1)X与Z的化合物
 与水反应转移的电子数为
与水反应转移的电子数为(2)用Y的某化合物可检查输送液态W单质的管道是否泄漏,其化学方程式为
(3)检查某常见固体物质为
 的操作为
的操作为(4)Q位于周期表的第
 溶于
溶于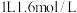 稀硝酸中(只被还原为
稀硝酸中(只被还原为 )的化学方程式为
)的化学方程式为
您最近一年使用:0次
解题方法
5 . 铁是一种应用广泛的金属。下列有关铁的叙述正确的是
| A.铁是地壳中含量最多的金属 | B.铁丝在氧气中燃烧生成氧化铁 |
| C.用铁可以回收硝酸银废液中的银 | D.炼铁就是把铁矿石变成纯净的氧化铁 |
您最近一年使用:0次
名校
6 . 某小组进行“铁与水蒸气”反应的产物及其性质探究系列实验。请回答实验中的问题:
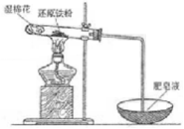
(1)写出该反应的化学方程式__________ ,若16.8g铁粉参加反应,转移电子数目为_____ 。
(2)待试管冷却后,取少许其中的固体物质溶于稀盐酸得溶液A,取所得液滴加KSCN溶液,溶液无颜色变化,说明硬质试管中固体物质的成分是_______ 溶液未变红色的原因是___________ (用离子方程式表示)。
(3)若要使(2)中所得溶液变红又不增加溶液离子种类,可以加入适量____ 试剂。
(4)另取(2)中溶液A,加入NaOH溶液,观察到生成白色絮状沉淀并迅速变成灰绿色,最后变成红褐色。沉淀转化过程发生的反应方程式为______________ 。
(5)某催化剂(主要成分FeO、Fe2O3)中+2价铁与+3价铁的物质的量之比为1:2时,其催化活性最高,此时铁的氧化物的混合物中铁的质量分数为________ (用小数表示,保留两位小数)。

(1)写出该反应的化学方程式
(2)待试管冷却后,取少许其中的固体物质溶于稀盐酸得溶液A,取所得液滴加KSCN溶液,溶液无颜色变化,说明硬质试管中固体物质的成分是
(3)若要使(2)中所得溶液变红又不增加溶液离子种类,可以加入适量
(4)另取(2)中溶液A,加入NaOH溶液,观察到生成白色絮状沉淀并迅速变成灰绿色,最后变成红褐色。沉淀转化过程发生的反应方程式为
(5)某催化剂(主要成分FeO、Fe2O3)中+2价铁与+3价铁的物质的量之比为1:2时,其催化活性最高,此时铁的氧化物的混合物中铁的质量分数为
您最近一年使用:0次
7 . 下列关于金属的说法不正确的是( )
| A.钠在空气中燃烧时,先熔化,再燃烧,生成淡黄色固体 |
| B.铝是地壳中含量最多的金属元素,铝在空气中受热熔化,剧烈燃烧 |
| C.铁在潮湿的空气中生成的氧化物疏松多孔,无法保护内层金属 |
| D.商代后期铸造出工艺精湛的后(司)母戊鼎,该鼎的用料属于有色金属材料 |
您最近一年使用:0次
2018-12-26更新
|
209次组卷
|
2卷引用:【全国百强校】山西省太原市第五中学2018-2019学年高一上学期12月月考化学试题
8 . 铁、铜混合粉末20.0g加入到100mL 5.0 mol·L-1FeCl3溶液中,剩余固体质量为5.2g(忽略反应前后溶液体积变化)。求:
(1)反应后溶液中FeCl2的物质的量浓度_____________ mol·L-1
(2)原固体混合物中铜的质量分数是_____________
(1)反应后溶液中FeCl2的物质的量浓度
(2)原固体混合物中铜的质量分数是
您最近一年使用:0次
2017-02-23更新
|
338次组卷
|
3卷引用:山西省晋中市祁县中学校2020届高三上学期10月月考化学试题
名校
9 . 铁元素在地壳中的含量丰富。关于铁及其化合物的说法错误的是( )
| A.铁合金是使用最早的合金 | B.Fe2O3 常用作红色油漆的原料 |
| C.Fe(OH)3 胶体可做净水剂 | D.Fe3O4 是具有磁性的黑色晶体 |
您最近一年使用:0次
2018-12-25更新
|
170次组卷
|
2卷引用:【全国百强校】山西省实验中学2018-2019学年高一上学期12月月考化学试题
10 . 如图中,A、B、C、D、E是单质,G、H、I、F是B、C、D、E分别和A形成的二元化合物.已知:①反应C+G B+H能放出大量的热,该反应曾应用于铁轨的焊接;②I是一种常见的温室气体,它和E可以发生反应:2E+I
B+H能放出大量的热,该反应曾应用于铁轨的焊接;②I是一种常见的温室气体,它和E可以发生反应:2E+I 2F+D,F中的E元素的质量分数为60%.回答问题:
2F+D,F中的E元素的质量分数为60%.回答问题:
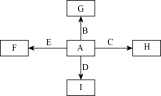
(1)① 中反应的化学方程式为________________________ ;
(2)化合物Ⅰ的电子式为____________ ,它的空间构型是______________ ;
(3)1.6g G 溶于盐酸,得到的溶液与铜粉完全反应,计算至少所需铜粉的质量_____________ (写出离子方程式和计算过程);
(4)C与过量NaOH溶液反应的离子方程式为___________________ ,反应后溶液与过量化合物Ⅰ反应的离子方程式为__________________ ;
(5)E在I中燃烧观察到的现象是_____________________ 。
 B+H能放出大量的热,该反应曾应用于铁轨的焊接;②I是一种常见的温室气体,它和E可以发生反应:2E+I
B+H能放出大量的热,该反应曾应用于铁轨的焊接;②I是一种常见的温室气体,它和E可以发生反应:2E+I 2F+D,F中的E元素的质量分数为60%.回答问题:
2F+D,F中的E元素的质量分数为60%.回答问题:
(1)① 中反应的化学方程式为
(2)化合物Ⅰ的电子式为
(3)1.6g G 溶于盐酸,得到的溶液与铜粉完全反应,计算至少所需铜粉的质量
(4)C与过量NaOH溶液反应的离子方程式为
(5)E在I中燃烧观察到的现象是
您最近一年使用:0次
2016-12-09更新
|
271次组卷
|
2卷引用:山西省阳高县第一中学2018届高三上学期第二次月考化学试题



