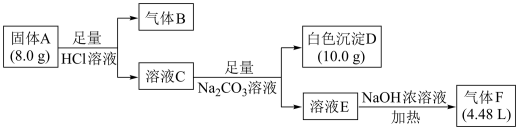
如图中,A、B、C、D、E是单质,G、H、I、F是B、C、D、E分别和A形成的二元化合物.已知:①反应C+G B+H能放出大量的热,该反应曾应用于铁轨的焊接;②I是一种常见的温室气体,它和E可以发生反应:2E+I
B+H能放出大量的热,该反应曾应用于铁轨的焊接;②I是一种常见的温室气体,它和E可以发生反应:2E+I 2F+D,F中的E元素的质量分数为60%.回答问题:
2F+D,F中的E元素的质量分数为60%.回答问题:
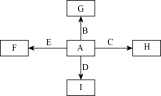
(1)① 中反应的化学方程式为________________________ ;
(2)化合物Ⅰ的电子式为____________ ,它的空间构型是______________ ;
(3)1.6g G 溶于盐酸,得到的溶液与铜粉完全反应,计算至少所需铜粉的质量_____________ (写出离子方程式和计算过程);
(4)C与过量NaOH溶液反应的离子方程式为___________________ ,反应后溶液与过量化合物Ⅰ反应的离子方程式为__________________ ;
(5)E在I中燃烧观察到的现象是_____________________ 。
 B+H能放出大量的热,该反应曾应用于铁轨的焊接;②I是一种常见的温室气体,它和E可以发生反应:2E+I
B+H能放出大量的热,该反应曾应用于铁轨的焊接;②I是一种常见的温室气体,它和E可以发生反应:2E+I 2F+D,F中的E元素的质量分数为60%.回答问题:
2F+D,F中的E元素的质量分数为60%.回答问题:
(1)① 中反应的化学方程式为
(2)化合物Ⅰ的电子式为
(3)1.6g G 溶于盐酸,得到的溶液与铜粉完全反应,计算至少所需铜粉的质量
(4)C与过量NaOH溶液反应的离子方程式为
(5)E在I中燃烧观察到的现象是
更新时间:2016-12-09 14:35:27
|
相似题推荐
【推荐1】I.由三种元素组成的化合物X,按如下流程进行实验。相同条件下,非金属氧化物A的密度是氢气的22倍。B是强碱、焰色反应为黄色,气体C能使湿润的红色石蕊试纸变蓝,气体E是空气的主要成分。单质G是一种高强度、抗腐蚀的稀有金属。

请回答:
(1)组成X的三种元素_______ ,D的化学式_______ 。
(2)单质F制备单质G的化学方程式是_______ 。
(3)化合物X与非金属氧化物A反应的化学方程式是_______ 。
II.某同学设计了如下实验装置,进行浓硫酸与蔗糖的反应实验。

请回答:
(1)实验开始时,先在烧瓶中加入15g蔗糖,并滴入几滴水使蔗糖完全湿润,然后从分液漏斗中加入15 mL浓硫酸,水的作用是__ 。
(2)为了检验实验中产生的 ,A、C试管中的试剂分别是
,A、C试管中的试剂分别是_______ 、_______ 。(可供选用的药品:酸性高锰酸钾溶液、 溶液、澄清石灰水、酚酞试剂)
溶液、澄清石灰水、酚酞试剂)

请回答:
(1)组成X的三种元素
(2)单质F制备单质G的化学方程式是
(3)化合物X与非金属氧化物A反应的化学方程式是
II.某同学设计了如下实验装置,进行浓硫酸与蔗糖的反应实验。

请回答:
(1)实验开始时,先在烧瓶中加入15g蔗糖,并滴入几滴水使蔗糖完全湿润,然后从分液漏斗中加入15 mL浓硫酸,水的作用是
(2)为了检验实验中产生的
 ,A、C试管中的试剂分别是
,A、C试管中的试剂分别是 溶液、澄清石灰水、酚酞试剂)
溶液、澄清石灰水、酚酞试剂)
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐2】一定条件下经不同的化学反应,可以实现图示变化,A为酸式盐;B为无色无味气体;无色气体D可使红色石蕊试纸变蓝:X、F和Y为气体单质,且Y为有色气体,F为空气的主要成分之一;G为正盐,G和无色气体M在溶液中可反应生成B。
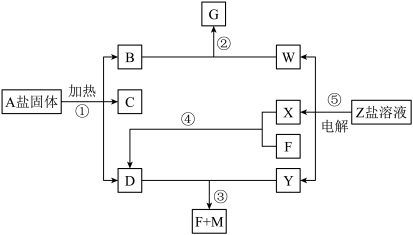
(1)写出下列物质的化学式:A___________ ;Y___________
(2)写出反应⑤的离子方程式___________ 。
(3)写出反应③的化学方程式___________ 。
(4)常温下pH=10,体积均为100mL的D、W两溶液与M反应,消耗的M的物质的量关系D___________ W(填“大于”“小于”或“等于”)。

(1)写出下列物质的化学式:A
(2)写出反应⑤的离子方程式
(3)写出反应③的化学方程式
(4)常温下pH=10,体积均为100mL的D、W两溶液与M反应,消耗的M的物质的量关系D
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐1】某科研小组探究工业废Cu粉(杂质可能含有SiO2、Al2O3、Fe2O3中的一种或几种)的组成并制备少量CuSO4·5H2O,实现废物综合利用。他们进行了两组实验,过程如下:
Ⅰ:
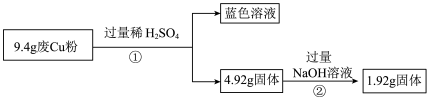
Ⅱ:
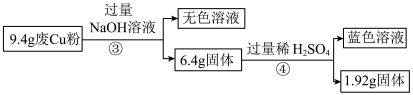
(1)废Cu粉中含有的杂质是________________ 。
(2)分别写出过程①③中发生反应的离子方程式:
①________________________________ 。
③________________________________ 。
(3)综合过程Ⅰ、II,计算工业废Cu粉中各成分的质量之比是________ (可不必化简)。
(4)已知25℃时:
从Ⅱ中所得蓝色溶液中分离提纯得到CuSO4·5H2O晶体,需要经过下列步骤:
a、向蓝色溶液中加入一定量的H2O2溶液;
b、调节溶液的pH为__________ 之间;
c、然后过滤、结晶,再过滤,可得CuSO4·5H2O
下列关于实验操作的叙述中,正确的是__________ (填字母)。
A.H2O2是绿色氧化剂,在氧化过程中不引进杂质、不产生污染
B.将Fe2+氧化为Fe3+的主要原因是Fe(OH)2沉淀比Fe(OH)3沉淀较难过滤
C.上述步骤c中第一次过滤是为了得到滤液,第二次过滤是为了得到固体
D.在pH >4的溶液中Fe3+一定不能大量存在
Ⅰ:

Ⅱ:

(1)废Cu粉中含有的杂质是
(2)分别写出过程①③中发生反应的离子方程式:
①
③
(3)综合过程Ⅰ、II,计算工业废Cu粉中各成分的质量之比是
(4)已知25℃时:
| 电解质 | Cu(OH)2 | Fe(OH)2 | Fe(OH)3 |
| 开始沉淀时的pH | 5.4 | 6.5 | 3.5 |
| 完全沉淀时的pH | 6.4 | 9.6 | 4.0 |
从Ⅱ中所得蓝色溶液中分离提纯得到CuSO4·5H2O晶体,需要经过下列步骤:
a、向蓝色溶液中加入一定量的H2O2溶液;
b、调节溶液的pH为
c、然后过滤、结晶,再过滤,可得CuSO4·5H2O
下列关于实验操作的叙述中,正确的是
A.H2O2是绿色氧化剂,在氧化过程中不引进杂质、不产生污染
B.将Fe2+氧化为Fe3+的主要原因是Fe(OH)2沉淀比Fe(OH)3沉淀较难过滤
C.上述步骤c中第一次过滤是为了得到滤液,第二次过滤是为了得到固体
D.在pH >4的溶液中Fe3+一定不能大量存在
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
【推荐2】长余辉材料在发光照明、交通等领域具有广泛的应用前景。下图是一种利用大理石(主要成分CaCO3和MgCO3)和铝土矿(主要成分Al2O3,还含少量Fe2O3杂质)制备一种长余辉材料(Ca12Al14Ox)的工艺流程图。回答下列问题:
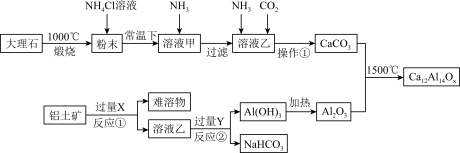
(1)Ca12Al14Ox中x的数值为______ ,试剂X的名称是_________ 。
(2)NH4Cl溶液能溶解“粉末”的原因是_________ ,发生的主要反应的化学方程为______ 。
(3)反应②的离子方程式为_______ 。
(4)实验室加热Al(OH)3应在________ (填仪器名称)进行;操作①包括_____ 、干燥等。
(5)若溶液甲中c(Mg2+) <5×10-5mol•L-1元素损失,此时应调节溶液pH大于______ ,为减少钙元素损失,应控制溶液甲中c(Ca2+)≤______ 。常温下Ksp[Mg(OH)2]=5×10-11,Ksp[Ca(OH)2]=5×10-6。

(1)Ca12Al14Ox中x的数值为
(2)NH4Cl溶液能溶解“粉末”的原因是
(3)反应②的离子方程式为
(4)实验室加热Al(OH)3应在
(5)若溶液甲中c(Mg2+) <5×10-5mol•L-1元素损失,此时应调节溶液pH大于
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐3】某油脂厂废弃的油脂加氢镍催化剂主要含金属Ni、Al、Fe及其氧化物,还有少量其他不溶性物质。采用如下工艺流程回收其中的镍制备硫酸镍晶体( ):
):

某温度下,溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
回答下列问题:
(1)“碱浸”中NaOH的作用除了去除催化剂表面的油脂外,还具有作用是___________ (用化学方程式表示)。为回收金属,通常用稀硫酸将“滤液①”调为中性,生成沉淀,该沉淀的化学式为___________ 。
(2)“滤液②”中含有的金属离子除了“Ni2+”,还有___________ 。
(3)“转化”中加入 的主要作用是
的主要作用是___________ (用离子方程式表示)。
(4)利用上述表格数据,计算 的
的
___________ (列出计算式即可,不用化简)。如果“转化”后的溶液中 浓度为
浓度为 ,则“调pH”应控制pH不超过
,则“调pH”应控制pH不超过___________ (填数值)。
 ):
):
某温度下,溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
| 金属离子 |  |  |  |  |
开始沉淀时( )的pH )的pH | 7.2 | 3.7 | 2.2 | 7.5 |
沉淀完全时( )的pH )的pH | 8.7 | 4.7 | 3.2 | 9.0 |
(1)“碱浸”中NaOH的作用除了去除催化剂表面的油脂外,还具有作用是
(2)“滤液②”中含有的金属离子除了“Ni2+”,还有
(3)“转化”中加入
 的主要作用是
的主要作用是(4)利用上述表格数据,计算
 的
的
 浓度为
浓度为 ,则“调pH”应控制pH不超过
,则“调pH”应控制pH不超过
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐1】铁、铜等金属及其化合物在日常生产生活中用途非常广泛.
Ⅰ.实验室欲制备0.3mol Cu(NO3)2晶体,甲、乙两同学分别设计实验方案如下:
甲:Cu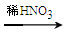 Cu(NO3)2 ;乙:Cu
Cu(NO3)2 ;乙:Cu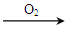 CuO
CuO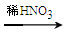 Cu(NO3)2
Cu(NO3)2
(1)从绿色化学的角度分析,___________ 同学的方案更合理
(2)乙同学实验时通入O2的速率不宜过大,为便于观察和控制产生O2的速率,宜选择__________ 装置(填字母序号)。
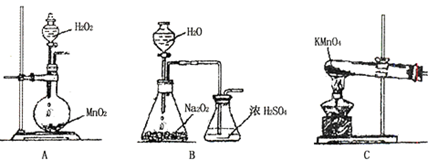
Ⅱ.某化学实验小组通过实验来探究一包黑色粉是否由Fe3O4、CuO组成探究过程如下:
(1)提出假设:
假设1.黑色粉末是CuO;
假设2.黑色粉末是Fe3O4;
假设3.黑色粉末是CuO和Fe3O4的混合物。
(2)设计探究实验:
取少量粉末放入足量稀硫酸中,在所得溶液中滴加KSCN试剂。
①若假设1成立,则实验现象是溶液显蓝色。
②若假设2或3成立,则实验现象是__________ 。
为进一步探究,继续向所得溶液加入足量铁粉,若产生_________ 的现象,则假设3成立。
有另一小组同学提出,若混合物中CuO含量较少,可能加入铁粉后实验现象不明显。
查阅资料:Cu2+与足量氨水反应生成深蓝色溶液,Cu2++4NH3·H2O=Cu(NH3)42++4H2O。
为探究是假设2还是假设3成立,另取少量粉末加稀硫酸充分溶解后,再加入足量氨水,若假设2成立,则产生__________ 现象;若假设3成立,则产生________ 现象。
Ⅲ.由Fe3O4、FeO、CuO、Fe组成的固体混合物,在加热条件下用足量的CO还原,得到金属混合物2.86g,将生成的CO2气体用足量的澄清石灰水吸收后,产生5.00g白色沉淀。固体混合物的质量是________ 。
Ⅰ.实验室欲制备0.3mol Cu(NO3)2晶体,甲、乙两同学分别设计实验方案如下:
甲:Cu
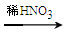 Cu(NO3)2 ;乙:Cu
Cu(NO3)2 ;乙:Cu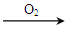 CuO
CuO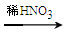 Cu(NO3)2
Cu(NO3)2(1)从绿色化学的角度分析,
(2)乙同学实验时通入O2的速率不宜过大,为便于观察和控制产生O2的速率,宜选择

Ⅱ.某化学实验小组通过实验来探究一包黑色粉是否由Fe3O4、CuO组成探究过程如下:
(1)提出假设:
假设1.黑色粉末是CuO;
假设2.黑色粉末是Fe3O4;
假设3.黑色粉末是CuO和Fe3O4的混合物。
(2)设计探究实验:
取少量粉末放入足量稀硫酸中,在所得溶液中滴加KSCN试剂。
①若假设1成立,则实验现象是溶液显蓝色。
②若假设2或3成立,则实验现象是
为进一步探究,继续向所得溶液加入足量铁粉,若产生
有另一小组同学提出,若混合物中CuO含量较少,可能加入铁粉后实验现象不明显。
查阅资料:Cu2+与足量氨水反应生成深蓝色溶液,Cu2++4NH3·H2O=Cu(NH3)42++4H2O。
为探究是假设2还是假设3成立,另取少量粉末加稀硫酸充分溶解后,再加入足量氨水,若假设2成立,则产生
Ⅲ.由Fe3O4、FeO、CuO、Fe组成的固体混合物,在加热条件下用足量的CO还原,得到金属混合物2.86g,将生成的CO2气体用足量的澄清石灰水吸收后,产生5.00g白色沉淀。固体混合物的质量是
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
【推荐2】Ⅰ.中学化学中几种常见物质的转化关系如图(部分产物未列出)。A是一种金属单质,D是一种非金属固体单质。
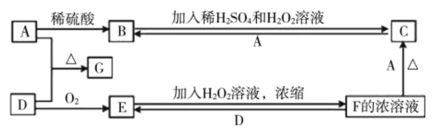
请回答下列问题:
(1)写出反应E+H2O2→F的化学方程式:___________ 。
(2)若反应F+D→E转移的电子数为3.01×1023,则消耗D的质量为___________ g。
Ⅱ.氮气是一种常见的气体,其在一定条件下可以转化为氮氧化物NO、NO2等。
(3)NO、NO2均为有毒气体,可以把NO、NO2一起通入氢氧化钠溶液中进行尾气处理,得到一种常见的食品添加剂。写出该过程发生的离子方程式:___________ 。
(4)把a g的Mg、Cu固体混合物加到足量的硝酸溶液中得到蓝色溶液和气体。所产生的气体与b L(标准状况)的O2一起通入水中得到只含硝酸的水溶液。往蓝色溶液中滴加氢氧化钠溶液至恰好完全沉淀,所得沉淀的质量为___________ g.(用a、b的代数式表示)
(5)金属Mg可以在NO2燃烧,产物可能为MgO、Mg3N2和N2,现有13.2g的Mg粉,在足量的NO2中充分燃烧,得到21.0g的固体和1120mL(标准状况)的气体。写出燃烧过程发生的化学方程式:___________ 。

请回答下列问题:
(1)写出反应E+H2O2→F的化学方程式:
(2)若反应F+D→E转移的电子数为3.01×1023,则消耗D的质量为
Ⅱ.氮气是一种常见的气体,其在一定条件下可以转化为氮氧化物NO、NO2等。
(3)NO、NO2均为有毒气体,可以把NO、NO2一起通入氢氧化钠溶液中进行尾气处理,得到一种常见的食品添加剂。写出该过程发生的离子方程式:
(4)把a g的Mg、Cu固体混合物加到足量的硝酸溶液中得到蓝色溶液和气体。所产生的气体与b L(标准状况)的O2一起通入水中得到只含硝酸的水溶液。往蓝色溶液中滴加氢氧化钠溶液至恰好完全沉淀,所得沉淀的质量为
(5)金属Mg可以在NO2燃烧,产物可能为MgO、Mg3N2和N2,现有13.2g的Mg粉,在足量的NO2中充分燃烧,得到21.0g的固体和1120mL(标准状况)的气体。写出燃烧过程发生的化学方程式:
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐3】X、Y、Z、W四种物质有如下相互转化关系(其中X、W为单质,Y、Z为化合物,未列出反应条件)

Ⅰ.若Z是生活中常用的调味品,W遇淀粉溶液变蓝,则:
(1)常温下,X的颜色是____________ 。
(2)工业上Z有多种用途,用化学方程式表示Z的一种用途_________________________ 。
(3)生活中所用的Z加入了碘酸钾,过量X与Y溶液反应时可以得到这种碘酸盐,此反应的离子方程式是______________________________________ 。
Ⅱ.若X是工业上用量最大的金属单质,Z是一种具有磁性的黑色晶体,则:
(1)X与Y反应的化学方程式是__________________________________ 。
(2)将3.48g Z加入50mL 4mol/L的稀HNO3中充分反应,产生112mL的NO(标准状况),向反应后的溶液中滴加NaOH溶液能产生沉淀.当沉淀量最多,至少需要加入2mol/L的NaOH溶液_____ mL (精确到0.1)。

Ⅰ.若Z是生活中常用的调味品,W遇淀粉溶液变蓝,则:
(1)常温下,X的颜色是
(2)工业上Z有多种用途,用化学方程式表示Z的一种用途
(3)生活中所用的Z加入了碘酸钾,过量X与Y溶液反应时可以得到这种碘酸盐,此反应的离子方程式是
Ⅱ.若X是工业上用量最大的金属单质,Z是一种具有磁性的黑色晶体,则:
(1)X与Y反应的化学方程式是
(2)将3.48g Z加入50mL 4mol/L的稀HNO3中充分反应,产生112mL的NO(标准状况),向反应后的溶液中滴加NaOH溶液能产生沉淀.当沉淀量最多,至少需要加入2mol/L的NaOH溶液
您最近一年使用:0次