1 . 杜甫诗句中“朱门酒肉臭,路有冻死骨”这里的“朱门”是指涂有_______的门。
A. | B. | C. | D. |
您最近一年使用:0次
解题方法
2 . 铁元素是人体必需的微量元素之一。口服补铁剂可治疗缺铁性贫血。其中多糖铁无论是吸收效果、口味还是副作用方面都比传统补铁剂更优秀。
某实验小组为研究多糖铁中铁元素的价态及其含量,设计并进行了如下实验:
【实验一】检验该补铁剂中铁元素的价态
Ⅰ、猜想与假设
同学甲:多糖铁中铁元素价态均为+2价
同学乙:多糖铁中铁元素价态均为+3价
(1)同学丙认为甲、乙猜测均不准确,他认为多糖铁中铁元素价态可能为______
Ⅱ、查阅资料
①多糖铁的化学式为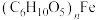 ,溶于盐酸时产生含铁元素的离子;
,溶于盐酸时产生含铁元素的离子;
②人体内血红蛋白中铁元素化合价为-+2价;
③ 遇
遇 会产生蓝色沉淀。
会产生蓝色沉淀。
Ⅲ、实验方案设计
可选用试剂:盐酸、酸性 溶液、NaOH溶液、KSCN溶液、
溶液、NaOH溶液、KSCN溶液、 溶液
溶液
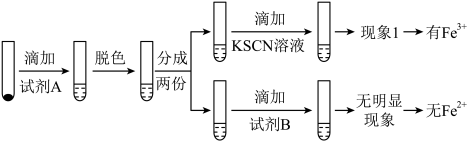
(2)试剂A为______ ;试剂B为______ 。
(3)现象1为:__________________ ;
Ⅳ、结果与讨论:多糖铁中铁元素的价态为+3价
(4)多糖铁与维生素C同时服用效果更好,试分析维生素C在这一过程中的作用是____________ 。
(5)有同学表示多糖铁在生产的过程中不能使用铜制容器,请用离子反应方程式说明原因:____________ 。
【实验二】测量该多糖铁补铁剂中铁元素的含量
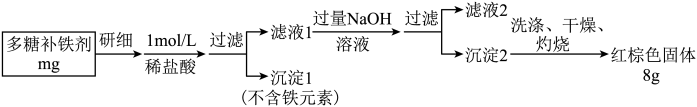
(6)请写出沉淀2转化成红棕色固体的化学方程式:____________ 。
(7)多糖补铁剂中铁元素的质量分数为______ (用a和m表示)
某实验小组为研究多糖铁中铁元素的价态及其含量,设计并进行了如下实验:
【实验一】检验该补铁剂中铁元素的价态
Ⅰ、猜想与假设
同学甲:多糖铁中铁元素价态均为+2价
同学乙:多糖铁中铁元素价态均为+3价
(1)同学丙认为甲、乙猜测均不准确,他认为多糖铁中铁元素价态可能为
Ⅱ、查阅资料
①多糖铁的化学式为
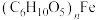 ,溶于盐酸时产生含铁元素的离子;
,溶于盐酸时产生含铁元素的离子;②人体内血红蛋白中铁元素化合价为-+2价;
③
 遇
遇 会产生蓝色沉淀。
会产生蓝色沉淀。Ⅲ、实验方案设计
可选用试剂:盐酸、酸性
 溶液、NaOH溶液、KSCN溶液、
溶液、NaOH溶液、KSCN溶液、 溶液
溶液
(2)试剂A为
(3)现象1为:
Ⅳ、结果与讨论:多糖铁中铁元素的价态为+3价
(4)多糖铁与维生素C同时服用效果更好,试分析维生素C在这一过程中的作用是
(5)有同学表示多糖铁在生产的过程中不能使用铜制容器,请用离子反应方程式说明原因:
【实验二】测量该多糖铁补铁剂中铁元素的含量

(6)请写出沉淀2转化成红棕色固体的化学方程式:
(7)多糖补铁剂中铁元素的质量分数为
您最近一年使用:0次
名校
3 . 铁作为生产、生活中的重要元素,下列方案设计、现象和结论均正确的是
| 目的 | 方案设计 | 现象和结论 | |
| A | 检验铁锈中是否含有二价铁 | 将铁锈溶于浓盐酸,滴入酸性 溶液 溶液 | 紫色褪去,说明铁锈中含有二价铁 |
| B | 制备 胶体 胶体 | 向沸水中滴入几滴饱和 溶液,继续煮沸至产生红褐色沉淀,并用激光笔照射 溶液,继续煮沸至产生红褐色沉淀,并用激光笔照射 | 丁达尔效应,产生了胶体 |
| C | 配制 溶液 溶液 | 将 固体溶于较浓的盐酸中,再加水稀释至所需的浓度 固体溶于较浓的盐酸中,再加水稀释至所需的浓度 | 得到黄色溶液 |
| D | 比较 和 和 的氧化性强弱 的氧化性强弱 | 取适量 溶液于试管中,滴入 溶液于试管中,滴入 溶液,振荡,观察现象 溶液,振荡,观察现象 | 若产生气体使带火星的木条复燃,说明 的氧化性强于 的氧化性强于 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
4 . 为探究FeCl3溶液和Na2SO3溶液混合后Fe3+发生怎样的化学反应,进行了如下实验(FeCl3和Na2SO3溶液浓度均为0.50mol·L-1)。
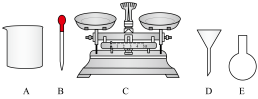
(1)由Na2SO3固体配制0.50mol·L-1Na2SO3溶液,需要的仪器除药匙、玻璃棒、容量瓶外,下列仪器中还需要___________ (填字母)。
(2)根据实验②的现象得出FeCl3溶液和Na2SO3溶液反应生成了___________ 。
(3)甲同学根据实验③中现象得出FeC13溶液和Na2SO3溶液发生了氧化还原反应,写出其相应的离子方程式:___________ 。
(4)乙同学认为实验③中现象不足以说明FeC13溶液和Na2SO3溶液发生了氧化还原反应,你认为该同学的理由是___________ ;请你帮助乙同学重新设计一个实验来证明FeCl3溶液和Na2SO3溶液发生了氧化还原反应:___________ (填操作及对应现象)。
(5)结论:该实验说明在该条件下Fe3+既发生了___________ 反应又发生了还原反应。
| 实验 | 操作与现象 |
| ① | 先向试管中加入10mLFeCl3溶液,再加入10mLNa2SO3溶液,振荡后发现试管中颜色由棕黄色变为红褐色(无气泡产生,也无沉淀生成)。 |
| ② | 用激光灯从侧面照射实验①得到的混合体系,观察到一条光亮的通路。 |
| ③ | 取实验①反应后的混合体系少许于试管中,先加入过量稀盐酸酸化后,再滴加氯化钡溶液,产生白色沉淀。 |
| ④ | 将实验①反应后的混合体系放置一小时后,溶液变为淡绿色。 |
(1)由Na2SO3固体配制0.50mol·L-1Na2SO3溶液,需要的仪器除药匙、玻璃棒、容量瓶外,下列仪器中还需要

(2)根据实验②的现象得出FeCl3溶液和Na2SO3溶液反应生成了
(3)甲同学根据实验③中现象得出FeC13溶液和Na2SO3溶液发生了氧化还原反应,写出其相应的离子方程式:
(4)乙同学认为实验③中现象不足以说明FeC13溶液和Na2SO3溶液发生了氧化还原反应,你认为该同学的理由是
(5)结论:该实验说明在该条件下Fe3+既发生了
您最近一年使用:0次
2023·河南郑州·三模
5 . 化学是一门以实验为基础的自然学科。以下实验项目是高中化学课程标准规定的四个学生必做实验,依据所提供的实验药品和仪器能完成实验项目的是
| 实验项目 | 实验药品 | 所用玻璃仪器 | |
| A | 配制100mL0.1mol·L-1的氯化钠溶液 | 氯化钠固体、蒸馏水 | 100mL容量瓶、烧杯、胶头滴管 |
| B | 探究Fe2+和Fe3+的氧化性和还原性 | FeSO4溶液、FeCl3溶液、氯水、KI溶液、KSCN溶液、锌片、淀粉溶液 | 试管、胶头滴管 |
| C | 探究不同价态硫元素之间的转化 | 铜片、稀H2SO4、浓H2SO3、Na2SO3溶液、氯水、Na2S溶液 | 试管、胶头滴管 |
| D | 用化学沉淀法去除粗盐中的杂质离子 | 粗食盐水、Na2CO3溶液、BaCl2溶液、NaOH溶液 | 烧杯、胶头滴管、试管表面皿、玻璃棒 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
6 . 金属及其化合物在人类生活、生产中发挥着重要的作用。
(1)中国四大发明之一的指南针由天然磁石制成,其主要成分是_______ (填化学式)。
(2)下列物质中属于合金的是_______。
(3)“84消毒液”有效成分是NaClO。某次实验需要使用 的NaClO溶液,欲用NaClO固体配制该溶液,实验中需要称量
的NaClO溶液,欲用NaClO固体配制该溶液,实验中需要称量_______ g NaClO晶体,下图列举的仪器中需要的有_______ 种(填写数目),若定容时俯视刻度线,则所配溶液浓度c_______  (填“>”、“=”或“<”)
(填“>”、“=”或“<”)

(4)工业上常用 溶液作为“腐蚀液”,刻制铜印刷电路板。写出
溶液作为“腐蚀液”,刻制铜印刷电路板。写出 溶液与金属铜发生反应的离子方程式:
溶液与金属铜发生反应的离子方程式:_______ 。
(5)向盛有氯化铁、氯化亚铁、氯化铜混合溶液的烧杯中加入铁粉和铜粉,反应结束后,下列结果不可能出现的是_______。
(1)中国四大发明之一的指南针由天然磁石制成,其主要成分是
(2)下列物质中属于合金的是_______。
| A.钢 | B.水银 | C.黄铜 | D.青铜 |
 的NaClO溶液,欲用NaClO固体配制该溶液,实验中需要称量
的NaClO溶液,欲用NaClO固体配制该溶液,实验中需要称量 (填“>”、“=”或“<”)
(填“>”、“=”或“<”)
(4)工业上常用
 溶液作为“腐蚀液”,刻制铜印刷电路板。写出
溶液作为“腐蚀液”,刻制铜印刷电路板。写出 溶液与金属铜发生反应的离子方程式:
溶液与金属铜发生反应的离子方程式:(5)向盛有氯化铁、氯化亚铁、氯化铜混合溶液的烧杯中加入铁粉和铜粉,反应结束后,下列结果不可能出现的是_______。
| A.有铜无铁 | B.有铁无铜 | C.铁、铜都有 | D.铁、铜都无 |
您最近一年使用:0次
解题方法
7 . 下列有关化学知识的叙述错误的是
| A.青铜属于合金 | B.纤维素属于有机高分子 |
| C.白醋可用于去除水壶中的水垢 | D. 可用作缺铁性贫血的补铁剂 可用作缺铁性贫血的补铁剂 |
您最近一年使用:0次
名校
8 . 下列对与颜色有关的化学过程的解释正确的是
| 实验 | 反应现象或事实 | 解释 |
| ① | 金属钠在空气燃烧,火焰呈黄色 | 生成的 为淡黄色固体 为淡黄色固体 |
| ② | 铁丝在 中燃烧有红棕色的烟 中燃烧有红棕色的烟 | 生成的 为红棕色固体 为红棕色固体 |
| ③ | 同一种粘土烧制的砖有红色和青色 | 铁元素化合价不同 |
| ④ | 铝热剂溶于足量盐酸,再加 溶液,溶液没出现红色 溶液,溶液没出现红色 | 铝热剂中一定不含三价铁 |
| A.①②③④ | B.①②④ | C.②③ | D.③④ |
您最近一年使用:0次
名校
9 . 已知 2FeCl3+Fe=3FeCl2。在 FeCl3 溶液中加入一定量的 Fe,当反应进行到氯化铁和氯化亚铁的质量分数相等时,求此刻已参加反应的氯化铁和剩余的氯化铁的质量比_______ 。(相对分子质量 FeCl3:162.5 FeCl2:127 )
您最近一年使用:0次
名校
解题方法
10 . 下列操作不能达到实验目的的是
| 实验目的 | 操作 | |
| A | 向锥形瓶中滴加半滴 溶液 溶液 | 控制液滴悬而不落,用锥形瓶内壁把液滴沾下来 |
| B | 检验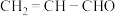 中含有碳碳双键 中含有碳碳双键 | 取少许丙烯醛滴加到盛有溴水的试管中 |
| C | 检验 溶液是否变质 溶液是否变质 | 取少量待测液于试管中,加入足量稀盐酸,再加入足量 溶液 溶液 |
| D | 探究 和 和 的反应存在一定的限度 的反应存在一定的限度 | 将 溶液与 溶液与  溶液混合,充分反应后分成两份,一份滴加几滴 溶液混合,充分反应后分成两份,一份滴加几滴 溶液,另一份滴加几滴淀粉溶液 溶液,另一份滴加几滴淀粉溶液 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-01-25更新
|
387次组卷
|
3卷引用:安徽省合肥市庐巢八校联考2022-2023学年高二下学期5月期中考试化学试题



