名校
解题方法
1 . 某小组以FeCl3溶液为研究对象,探究物质之间反应的多样性,进行了如下实验。
Ⅰ.探究FeCl3溶液中的离子平衡和离子反应。
(1)配制50 mL 1.0 mol/L的FeCl3溶液,测其pH约为0.7,即c(H+) = 0.2 mol/L。
①用化学用语解释FeCl3溶液呈酸性的原因___________ 。
②下列实验方案中,能使FeCl3溶液pH升高的是___________ 。
a.加水稀释 b.加入FeCl3固体 c.滴加浓KSCN溶液 d.加入NaHCO3固体
(2)小组同学利用上述FeCl3溶液探究其与足量锌粉的反应。实验操作及现象如下:
已知:Zn的性质与Al相似,能发生反应:Zn+2NaOH=Na2ZnO2+H2↑。
①结合实验现象和平衡移动原理解释出现红褐色沉淀的原因___________ 。
②用离子方程式解释反应后溶液为浅绿色的原因___________ 。
(3)为进一步探究上述1.0 mol/L FeCl3溶液中Fe3+和H+氧化性的相对强弱,继续实验并观察到反应开始时现象如下:
小组同学得出结论:在1.0mol/L FeCl3溶液中,Fe3+的氧化性比H+更强。
Ⅱ.探究FeCl3溶液与碱性物质之间的反应。
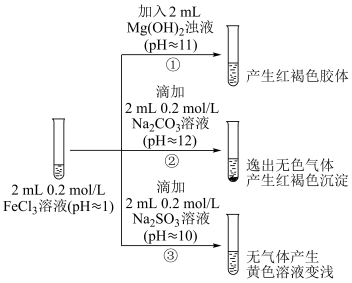
(4)②中逸出的无色气体是___________ (写化学式)。
(5)对于③中的实验现象,同学们有诸多猜测,继续进行实验:
ⅰ.甲组:取③中反应后溶液少许,滴入稀盐酸酸化,再滴加BaCl2溶液,产生白色沉淀。得出结论:FeCl3与Na2SO3发生了氧化还原反应,离子方程式是___________ 。
ⅱ.乙组:认为甲组的实验不严谨,重新设计并进行实验,证实了甲组的结论是正确的。其实验方案是___________ 。
(6)受上述实验启发,小组同学对pH≈8的1mol/L NaF溶液与FeCl3溶液混合时的现象产生了好奇并进行实验:
i.⑤的实验目的是___________ 。
ⅱ.为探究④中溶液变无色的原因,进行了如下实验:

资料显示: FeF3溶液为无色。
请用化学平衡移动原理解释红褐色沉淀产生的原因___________ 。
(7)根据以上实验,FeCl3溶液与碱性物质之间反应的多样性与___________ 有关。
Ⅰ.探究FeCl3溶液中的离子平衡和离子反应。
(1)配制50 mL 1.0 mol/L的FeCl3溶液,测其pH约为0.7,即c(H+) = 0.2 mol/L。
①用化学用语解释FeCl3溶液呈酸性的原因
②下列实验方案中,能使FeCl3溶液pH升高的是
a.加水稀释 b.加入FeCl3固体 c.滴加浓KSCN溶液 d.加入NaHCO3固体
(2)小组同学利用上述FeCl3溶液探究其与足量锌粉的反应。实验操作及现象如下:
| 操作 | 现象 |
| 向反应瓶中加入6.5g锌粉,然后加入50mL 1.0 mol/L的FeCl3溶液,搅拌 | 溶液温度迅速上升,稍后出现红褐色沉淀,同时出现少量气泡;反应一段时间后静置,上层溶液为浅绿色 |
| 收集检验反应过程中产生的气体 | 集气管口靠近火焰,有爆鸣声 |
①结合实验现象和平衡移动原理解释出现红褐色沉淀的原因
②用离子方程式解释反应后溶液为浅绿色的原因
(3)为进一步探究上述1.0 mol/L FeCl3溶液中Fe3+和H+氧化性的相对强弱,继续实验并观察到反应开始时现象如下:
| 操作 | 现象 |
| 将5 mL 1.0 mol/L的FeCl3溶液与0.65 g锌粉混合 | 溶液温度迅速上升,开始时几乎没有气泡 |
| 将 | 溶液中立即产生大量气泡 |
Ⅱ.探究FeCl3溶液与碱性物质之间的反应。

(4)②中逸出的无色气体是
(5)对于③中的实验现象,同学们有诸多猜测,继续进行实验:
ⅰ.甲组:取③中反应后溶液少许,滴入稀盐酸酸化,再滴加BaCl2溶液,产生白色沉淀。得出结论:FeCl3与Na2SO3发生了氧化还原反应,离子方程式是
ⅱ.乙组:认为甲组的实验不严谨,重新设计并进行实验,证实了甲组的结论是正确的。其实验方案是
(6)受上述实验启发,小组同学对pH≈8的1mol/L NaF溶液与FeCl3溶液混合时的现象产生了好奇并进行实验:
| 实验操作 及现象 | ④向2 mL 0.2 mol/LFeCl3溶液中滴入2 mL 1 mol/LNaF溶液,溶液变无色 |
| ⑤向2 mL 0.2 mol/LFeCl3溶液中滴入2 mL蒸馏水,溶液颜色变浅 |
ⅱ.为探究④中溶液变无色的原因,进行了如下实验:

资料显示: FeF3溶液为无色。
请用化学平衡移动原理解释红褐色沉淀产生的原因
(7)根据以上实验,FeCl3溶液与碱性物质之间反应的多样性与
您最近一年使用:0次



