1 . 下列实验操作和现象及所得结论均正确 的是
| 选项 | 实验操作和现象 | 结论 |
| A | 少量溶液X,向其中滴加少量NaOH溶液,瓶口湿润的红色石蕊试纸未变蓝 | 溶液中一定不含 |
| B | 取适量浓硝酸于试管中,将灼热的木炭插入试管,产生红棕色气体 | 浓硝酸与炭反应产生 |
| C | 室温下,向 溶液中滴加少量KI溶液,再滴加几滴淀粉溶液,溶液变蓝色 溶液中滴加少量KI溶液,再滴加几滴淀粉溶液,溶液变蓝色 | 氧化性: |
| D | 向 溶液中逐滴加入稀氨水至过量,产生白色沉淀,并逐渐增多,后慢慢溶解 溶液中逐滴加入稀氨水至过量,产生白色沉淀,并逐渐增多,后慢慢溶解 | 碱性: |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
解题方法
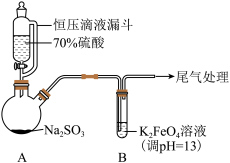
2 . 铸铁的主要成分为 和C,用下图所示实验研究铸铁与热的浓硫酸的反应(夹持和加热装置已略去)。
和C,用下图所示实验研究铸铁与热的浓硫酸的反应(夹持和加热装置已略去)。 、
、 ,他们依据的反应为
,他们依据的反应为 、
、___________ 。
(2)检测反应后A中所得溶液中含有 ,实验方案是取少量待测溶液,将其加入适量水中稀释,
,实验方案是取少量待测溶液,将其加入适量水中稀释,___________ 。
(3)实验现象证明A中确实有 、
、 生成。
生成。
①U型管a侧棉花的紫红色褪去,证明有___________ 生成。
②证明有 生成的实验现象是
生成的实验现象是___________ 。
(4)下列试剂中,也可用于该实验中检验 的是
的是___________ (填序号)。
a. 溶液 b.品红溶液 c.紫色石蕊溶液
溶液 b.品红溶液 c.紫色石蕊溶液
(5)取上述反应生成的0.56L(标准状况下)混合气体通入足量 溶液中,发生反应的化学方程式是
溶液中,发生反应的化学方程式是___________ ,反应完全后,向溶液中加入足量 溶液生成白色沉淀,分离、干燥后得到固体4.66g,混合气体中
溶液生成白色沉淀,分离、干燥后得到固体4.66g,混合气体中 的体积分数为
的体积分数为___________ 。
 和C,用下图所示实验研究铸铁与热的浓硫酸的反应(夹持和加热装置已略去)。
和C,用下图所示实验研究铸铁与热的浓硫酸的反应(夹持和加热装置已略去)。
 、
、 ,他们依据的反应为
,他们依据的反应为 、
、(2)检测反应后A中所得溶液中含有
 ,实验方案是取少量待测溶液,将其加入适量水中稀释,
,实验方案是取少量待测溶液,将其加入适量水中稀释,(3)实验现象证明A中确实有
 、
、 生成。
生成。①U型管a侧棉花的紫红色褪去,证明有
②证明有
 生成的实验现象是
生成的实验现象是(4)下列试剂中,也可用于该实验中检验
 的是
的是a.
 溶液 b.品红溶液 c.紫色石蕊溶液
溶液 b.品红溶液 c.紫色石蕊溶液(5)取上述反应生成的0.56L(标准状况下)混合气体通入足量
 溶液中,发生反应的化学方程式是
溶液中,发生反应的化学方程式是 溶液生成白色沉淀,分离、干燥后得到固体4.66g,混合气体中
溶液生成白色沉淀,分离、干燥后得到固体4.66g,混合气体中 的体积分数为
的体积分数为
您最近半年使用:0次
名校
解题方法
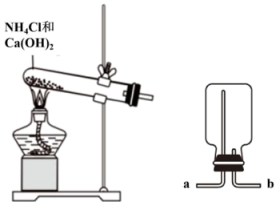
3 . 某化学实验小组同学利用如图所示装置制备氨气,并探究氨气的性质(部分仪器已略去)。___________ 。
(2)干燥氨气可选用的试剂是___________ (填序号)。
①浓H2SO4 ②碱石灰 ③P2O5
(3)收集氨气时,氨气的进气口为___________ (填“a”或“b”)。
(4)证明烧瓶中氨气集满的方法是___________ 。
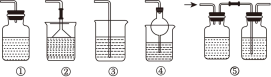
(5)为防止环境污染,下列装置中(盛放的液体均为水)可用于吸收多余氨气的是___________ (填序号)。___________ (填选项代号)。
a.装置Ⅰ中红色Fe2O3粉末变为黑色粉末,经检验是一种铁的氧化物
b.装置Ⅱ中无水CuSO4粉末变为蓝色
c.装置Ⅲ无水CaCl2的质量增加
d.生成一种无色无味气体,该气体无污染
(7)小组同学继续对(6)装置I反应后黑色粉末的组成进行探究。
(8)结合(6)(7)实验,写出(6)中NH3还原Fe2O3的化学方程式___________ 。
(2)干燥氨气可选用的试剂是
①浓H2SO4 ②碱石灰 ③P2O5
(3)收集氨气时,氨气的进气口为
(4)证明烧瓶中氨气集满的方法是
(5)为防止环境污染,下列装置中(盛放的液体均为水)可用于吸收多余氨气的是
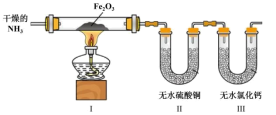
a.装置Ⅰ中红色Fe2O3粉末变为黑色粉末,经检验是一种铁的氧化物
b.装置Ⅱ中无水CuSO4粉末变为蓝色
c.装置Ⅲ无水CaCl2的质量增加
d.生成一种无色无味气体,该气体无污染
(7)小组同学继续对(6)装置I反应后黑色粉末的组成进行探究。
| 操作 | 现象 | 结论或离子方程式 |
| 步骤1:取少量黑色粉末于小烧杯中,加入过量盐酸 | 黑色粉末全部溶解,无气泡产生,溶液呈浅绿色 | 溶液中可能含有Fe2+ |
| 步骤2:取步骤1少量溶液于试管中,滴入2-3滴KSCN溶液,振荡 | 溶液颜色 | 溶液中不含有Fe3+ |
| 步骤3:向步骤2试管中滴入少量氯水 | 溶液变红色 | 涉及离子方程式有 Fe(SCN)3 Fe(SCN)3 |
您最近半年使用:0次
名校
4 . 氰化氢(HCN,一元弱酸,易挥发)主要应用于电镀、采矿、药物合成等工业生产。HCN,CN-能抑制人体组织细胞内酶的活性,不能直接排放到环境中。
(1)Na2S2O3在临床上常用于氰化物的解毒剂。解毒的原理是 将CN-转化为SCN-和
将CN-转化为SCN-和 。验证该转化过程中生成SCN-的实验方法是:向NaCN溶液中加入过量的Na2S2O3的溶液,充分反应后,取少量反应后的溶液于试管中,加入足量稀盐酸酸化,
。验证该转化过程中生成SCN-的实验方法是:向NaCN溶液中加入过量的Na2S2O3的溶液,充分反应后,取少量反应后的溶液于试管中,加入足量稀盐酸酸化,___________ 。
(2)Cu2+可催化过氧化氢氧化废水中的CN-。
①反应不能在酸性条件下进行,原因是___________ 。
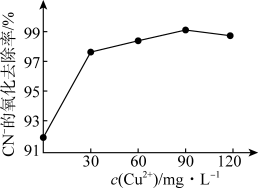
②在含氰废水总景、过氧化氢用量和溶液pH一定的情况下,反应相同时间,测得CN-的氧化去除率随c(Cu2+)的变化与如图所示。c(Cu2+)超过90mg·L-1时,CN-的氧化去除率有所下降,原因是___________ 。 ,其反应的离子方程式为
,其反应的离子方程式为___________ 。
(4)在铜镍为催化剂(Cu、CuO为活性组分,Cu的催化活性效果更好)的条件下,可利用反应:HCN(g)+H2O(g) NH3(g)+CO(g) △H>0
NH3(g)+CO(g) △H>0
除去废气中的HCN。将含相同比例的HCN(g)、H2O(g)、CO(g)[或N2(g)]混合气体分别通过催化剂,反应相同的时间,测得HCN(g)的去除率随温度变化如图所示。200℃时含CO的混合气体中HCN(g)的去除率较高,而400℃时含CO的混合气体中HCN(g)的去除率较低。其原因是___________ 。
(1)Na2S2O3在临床上常用于氰化物的解毒剂。解毒的原理是
 将CN-转化为SCN-和
将CN-转化为SCN-和 。验证该转化过程中生成SCN-的实验方法是:向NaCN溶液中加入过量的Na2S2O3的溶液,充分反应后,取少量反应后的溶液于试管中,加入足量稀盐酸酸化,
。验证该转化过程中生成SCN-的实验方法是:向NaCN溶液中加入过量的Na2S2O3的溶液,充分反应后,取少量反应后的溶液于试管中,加入足量稀盐酸酸化,(2)Cu2+可催化过氧化氢氧化废水中的CN-。
①反应不能在酸性条件下进行,原因是
②在含氰废水总景、过氧化氢用量和溶液pH一定的情况下,反应相同时间,测得CN-的氧化去除率随c(Cu2+)的变化与如图所示。c(Cu2+)超过90mg·L-1时,CN-的氧化去除率有所下降,原因是
 ,其反应的离子方程式为
,其反应的离子方程式为(4)在铜镍为催化剂(Cu、CuO为活性组分,Cu的催化活性效果更好)的条件下,可利用反应:HCN(g)+H2O(g)
 NH3(g)+CO(g) △H>0
NH3(g)+CO(g) △H>0除去废气中的HCN。将含相同比例的HCN(g)、H2O(g)、CO(g)[或N2(g)]混合气体分别通过催化剂,反应相同的时间,测得HCN(g)的去除率随温度变化如图所示。200℃时含CO的混合气体中HCN(g)的去除率较高,而400℃时含CO的混合气体中HCN(g)的去除率较低。其原因是

您最近半年使用:0次
名校
5 . 利用金属矿渣(含有FeS2、SiO2及Cu2O)制备FeCO3的实验流程如下。已知煅烧过程中FeS2和Cu2O转化为Fe2O3和CuO。___________ (写化学式),该物质是工业制备硅的原料,写出该物质与焦炭反应制备硅的化学方程式:___________ 。
(2)FeS2在空气中煅烧的化学方程式为___________ 。
(3)在“还原”步骤,在向酸浸后溶液加入过量铁屑,除了能将 转化为
转化为 外,还能
外,还能___________ 。若将6g铁粉加入200mLFe2(SO4)3和CuSO4的混合溶液中,充分反应得到200mL FeSO4溶液和5.2g固体沉淀物。
FeSO4溶液和5.2g固体沉淀物。
①5.2g固体沉淀物的成份为___________ (写化学式)。
②原Fe2(SO4)3溶液的物质的量浓度是___________ 。(写出计算过程)
(4)检验 是否完全被还原的实验操作是
是否完全被还原的实验操作是___________ 。
(5)制备FeCO3,写出“沉铁”步骤发生反应的离子方程式:___________ 。
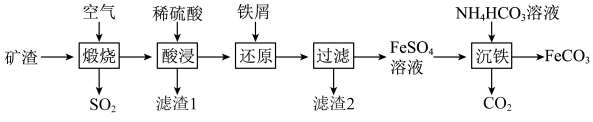
(2)FeS2在空气中煅烧的化学方程式为
(3)在“还原”步骤,在向酸浸后溶液加入过量铁屑,除了能将
 转化为
转化为 外,还能
外,还能 FeSO4溶液和5.2g固体沉淀物。
FeSO4溶液和5.2g固体沉淀物。①5.2g固体沉淀物的成份为
②原Fe2(SO4)3溶液的物质的量浓度是
(4)检验
 是否完全被还原的实验操作是
是否完全被还原的实验操作是(5)制备FeCO3,写出“沉铁”步骤发生反应的离子方程式:
您最近半年使用:0次
6 . 某固体粉末甲中可能含有K2CO3、KNO3、NaNO2、K2SO3、Na2SO4、Fe、FeO、Fe2O3中的若干种。某同学为确定该固体粉末的成分,取甲进行连续实验。实验过程及现象如下:
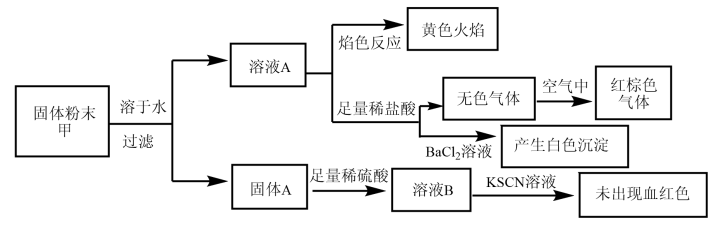
| A.固体粉末中含有钠元素,但不含钾元素 |
| B.固体粉末中无法确定是否含有K2SO3 |
| C.固体粉末中至少含有KNO3、NaNO2中的一种 |
| D.固体粉末中可能含有K2CO3、不含Fe2O3 |
您最近半年使用:0次
名校
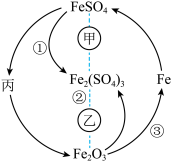
7 . 在一定条件下,某些物质具有如图所示的转化关系。丙为白色固体,其悬浊液在空气中会迅速变为灰绿色,最终变为红褐色。请回答下列问题:
(1)根据分析可知丙为________________ (填化学式);甲可能是__________ (填标号,下同),乙可能是__________ 。
A.稀硝酸 B. 溶液 C.
溶液 C. D.
D. 溶液
溶液
(2)实验室保存 溶液时,为了防止其被氧化,可以往溶液中加入适量
溶液时,为了防止其被氧化,可以往溶液中加入适量___________ (填药品名称);可以用______________ (填化学式)溶液来检验 溶液中的
溶液中的 是否被氧化。
是否被氧化。
(3)丙的悬浊液在空气中变色的原因为____________________ (填化学方程式);工业上高炉炼铁可以实现③的转化,所得到的炽热的铁水注入模具之前,模具必须进行充分的干燥处理,原因是____________________ (填化学方程式)。
(1)根据分析可知丙为
A.稀硝酸 B.
 溶液 C.
溶液 C. D.
D. 溶液
溶液(2)实验室保存
 溶液时,为了防止其被氧化,可以往溶液中加入适量
溶液时,为了防止其被氧化,可以往溶液中加入适量 溶液中的
溶液中的 是否被氧化。
是否被氧化。(3)丙的悬浊液在空气中变色的原因为
您最近半年使用:0次
2024-04-21更新
|
94次组卷
|
2卷引用:河北省保定市定州市第二中学2023-2024学年高一下学期3月月考化学试题
名校
解题方法
8 . 工业上以辉铋矿粉(主要成分是 ,含少量
,含少量 、
、 、
、 等杂质)为原料制备
等杂质)为原料制备 (铋酸钠,浅黄色不溶于冷水的固体,是常用试剂),流程如下:
(铋酸钠,浅黄色不溶于冷水的固体,是常用试剂),流程如下: 难溶于水;
难溶于水;
②酸浸后,矿粉中的硫元素完全变为硫单质;
回答下列问题:
(1) 中Cu的化合价为
中Cu的化合价为___________ ,酸浸过程中, 反应的离子方程式
反应的离子方程式___________ 。
(2)检验“酸浸”液中是否含 ,可选择
,可选择 溶液。能证明不存在
溶液。能证明不存在 的实验现象是
的实验现象是___________ 。
(3)氧化后,从反应体系中分离出 粗产品的操作名称是
粗产品的操作名称是___________ 。
(4)上述流程中,基态原子未成对电子数最多的金属元素名称是___________ 。
(5)向 和
和 混合溶液中通入氯气制备
混合溶液中通入氯气制备 的离子方程式
的离子方程式___________ 。
(6)已知常温下, ,调节FeCl3溶液至
,调节FeCl3溶液至 ,所得溶液中c(Fe3+)=
,所得溶液中c(Fe3+)=___________ 。
 ,含少量
,含少量 、
、 、
、 等杂质)为原料制备
等杂质)为原料制备 (铋酸钠,浅黄色不溶于冷水的固体,是常用试剂),流程如下:
(铋酸钠,浅黄色不溶于冷水的固体,是常用试剂),流程如下: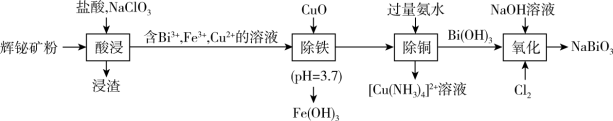
 难溶于水;
难溶于水;②酸浸后,矿粉中的硫元素完全变为硫单质;
回答下列问题:
(1)
 中Cu的化合价为
中Cu的化合价为 反应的离子方程式
反应的离子方程式(2)检验“酸浸”液中是否含
 ,可选择
,可选择 溶液。能证明不存在
溶液。能证明不存在 的实验现象是
的实验现象是(3)氧化后,从反应体系中分离出
 粗产品的操作名称是
粗产品的操作名称是(4)上述流程中,基态原子未成对电子数最多的金属元素名称是
(5)向
 和
和 混合溶液中通入氯气制备
混合溶液中通入氯气制备 的离子方程式
的离子方程式(6)已知常温下,
 ,调节FeCl3溶液至
,调节FeCl3溶液至 ,所得溶液中c(Fe3+)=
,所得溶液中c(Fe3+)=
您最近半年使用:0次
9 . 某实验小组探究SO2与K2FeO4的反应,实验如下。
资料:i.K2FeO4为紫色固体,微溶于KOH溶液;具有强氧化性,在酸性或中性溶液中快速产生O2,在碱性溶液中较稳定。
ii.Fe3+可以与C2O 形成[Fe(C2O4)3]3-;
形成[Fe(C2O4)3]3-;
(1)A中产生SO2的化学方程式为___________ 。
(2)暗红褐色沉淀X可能含Fe3+、OH-、SO 、SO
、SO ,检验如下:
,检验如下:
实验二:向X中加入足量盐酸,沉淀溶解。取少量溶液,滴加KSCN溶液后变红。证明溶液中存在___________ 。另取少量溶液滴加BaCl2溶液,产生白色沉淀,但不能确认含有SO ,原因是
,原因是___________ 。
实验三:向X中加入H2C2O4溶液,沉淀溶解。继续滴加BaCl2溶液,产生白色沉淀,过滤后,向沉淀中加入盐酸,白色沉淀溶解。确认X中不含SO 。
。
实验三中用H2C2O4溶液溶解沉淀的目的是:___________ 。
实验四:向X中加入足量盐酸,沉淀溶解。加入几滴碘水(含淀粉),蓝色立即褪去。静置,一段时间后蓝色复现,振荡,不褪色。
结合离子方程式解释沉淀溶解后的现象:___________ 。
(3)查阅资料:a.Fe3+、SO 、H2O(或OH﹣)会形成配合物HOFeOSO2。
、H2O(或OH﹣)会形成配合物HOFeOSO2。 和O2在金属离子的催化作用下产生具有强氧化性的过一硫酸(HSO
和O2在金属离子的催化作用下产生具有强氧化性的过一硫酸(HSO
①向溶液Y中滴加2滴KSCN溶液,未见红色;再加几滴6mol·L-1盐酸,溶液变红。溶液Y中存在Fe(Ⅲ),但直接滴加KSCN溶液未见红色的原因是___________ 。
②取出部分实验一中的橙色溶液,久置不褪色。结合资料a中过程ii分析实验一中溶液最终“几乎无色”的原因:___________ 。
总结:SO2与K2FeO4发生了氧化还原反应和复分解反应,并且遵循化学反应速率和限度规律。
资料:i.K2FeO4为紫色固体,微溶于KOH溶液;具有强氧化性,在酸性或中性溶液中快速产生O2,在碱性溶液中较稳定。
ii.Fe3+可以与C2O
 形成[Fe(C2O4)3]3-;
形成[Fe(C2O4)3]3-;| 装置 | 操作及现象 |
| 实验一:向B中通入SO2,产生暗红褐色沉淀X和溶液Y(略显红色);继续通入SO2一段时间后,溶液呈红色,继而变为橙色,最终沉淀消失,溶液几乎无色。 |
(1)A中产生SO2的化学方程式为
(2)暗红褐色沉淀X可能含Fe3+、OH-、SO
 、SO
、SO ,检验如下:
,检验如下:实验二:向X中加入足量盐酸,沉淀溶解。取少量溶液,滴加KSCN溶液后变红。证明溶液中存在
 ,原因是
,原因是实验三:向X中加入H2C2O4溶液,沉淀溶解。继续滴加BaCl2溶液,产生白色沉淀,过滤后,向沉淀中加入盐酸,白色沉淀溶解。确认X中不含SO
 。
。实验三中用H2C2O4溶液溶解沉淀的目的是:
实验四:向X中加入足量盐酸,沉淀溶解。加入几滴碘水(含淀粉),蓝色立即褪去。静置,一段时间后蓝色复现,振荡,不褪色。
结合离子方程式解释沉淀溶解后的现象:
(3)查阅资料:a.Fe3+、SO
 、H2O(或OH﹣)会形成配合物HOFeOSO2。
、H2O(或OH﹣)会形成配合物HOFeOSO2。
 和O2在金属离子的催化作用下产生具有强氧化性的过一硫酸(HSO
和O2在金属离子的催化作用下产生具有强氧化性的过一硫酸(HSO
①向溶液Y中滴加2滴KSCN溶液,未见红色;再加几滴6mol·L-1盐酸,溶液变红。溶液Y中存在Fe(Ⅲ),但直接滴加KSCN溶液未见红色的原因是
②取出部分实验一中的橙色溶液,久置不褪色。结合资料a中过程ii分析实验一中溶液最终“几乎无色”的原因:
总结:SO2与K2FeO4发生了氧化还原反应和复分解反应,并且遵循化学反应速率和限度规律。
您最近半年使用:0次
名校
解题方法
10 . 华铁粉的主要成分为醋酸亚铁,可清热解毒,凉血消肿。以粗氯化铁(含少量 )为原料制备华铁粉的流程如下:
)为原料制备华铁粉的流程如下:
 )为原料制备华铁粉的流程如下:
)为原料制备华铁粉的流程如下: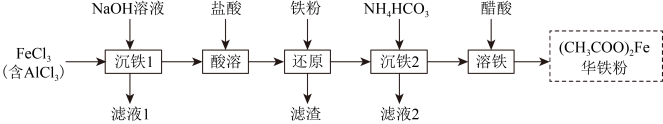
A.“沉铁1”中可用氨水替代 溶液 溶液 |
B.“还原”时加入铁粉的目的是将 转化成 转化成 |
C.滤液2的主要成分是 |
D.“溶铁”的离子方程式为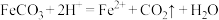 |
您最近半年使用:0次